2019高三·全国·专题练习
解题方法
1 . 无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:
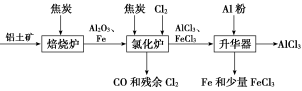
已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)Cl2的电子式________ 。
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为______________ ;炉气中残余的少量Cl2,可用NaOH溶液吸收,其离子方程式为_____________________________________ 。
(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围________ 。
a.低于183 ℃ b.介于183 ℃和315 ℃之间
c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品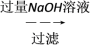 NaAlO2溶液
NaAlO2溶液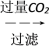 Al(OH)3
Al(OH)3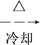 n克Al2O3
n克Al2O3
计算该样品中AlCl3的质量分数________ (结果用m、n表示,不必化简)。

已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)Cl2的电子式
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为
(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围
a.低于183 ℃ b.介于183 ℃和315 ℃之间
c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品
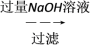 NaAlO2溶液
NaAlO2溶液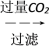 Al(OH)3
Al(OH)3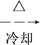 n克Al2O3
n克Al2O3计算该样品中AlCl3的质量分数
您最近一年使用:0次
13-14高三·全国·课时练习
名校
解题方法
2 . 位于短周期的四种元素A、B、C、D,其原子序数依次增大。A在周期表中原子半径最小;B是地壳中含量最高的元素;B、D位于同一主族;C的原子半径在同周期中最大。回答下列问题:
(1)写出由上述元素形成的具有漂白作用的3种物质的化学式:_________ 、_________ 、_________ 。
(2)写出含B元素质量分数最高的化合物的电子式:_____________ 。
(3)分别由A、B、C、D四种元素组成的两种化合物X和Y可以发生反应,试写出该反应的离子方程式:______________________ 。
(4)用电子式表示化合物C2B的形成过程:__________________ 。
(1)写出由上述元素形成的具有漂白作用的3种物质的化学式:
(2)写出含B元素质量分数最高的化合物的电子式:
(3)分别由A、B、C、D四种元素组成的两种化合物X和Y可以发生反应,试写出该反应的离子方程式:
(4)用电子式表示化合物C2B的形成过程:
您最近一年使用:0次
2016-12-09更新
|
167次组卷
|
3卷引用:2014年高考化学一轮复习课后规范训练5-2练习卷
解题方法
3 . 我国化学家侯德榜改革国外的纯碱生产工艺,生产流程示意简图如下:
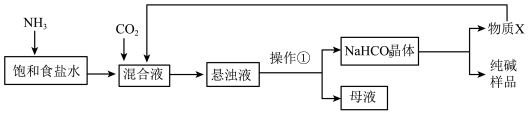
(1)物质X的电子式为_______ ;
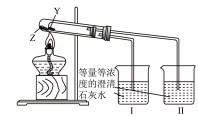
(2)上述转化过程可证明热稳定性:NaHCO3_______ Na2CO3(填“>”、“=”或“<”);如图装置也可比较二者的稳定性,则Z为_______ (填物质名称),烧杯_______ (填“I”或“II”)中溶液变浑浊。
(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为_______ 。
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为_______ %(精确到0.1)。

(1)物质X的电子式为
(2)上述转化过程可证明热稳定性:NaHCO3

(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为
您最近一年使用:0次
2023-02-14更新
|
317次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题
山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题山东省聊城市2022-2023学年高一上学期期末考试化学试题(已下线)专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
4 . “遥遥领先”的华为芯片制造过程用了蚀刻技术。利用NF3进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。该反应微观示意图如下,下列说法不正确的是
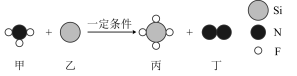

| A.物质丁是空气中含量最多的气体 |
| B.反应生成的丙和丁微粒数之比为1∶1 |
| C.丙物质为气体 |
| D.上述反应为置换反应 |
您最近一年使用:0次
5 . 现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号B:___________ ;C:___________ ;D___________ 。
(2)用元素符号表示 的电子式为
的电子式为___________ 。
(3)C在火焰上灼烧产生的黄光是一种(填字母)___________ 。
a.吸收光谱 b.发射光谱
(4)E元素在元素周期表的位置为:___________ ,属于___________ 区。
(5)E最高能层电子的电子云轮廓形状为___________ 。与其同周期的元素中,基态原子最外层电子数与其相同的全部元素的价电子排布式为___________ 。
(6)某主族元素X的前3级电离能如下表所示,则X位于___________ 族。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有11个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示
 的电子式为
的电子式为(3)C在火焰上灼烧产生的黄光是一种(填字母)
a.吸收光谱 b.发射光谱
(4)E元素在元素周期表的位置为:
(5)E最高能层电子的电子云轮廓形状为
(6)某主族元素X的前3级电离能如下表所示,则X位于
| 元素 | 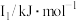 | 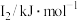 | 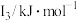 |
| X | 737.7 | 1450.7 | 7732.7 |
您最近一年使用:0次
2023-12-25更新
|
168次组卷
|
2卷引用:陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 2007年11月26日,我国首次月球探测工程第一幅月面图象发布。月球的月壤中含有丰富的3He,月海玄武岩中蕴藏着丰富的Na、Mg、Cu等金属矿产资源和大量的SiO2等。完成下列填空:
(1)3He是高效核能原料,其原子核内中子数为_______ ;3He的电子式为_______ 。
(2)Na的原子结构示意图为_______ ;Na与Na+两种微粒结构上相同的是_______ (选填编号)。
a.质子数 b.电子数 c.电子层数 d.最外层电子数
(3)Mg2+核外电子所占据的电子层中,能量最高的是_______ 层(填符号)。月球上某矿石经处理的MgO中含有少量SiO2,可以用_______ 溶液除去SiO2。
(4)铜元素近似平均相对原子质量计算式为63×69.17%+x×30.83% = 63.62。该计算式中63是指_______ 。x的值为_______ ;x所对应的同位素原子的质量分数_______ (选填“大于”“小于”或“等于”)30.83%。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
a.质子数 b.电子数 c.电子层数 d.最外层电子数
(3)Mg2+核外电子所占据的电子层中,能量最高的是
(4)铜元素近似平均相对原子质量计算式为63×69.17%+x×30.83% = 63.62。该计算式中63是指
您最近一年使用:0次
7 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)W在周期表中的位置是___________ 。
(2)写出化合物Z2R的电子式:___________ 。
(3)写出化合物X2Y2的结构式:___________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是___________ (用元素的离子符号表示)。
(5)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(6)X、Y、Z三种元素形成的化合物是___________ (填化学式),含有化学键的类型是___________ 。
(1)W在周期表中的位置是
(2)写出化合物Z2R的电子式:
(3)写出化合物X2Y2的结构式:
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(6)X、Y、Z三种元素形成的化合物是
您最近一年使用:0次
名校
8 . X、Y、Z、J、R、Q六种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,Y的简单氢化物水溶液呈碱性,J元素的焰色试验呈黄色,X能与J形成离子化合物,且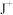 的半径大于
的半径大于 的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为
的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为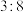 。请回答:
。请回答:
(1)Q元素在周期表中的位置为_______ 。
(2)六种元素原子半径最大的是_______ ,简单离子半径最大的是_______ 。(填元素符号)。
(3)元素的非金属性Z_______ (填“>”或“<”)Q。下列各项中,不能说明这一结论的事实有_______ (填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)R的最高价氧化物与J的最高价氧化物的水化物反应的化学方程式_______ 。
(5)X与Z简单化合物的空间构型为_______ ,用电子式表示X与J化合物的形成过程_______ ;X与Q在一定条件下可以形成极不稳定的原子个数比为 的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:_______ 。
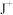 的半径大于
的半径大于 的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为
的半径,R的周期序数等于主族序数,Q的最外层电子数与其电子总数之比为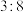 。请回答:
。请回答:(1)Q元素在周期表中的位置为
(2)六种元素原子半径最大的是
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)R的最高价氧化物与J的最高价氧化物的水化物反应的化学方程式
(5)X与Z简单化合物的空间构型为
 的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式:
您最近一年使用:0次
2023-01-16更新
|
324次组卷
|
3卷引用:山西省运城市康杰中学2022-2023学年高一上学期1月期末考试化学试题
名校
9 . 元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表回答问题:
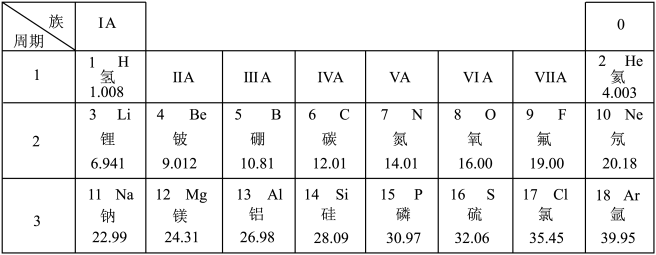
(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为___________ 。
(3)已知某微粒的结构示意图为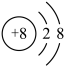 ,请写出该微粒的符号
,请写出该微粒的符号___________ 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为___________ 。
(5)表中Ne和Ar的化学性质相似的原因是___________ 。

(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
| A.门捷列夫 | B.拉瓦锡 | C.道尔顿 | D.阿伏加德罗 |
(3)已知某微粒的结构示意图为
 ,请写出该微粒的符号
,请写出该微粒的符号(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为
(5)表中Ne和Ar的化学性质相似的原因是
您最近一年使用:0次
22-23高一·全国·单元测试
解题方法
10 . A~D为核电荷数小于18的元素,其性质或结构信息如下表:
请根据表中的信息回答下列问题:
(1)四种元素名称为:A_______ ;C_______ 。
(2)B原子的结构示意图:_______ 。
(3)由A、B、D三种元素构成的物质中含有的化学键类型_______ ,写出该物质的电子式:_______ ,写出该物质在水中的电离方程式_______ 。
(4)AC的浓溶液与化合物DCB3的溶液反应生成C的单质,其中的还原反应为_______ →_______ (用化学式表示),每有1 mol DCB3参加反应,电子转移_______ mol。
(5)A~D四种元素的三种元素形成的DBA、DCB、ACB三物质中,属于离子化合物的是_______ (写电子式),属于共价化合物是_______ (写电子式)。
| 元素 | A | B | C | D |
| 性质或结构信息 | 原子核内只有1个质子 | 海水中含量最多,其原子有2个电子层 | 其阴离子是构成食盐的粒子 | 其原子的M电子层上只有1个电子 |
(1)四种元素名称为:A
(2)B原子的结构示意图:
(3)由A、B、D三种元素构成的物质中含有的化学键类型
(4)AC的浓溶液与化合物DCB3的溶液反应生成C的单质,其中的还原反应为
(5)A~D四种元素的三种元素形成的DBA、DCB、ACB三物质中,属于离子化合物的是
您最近一年使用:0次



