名校
解题方法
1 . 物质的分类及物质的结构可以帮助我们更全面的认识物质的性质。
I.如图为氯及其化合物的价类二维图,回答下列问题:
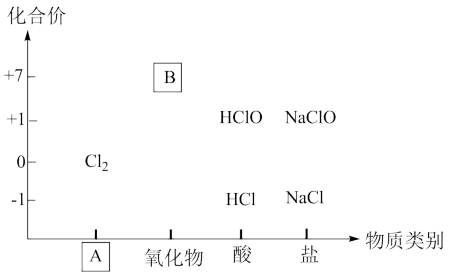
(1)图中A的物质类别为_______ ;B的化学式是_______
(2)关于盐酸与 反应,同学们持不同意见,甲同学认为发生反应:
反应,同学们持不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于_______ 反应(填四大基本反应类型);乙同学则认为发生氧化还原反应: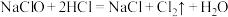 ,反应中
,反应中 体现的性质是
体现的性质是_______ 。最终,丙同学通过实验证明乙同学的看法正确,过程如下:向盛有盐酸的试管中滴加 溶液后,将湿润的有色布条置于试管口,布条出现
溶液后,将湿润的有色布条置于试管口,布条出现_______ 现象。
II.部分主族元素的原子结构特点如下表:
请回答下列问题:
(3)画出W原子的结构示意图:_______
(4)元素X与元素Z相比,非金属性较强的是_______ (填元素名称);写出一个能表示 非金属性强弱关系的反应的化学方程式:
非金属性强弱关系的反应的化学方程式:_______
(5)元素X和元素Y以原子个数比为1∶1化合形成化合物Q,写出Q的电子式:_______ 。元素W和元素Y化合形成化合物M,Q和M的电子总数相等,以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒且在自然界中稳定存在的物质,写出该反应的化学方程式:_______
I.如图为氯及其化合物的价类二维图,回答下列问题:

(1)图中A的物质类别为
(2)关于盐酸与
 反应,同学们持不同意见,甲同学认为发生反应:
反应,同学们持不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于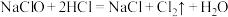 ,反应中
,反应中 体现的性质是
体现的性质是 溶液后,将湿润的有色布条置于试管口,布条出现
溶液后,将湿润的有色布条置于试管口,布条出现II.部分主族元素的原子结构特点如下表:
| 元素 | 原子结构特点 |
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 最外层电子数是次外层电子数的2.5倍 |
(3)画出W原子的结构示意图:
(4)元素X与元素Z相比,非金属性较强的是
 非金属性强弱关系的反应的化学方程式:
非金属性强弱关系的反应的化学方程式:(5)元素X和元素Y以原子个数比为1∶1化合形成化合物Q,写出Q的电子式:
您最近一年使用:0次
名校
解题方法
2 . 下表是元素周期表的一部分,用化学用语回答下列有关问题:
(1)写出下列元素符号:①_______ ,画出原子的结构示意图:④_______ 。
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是_______ 。
(3)元素⑦与元素⑧相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成_______ (填“离子”或“共价”)化合物,用电子式表示其形成过程:_______ 。①的+4价氧化物被烧碱溶液吸收生成两种钠盐的离子方程是_______ 。
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种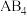 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:_______ 。
(6) 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成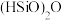 等,写出该反应的化学方程式
等,写出该反应的化学方程式_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑧ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是
(3)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种
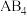 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:(6)
 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成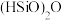 等,写出该反应的化学方程式
等,写出该反应的化学方程式
您最近一年使用:0次
3 . 现有部分短周期主族元素的性质或原子结构如下表:
(1)元素Y在周期表中的位置_________ (周期、族)。
(2)XN2的电子式是:_________ ,Y的简单氢化物的结构式_________ 。
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_________ 。
(4)用电子式表示WZ的形成过程_________ 。
(5)元素Z和T相比,非金属性较强的是____________________ ,下列表述中能证明这一事实的是_________。
(6)写出W单质和H2O反应的化学方程式_________ ,所得溶液的溶质是_________ 化合物(填“离子”或“共价”)。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大的元素 |
| N | 原子序数比T小,且与T在同一主族 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正价为+7价 |
(2)XN2的电子式是:
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(4)用电子式表示WZ的形成过程
(5)元素Z和T相比,非金属性较强的是
| A.常温下Z单质和T单质状态不同 |
| B.Z的氢化物比T的氢化物稳定 |
| C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应 |
您最近一年使用:0次
2016-12-09更新
|
261次组卷
|
2卷引用:2015-2016学年吉林东北师大附属实验高一下期末化学试卷
解题方法
4 . 推断题
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
(1)写出下列元素名称:A_____ B____ C____ D_____ E___ F______________________________
(2)写出元素C的离子结构示意图____________ 。
(3)D、E、F的简单离子半径由大到小的顺序是___________________ 。
(4)B与C形成的化合物,既含有离子键又含有非极性键,该化合物的电子式为_______________ 。
(5)A、C、E三种元素形成的具有漂白性的化合物,该化合物的结构式为___________ 。
(6)D与E形成的化合物的类别是________________ (填共价化合物或离子化合物)。
(7)能证明C的非金属性比F强的实验事实是
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | A的单质是密度最小的物质 |
| B | B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D与B同周期,该周期中D的简单离子半径最小 |
| E | B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F | F元素最高正价与最低负价的代数和为4 |
(2)写出元素C的离子结构示意图
(3)D、E、F的简单离子半径由大到小的顺序是
(4)B与C形成的化合物,既含有离子键又含有非极性键,该化合物的电子式为
(5)A、C、E三种元素形成的具有漂白性的化合物,该化合物的结构式为
(6)D与E形成的化合物的类别是
(7)能证明C的非金属性比F强的实验事实是
您最近一年使用:0次
名校
解题方法
5 . A、B、C、D、E是原子序数由小到大排列的五种短周期元素,其中A、B、C、D的原子序数之和为32,A是元素周期表中原子半径最小的元素,B、C左右相邻,C、D位于同主族。
(1)E元素原子的结构示意图为:_____ ,写出一个能证明D、E两元素非金属性强弱的事实或反应方程式:________________________ 。
(2)A与C组成的化合物的电子式为_____ ,其中含有的化学键为_____ (填“极性键”“非极性键”“离子键”)。(若有多种可能,只需答出其中一种物质)
(3)A、B、C、D四种元素中的三种能组成一种强酸,该强酸的稀溶液能与铜反应,其中起氧化性作用的酸占消耗酸总物质的量的百分比是_____ 。
(4)由A、B、C、D四种元素组成的一种离子化合物X。
①已知1mol X能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下X与NaOH浓溶液反应的离子方程式:________________________ 。
②又知X既能与盐酸反应,又能与氯水反应,写出X的化学式:____________ 。
(1)E元素原子的结构示意图为:
(2)A与C组成的化合物的电子式为
(3)A、B、C、D四种元素中的三种能组成一种强酸,该强酸的稀溶液能与铜反应,其中起氧化性作用的酸占消耗酸总物质的量的百分比是
(4)由A、B、C、D四种元素组成的一种离子化合物X。
①已知1mol X能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下X与NaOH浓溶液反应的离子方程式:
②又知X既能与盐酸反应,又能与氯水反应,写出X的化学式:
您最近一年使用:0次
2016-12-09更新
|
395次组卷
|
2卷引用:2014-2015吉林省松原市扶余县一中高一下学期第一次月考化学试卷
9-10高一下·北京·期末
解题方法
6 . 现有部分短周期元素的性质或原子结构如下表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置___________________________ ;
②B元素原子结构示意图_____________________________ ;
③C单质分子的电子式__________________ ;用电子式表示A和B元素组成的化合物的形成过程________________________________________________________ ;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素____________ 。
(2)元素D与元素A相比,非金属性较强的是__________ (用元素符号表示),下列表述中能证明这一事实的是________________ (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是_____________________ (写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
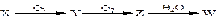
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:_____ ;生成该白色沉淀的化学方程式为_________ ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:_________ 。
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置
②B元素原子结构示意图
③C单质分子的电子式
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
(2)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
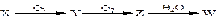
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:
您最近一年使用:0次
名校
解题方法
7 . 十九世纪初,科学家用氰酸银 与
与 在一定条件下反应制得尿素
在一定条件下反应制得尿素 实现了由无机物到有机物的合成。下列有关说法正确的是
实现了由无机物到有机物的合成。下列有关说法正确的是
 与
与 在一定条件下反应制得尿素
在一定条件下反应制得尿素 实现了由无机物到有机物的合成。下列有关说法正确的是
实现了由无机物到有机物的合成。下列有关说法正确的是A. 电子式为 电子式为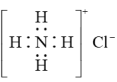 | B.第一电离能: |
| C.氰酸铵与尿素互为同分异构体 | D.尿素中所有原子可能处于同一平面 |
您最近一年使用:0次
2024-04-19更新
|
454次组卷
|
2卷引用:东北三省2023-2024学年高三下学期高考模拟试题(一)
解题方法
8 . 下列有关化学用语的说法正确的是
A.碳酸氢钠在水溶液中的电离方程式为:NaHCO3 Na++ Na++ |
B.基态氮原子的轨道表示式: |
C.顺-2-丁烯的球棍模型: |
| D.HClO的结构式为H−O−Cl |
您最近一年使用:0次
2024-01-13更新
|
316次组卷
|
3卷引用:吉林省吉林市2023-2024学年高三上学期第二次模拟考试 化学试题
吉林省吉林市2023-2024学年高三上学期第二次模拟考试 化学试题吉林省吉林市2023-2024学年高三上学期第二次模拟考试化学试题(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
解题方法
9 . 下列说法中正确的是
A.电石的电子式: |
| B.可以用酸性高锰酸钾溶液除去甲烷中混有的乙烯 |
C.乙炔的球棍模型: |
D. 的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷 |
您最近一年使用:0次
名校
10 . 如图是立方烷的球棍模型,下列有关说法不正确的是


| A.它的一氯代物只有一种 | B.它的二氯代物有两种 |
| C.它的核磁共振氢谱图上只有一组峰 | D.它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
您最近一年使用:0次
2022-12-20更新
|
224次组卷
|
3卷引用:吉林省长春市第五中学2022-2023学年高二下学期第一学程考试化学试题



