1 . 现有1~20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:
(1)元素A的原子核外电子的运动状态有___________ 种,价层电子轨道表示式为___________ 。B的离子与D的离子相互组合形成的干燥剂的化学式是___________ 。
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式___________ (用元素符号表示)。
(3)元素A与元素D相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.D的氢化物水溶液酸性比A的氢化物水溶液酸性强
(4)C的氢化物与A的最高价氧化物对应的水化物反应的化学方程式是___________ 。
| 元素 | 物质性质或微粒结构 |
| A | M层上有2对成对电子 |
| B | B的离子与D的离子具有相同电子层结构,且可以相互组合形成干燥剂 |
| C | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式
(3)元素A与元素D相比,非金属性较强的是
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.D的氢化物水溶液酸性比A的氢化物水溶液酸性强
(4)C的氢化物与A的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
名校
解题方法
2 . 针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是_______ (填元素符号),酸性最强的最高价氧化物对应水化物是______ (填化学式)。
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程___________ 。
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)非金属性①_____ ⑧(填“>”或“<”),请设计实验证明_________ (用化学方程式表示)。
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(6)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)最活泼的金属元素是
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)非金属性①
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(6)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
您最近一年使用:0次
3 . 下列为元素周期表的一部分,请回答下列问题:
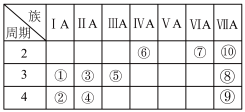
(1)①②⑤中,最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(2)②③④⑧中形成的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)若元素⑦的氢化物分子中原子个数比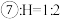 ,则该氢化物的电子式为
,则该氢化物的电子式为___________ ,该氢化物的空间结构为___________ 形(填“直线”或“V”)。
(4)已知同一主族元素具有相似的化学性质,则常温下元素②的过氧化物与水反应的化学方程式为___________ 。
(5)⑧的最高价氧化物对应的水化物化学式为___________ ,画出⑨的原子结构示意图___________ ,请设计实验证明⑧与⑨的单质氧化性强弱___________ 。
(6)⑧⑨⑩的气态氢化物中,最稳定的是___________ (填化学式)。

(1)①②⑤中,最高价氧化物对应的水化物碱性最强的是
(2)②③④⑧中形成的简单离子半径由大到小的顺序是
(3)若元素⑦的氢化物分子中原子个数比
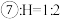 ,则该氢化物的电子式为
,则该氢化物的电子式为(4)已知同一主族元素具有相似的化学性质,则常温下元素②的过氧化物与水反应的化学方程式为
(5)⑧的最高价氧化物对应的水化物化学式为
(6)⑧⑨⑩的气态氢化物中,最稳定的是
您最近一年使用:0次
解题方法
4 . 某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
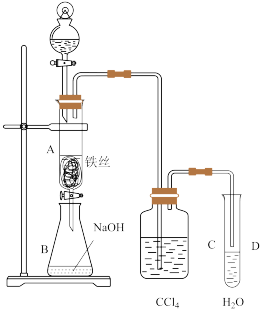
(1)写出A中反应的化学方程式_____ 。
(2)观察到A中的现象是_____ 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是______ ,写出有关的化学方程式_____ 。
(4)C中盛放CCl4的作用是_____ 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_____ ,现象是_____ 。
(6)羟基的电子式:______ 。

(1)写出A中反应的化学方程式
(2)观察到A中的现象是
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(4)C中盛放CCl4的作用是
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入
(6)羟基的电子式:
您最近一年使用:0次
2022-12-19更新
|
294次组卷
|
2卷引用:陕西省安康市汉滨区江北高级中学2020-2021学年高二下学期期中考试化学试题
名校
5 . 下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)最高价氧化物对应的水化物碱性最强的元素在周期表中的位置是___________ 。
(2)元素②⑥最高价氧化物对应的水化物之间反应的离子方程式为___________ 。
(3)能证明元素⑨⑩的非金属性相对强弱的实验事实是___________ (用离子方程式表示)。
(4)元素③⑤⑧⑨对应的简单离子的半径由大到小的排序为___________ (用相应的离子符号排序)。
(5)元素①和⑦以原子个数比1:1形成的化合物的电子式为___________ ;元素①和②形成的化合物的电子式为___________ ,该化合物与水反应的化学方程式是___________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ⑦ | |||||||
| 三 | ② | ④ | ⑥ | ⑧ | ⑨ | |||
| 四 | ③ | ⑤ | ⑩ |
(1)最高价氧化物对应的水化物碱性最强的元素在周期表中的位置是
(2)元素②⑥最高价氧化物对应的水化物之间反应的离子方程式为
(3)能证明元素⑨⑩的非金属性相对强弱的实验事实是
(4)元素③⑤⑧⑨对应的简单离子的半径由大到小的排序为
(5)元素①和⑦以原子个数比1:1形成的化合物的电子式为
您最近一年使用:0次
解题方法
6 . 已知W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。X和Ne的核外电子数相差1,且X和W能形成化合物原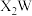 ;在Z所在的周期中,Z元素的最高价氧化物的水化物酸性最强;四种元素的最外层电子数之和为20,请回答下列问题:
;在Z所在的周期中,Z元素的最高价氧化物的水化物酸性最强;四种元素的最外层电子数之和为20,请回答下列问题:

(1)Y元素的名称为_______ 。
(2)W、X、Z三种元素形成具有漂白性的化合物的化学式为_______ ;W的氢化物中既含有极性键又含有非极性键的氢化物的电子式为_______ 。
(3)Y和Z的非金属性强弱:Y_______ Z(填“>”或“<”),写出一个可以证明该结论的化学方程式:_______ 。
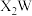 ;在Z所在的周期中,Z元素的最高价氧化物的水化物酸性最强;四种元素的最外层电子数之和为20,请回答下列问题:
;在Z所在的周期中,Z元素的最高价氧化物的水化物酸性最强;四种元素的最外层电子数之和为20,请回答下列问题:
(1)Y元素的名称为
(2)W、X、Z三种元素形成具有漂白性的化合物的化学式为
(3)Y和Z的非金属性强弱:Y
您最近一年使用:0次
名校
解题方法
7 . 氰化钠化学式为NaCN(C元素+2价,N元素-3价),氰化钠是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是____________________________________________ 。
(2)氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3═NaSCN+Na2SO3;已知:NaSCN中S为-2价,写出SCN-的电子式___________ 。
(3)CN-中C元素显+2价,N元素显-3价,说明非金属性N>C,请设计实验证明:_____________ 。
(4)同时HCN又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如表:
①向NaCN溶液中通入少量CO2,发生的离子反应为_______________________________ 。
②等体积、等物质的量浓度的HCOONa和NaCN溶液中所含离子总数的关系是:HCOONa______ NaCN。(填“>”、“<”或“=”)
(5)常温下,用0.10mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。

①常温时醋酸的电离常数为1.96×10-5,0.10 mol·L-1CH3COOH溶液中c(H+)=__________ mol·L-1。
②在①所示的溶液中溶质为_____
③在①和②所示溶液中c(CH3COO-)-c(CN-)_______ (填“>”、“<”或“=”)c(HCN)-c(CH3COOH)。
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是
(2)氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3═NaSCN+Na2SO3;已知:NaSCN中S为-2价,写出SCN-的电子式
(3)CN-中C元素显+2价,N元素显-3价,说明非金属性N>C,请设计实验证明:
(4)同时HCN又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
②等体积、等物质的量浓度的HCOONa和NaCN溶液中所含离子总数的关系是:HCOONa
(5)常温下,用0.10mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。

①常温时醋酸的电离常数为1.96×10-5,0.10 mol·L-1CH3COOH溶液中c(H+)=
②在①所示的溶液中溶质为
③在①和②所示溶液中c(CH3COO-)-c(CN-)
您最近一年使用:0次
2018-04-12更新
|
241次组卷
|
2卷引用:陕西省榆林市2018届高三第三次模拟测试理综化学试题
名校
8 . 纳米银粒是一种杀菌剂,对沙眼衣原体等数十种致病微生物都有强烈的抑制和杀灭作用,而且不会产生耐药性。可通过肼(N2H4)还原银氨溶液制备纳米颗粒。具体步骤如下:
Ⅰ.在洁净的试管中加入2%AgNO3溶液10mL,逐滴加入2%稀氨水,边滴边振荡至沉淀恰好完全溶解。
Ⅱ.取10mLN2H4溶液于大烧杯中并加入5g分散剂混合均匀,加热至55~60℃。
Ⅲ.将Ⅰ中所得溶液滴加到Ⅱ中所得的分散系中,反应15min。
Ⅳ.冷却、分离、洗涤、干燥得纳米银粉。
已知:AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的Ag2O。
回答下列问题:
(1)N2H4是一种常用还原剂,写出N2H4的电子式:___________ 。
(2)步骤Ⅲ发生反应的离子方程式为___________ ;验证纳米银颗粒生成的方法是___________ 。
(3)下列有关说法错误的是___________(填字母)。
(4)步骤I使用的AgNO3溶液需用HNO3酸化,其主要目的是___________ 。
(5)若用AgNO3溶液与维生素C以及明胶在一定条件下也可制得纳米银颗粒。
①该体系中维生素C的作用为___________ 。
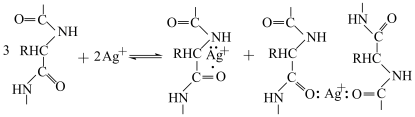
②已知明胶可与溶液中Ag+形成如下配合物,[Ag(明胶)]+得电子后,明胶继续吸附在银核表面。
明胶在该体系中充当___________ 。
Ⅰ.在洁净的试管中加入2%AgNO3溶液10mL,逐滴加入2%稀氨水,边滴边振荡至沉淀恰好完全溶解。
Ⅱ.取10mLN2H4溶液于大烧杯中并加入5g分散剂混合均匀,加热至55~60℃。
Ⅲ.将Ⅰ中所得溶液滴加到Ⅱ中所得的分散系中,反应15min。
Ⅳ.冷却、分离、洗涤、干燥得纳米银粉。
已知:AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的Ag2O。
回答下列问题:
(1)N2H4是一种常用还原剂,写出N2H4的电子式:
(2)步骤Ⅲ发生反应的离子方程式为
(3)下列有关说法错误的是___________(填字母)。
| A.步骤Ⅰ,银氨溶液也可用AgCl与氨水反应制得 |
| B.步骤Ⅱ,可采用水浴加热 |
| C.步骤Ⅲ,为了加快反应速度,可以一次性加入银氨溶液 |
| D.步骤Ⅳ,洗涤时可先水洗,再用乙醇洗涤 |
(4)步骤I使用的AgNO3溶液需用HNO3酸化,其主要目的是
(5)若用AgNO3溶液与维生素C以及明胶在一定条件下也可制得纳米银颗粒。
①该体系中维生素C的作用为
②已知明胶可与溶液中Ag+形成如下配合物,[Ag(明胶)]+得电子后,明胶继续吸附在银核表面。

明胶在该体系中充当
您最近一年使用:0次
解题方法
9 . 碳酸镧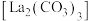 可用于治疗高磷酸盐血症,其制备的化学方程式为:
可用于治疗高磷酸盐血症,其制备的化学方程式为: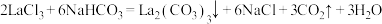 。下列相关微粒的说法正确的是
。下列相关微粒的说法正确的是
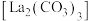 可用于治疗高磷酸盐血症,其制备的化学方程式为:
可用于治疗高磷酸盐血症,其制备的化学方程式为: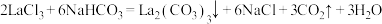 。下列相关微粒的说法正确的是
。下列相关微粒的说法正确的是A.镧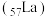 含有的中子数是57 含有的中子数是57 | B. 的球棍模型为 的球棍模型为 |
C. 的结构示意图: 的结构示意图: | D.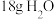 中有 中有 的电子 的电子 |
您最近一年使用:0次
10 . 下列说法不正确的是
| A.CH3—CH=CH2和CH2=CH2的最简式相同 | B.用分液的方法分离水和四氯化碳 |
| C.乙二醇和丙三醇互为同系物 | D.用酒精清洗沾到皮肤上的苯酚 |
您最近一年使用:0次
2023-06-29更新
|
40次组卷
|
2卷引用:陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题



