名校
1 . 化学用语是化学知识的重要组成部分。下列有关化学用语的描述错误的是
| A.乙醇的结构简式:CH3CH2OH | B.甲醛的结构简式:HCOH |
C.乙烯的球棍模型: | D.2-甲基-2-丁烯的键线式: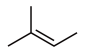 |
您最近半年使用:0次
名校
解题方法
2 . 2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”元素Mc可由反应: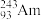 +
+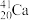 =
=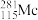 +3
+3 得到。
得到。
(1)该元素的质子数为___________ 。287Mc与288Mc互为________ 。
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:__________ ,该分子内存在的共价键类型有___________ 。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为_______ ,+5价简单含氧酸的化学式为_________ 。
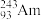 +
+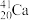 =
=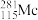 +3
+3 得到。
得到。(1)该元素的质子数为
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为
您最近半年使用:0次
解题方法
3 . 下列化学用语表述正确的是
A. 结构式为 结构式为 | B. 结构示意图为 结构示意图为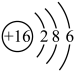 |
C. 电子式为: 电子式为: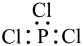 | D.中子数为8的氧原子: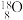 |
您最近半年使用:0次
名校
解题方法
4 . 某汽车安全气囊的产气药剂主要含有 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。
① 的电子式为
的电子式为_______ 。
②Na与冷水常温下发生反应,请写出该反应的化学方程式_______ 。
(2) 含有的化学键类型为
含有的化学键类型为_______ 。
(3)从结构组成的分类, 属于
属于_______ (选填“离子化合物”或“共价化合物”),请写出鉴别离子化合物和共价化合物的方法:_______ 。
(4)某些安全气囊产气药剂中含 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: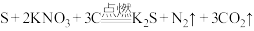
①标出该化学方程式电子转移的方向和数目_______ 。
②其中生成物 的电子式为
的电子式为_______ ; 的结构式为
的结构式为_______ 。
(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是_______ ,该元素单核负离子的结构示意图为_______ 。
 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。①
 的电子式为
的电子式为②Na与冷水常温下发生反应,请写出该反应的化学方程式
(2)
 含有的化学键类型为
含有的化学键类型为(3)从结构组成的分类,
 属于
属于(4)某些安全气囊产气药剂中含
 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: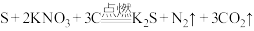
①标出该化学方程式电子转移的方向和数目
②其中生成物
 的电子式为
的电子式为 的结构式为
的结构式为(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是
您最近半年使用:0次
2024·上海·模拟预测
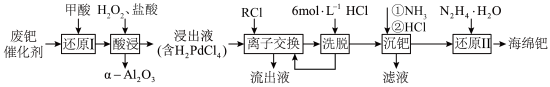
5 . 钯催化剂(主要成分为Pd、α-Al2O3,还含少量铁、铜等)是石油化工中催化加氢和催化氧化等反应的重要催化剂。一种从废钯催化剂中回收海绵钯的工艺流程如下:
②常温下,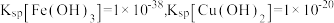 。
。
回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原___________ (填化学式)。
(2)“酸浸”过程中Pd转化的离子方程式为___________ 。
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为___________ 。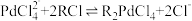 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是___________ 。
(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液) [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为___________ (填化学式)。
(6)N2H4的电子式为___________ 。
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为___________ 。
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。
②常温下,
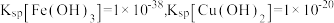 。
。回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原
(2)“酸浸”过程中Pd转化的离子方程式为
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为

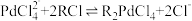 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液)
 [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为(6)N2H4的电子式为
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。

| A.H2O2中存在极性键和非极性键 |
| B.[PdCl4]2-中Pd2+提供空轨道形成配位键 |
| C.反应①、②、③均属于氧化还原反应 |
| D.等物质的量的H2和O2发生反应时,反应①和反应②转移的电子数之比为1:1 |
您最近半年使用:0次
名校
6 . 氮肥的大量使用排出的废水是造成河流及湖泊富营养化的主要因素之一、氨氮废水中的氮元素多以 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。
1.写出 的电子式
的电子式___________ 。
2.阴极生成H2O2的电极反应为:___________ 。氨氮氧化生成2.24LN2(标准状况),转移电子数为:___________ 。
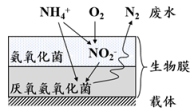
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。___________ 。
 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。1.写出
 的电子式
的电子式2.阴极生成H2O2的电极反应为:
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。
您最近半年使用:0次
名校
7 .  的电子式为
的电子式为___________ 。
 的电子式为
的电子式为
您最近半年使用:0次
名校
解题方法
8 .  的电子式为
的电子式为___________ 。 可用空气和
可用空气和 为原料直接制备。在与熔融金属
为原料直接制备。在与熔融金属 反应前,空气需依次通过
反应前,空气需依次通过___________ 、___________ 。
A.浓硫酸 B.饱和食盐水 C. 溶液 D.
溶液 D. 溶液
溶液
 的电子式为
的电子式为 可用空气和
可用空气和 为原料直接制备。在与熔融金属
为原料直接制备。在与熔融金属 反应前,空气需依次通过
反应前,空气需依次通过A.浓硫酸 B.饱和食盐水 C.
 溶液 D.
溶液 D. 溶液
溶液
您最近半年使用:0次
名校
解题方法
9 . 土壤中的硝酸盐会被细菌分解。有一种细菌是利用土壤中的硫化物来分解硝酸盐,其主要化学反应原理是:
(1) 、
、 、
、 、O元素的原子半径从大到小的顺序是
、O元素的原子半径从大到小的顺序是_______ 。
(2)上述反应中的各物质属于共价化合物是_______ ;氧化剂是_______ 。氮气的电子式是_______ 。
(3)非金属性S_______ O(写“ ”或“
”或“ ”)。用一个化学方程式证明硫与氧的非金属性强弱:
”)。用一个化学方程式证明硫与氧的非金属性强弱:_______ 。
(4)配平上述反应方程式,并标出电子转移的方向和数目。_______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______

(1)
 、
、 、
、 、O元素的原子半径从大到小的顺序是
、O元素的原子半径从大到小的顺序是(2)上述反应中的各物质属于共价化合物是
(3)非金属性S
 ”或“
”或“ ”)。用一个化学方程式证明硫与氧的非金属性强弱:
”)。用一个化学方程式证明硫与氧的非金属性强弱:(4)配平上述反应方程式,并标出电子转移的方向和数目。
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
您最近半年使用:0次
名校
解题方法
10 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
 (条件略)
(条件略)
1.写出 的电子式
的电子式___________ 。
2.能证明 是离子化合物的事实是___________。
是离子化合物的事实是___________。
3.下列说法正确的是___________。
4.下列说法中正确的是___________。
 (条件略)
(条件略)1.写出
 的电子式
的电子式2.能证明
 是离子化合物的事实是___________。
是离子化合物的事实是___________。| A.常温下是固体 | B.易溶于水 | C.水溶液能导电 | D.熔融态能导电 |
A. 和 和 溶于水时都会破坏离子键 溶于水时都会破坏离子键 |
B. 能电离出 能电离出 和 和 ,所以 ,所以 是离子化合物 是离子化合物 |
C. 中每个原子的最外层都具有8电子的稳定结构 中每个原子的最外层都具有8电子的稳定结构 |
D. 是共价分子,液氮汽化时破坏共价键和分子间作用力 是共价分子,液氮汽化时破坏共价键和分子间作用力 |
| A.离子化合物中一定只有离子键 | B.共价化合物中一定只有共价键 |
| C.氯化氢溶于水时会破坏离子键 | D.蔗糖溶于水时破坏分子间作用力 |
您最近半年使用:0次



