名校
1 . 已知X、Y、Z、R均为元素周期表中的短周期主族元素,它们具有如下特征:
(1)Z在元素周期表的位置_______ 。
(2)R的+1价含氧酸的电子式_______ 。
(3)Y的简单氢化物不能用Y的最高价氧化物对应水化物的浓溶液干燥的原因是_______ 。(用方程式表达)
(4)某同学设计了如下装置来探究X、Y、Z元素的非金属性强弱。

①试管D中盛放_______ 溶液。
②酸性KMnO4溶液的作用是_______ 。D中实验现象为_______ 。
③另一同学从实验目的上分析认为该实验设计部分正确,即该实验能够得出的结论仅为_______ 。
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 最高正价和最低负价代数和为4 |
| Z | 最高价氧化物对应水化物难溶于水,是一种很弱的酸 |
| R | M层上有7个电子 |
(2)R的+1价含氧酸的电子式
(3)Y的简单氢化物不能用Y的最高价氧化物对应水化物的浓溶液干燥的原因是
(4)某同学设计了如下装置来探究X、Y、Z元素的非金属性强弱。

①试管D中盛放
②酸性KMnO4溶液的作用是
③另一同学从实验目的上分析认为该实验设计部分正确,即该实验能够得出的结论仅为
您最近一年使用:0次
名校
解题方法
2 . 下表列出9种元素在周期表中的位置,请按要求回答问题。
(1)⑦的简单离子的结构示意图是______ 。表中标注的元素的最高价氧化物对应的水化物中碱性最强的碱是_____ (填写化学式)。③、④、⑨三种元素按原子半径由大到小的顺序排列为 ______ (用元素符号表示)。
(2)元素②的气态氢化物的电子式是_______ 。由3个元素②的原子组成带一个单位负电荷的阴离子中含有_______ 个电子。写出该元素氢化物与其最高价氧化对应水化物反应的离子方程式_____________ 。
(3)⑦、⑧两元素简单离子还原性强弱为______ (填离子符号)。
(4)某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在A、B两只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的③、⑨元素单质,观察现象。甲同学设计实验的目的是_____ 。写出元素⑨的单质与水反应的化学方程式为________ 。
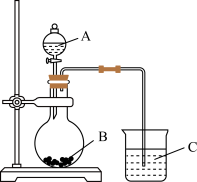
Ⅱ.乙同学设计如图装置以验证①、⑥、⑦元素的非金属性强弱。为了达到实验目的,仪器A、B、C分别选择的药品为A______ 、B______ 、C______ ;烧杯中发生反应的离子方程式为______________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
(2)元素②的气态氢化物的电子式是
(3)⑦、⑧两元素简单离子还原性强弱为
(4)某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在A、B两只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的③、⑨元素单质,观察现象。甲同学设计实验的目的是

Ⅱ.乙同学设计如图装置以验证①、⑥、⑦元素的非金属性强弱。为了达到实验目的,仪器A、B、C分别选择的药品为A
您最近一年使用:0次
2017-05-07更新
|
170次组卷
|
2卷引用:福建省永安市第一中学2016-2017学年高一下学期期中考试化学试题
名校
解题方法
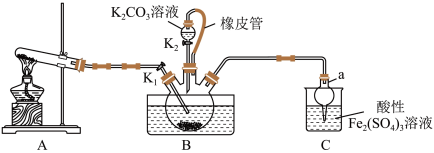
3 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: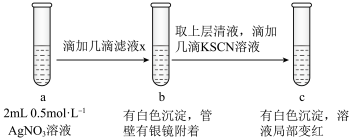
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
解题方法
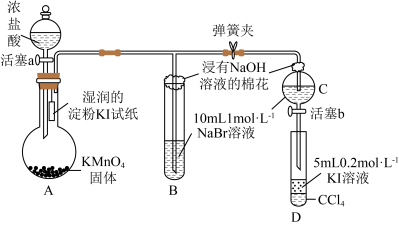
4 . 为证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
② 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。
实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
(1)NaOH的电子式为___________ 。
(2)A装置中制备氯气的离子方程式为___________ ,HCl的作用是做___________ 。
(3)B装置中主要反应的化学方程式为___________ 。
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是___________ 。
(5)过程③的实验目的是___________ 。
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:___________ 。
(7)下列事实能说明元素Y的非金属性比硫元素强的是___________ 。
a.Y单质通入 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊
b.与 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多
c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
②
 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
(1)NaOH的电子式为
(2)A装置中制备氯气的离子方程式为
(3)B装置中主要反应的化学方程式为
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是
(5)过程③的实验目的是
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:
(7)下列事实能说明元素Y的非金属性比硫元素强的是
a.Y单质通入
 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊b.与
 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
您最近一年使用:0次
名校
解题方法
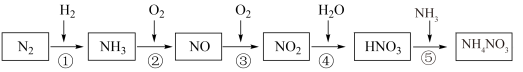
5 . 氮元素及其化合物的转化关系如图所示:___________ ,写出 的电子式
的电子式___________ 。
(2)浓、稀 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:___________ 。
(3)氮氧化物 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。 ,反应的化学方程式为
,反应的化学方程式为___________ ;装置B内的试剂是___________ 。
②在装置 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为___________ 。
③工厂里常采用 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:___________ 。
④用不同浓度的 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量) 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是___________ 。
(4) 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:___________ (写出操作步骤、现象和结论)。
 的电子式
的电子式(2)浓、稀
 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:(3)氮氧化物
 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。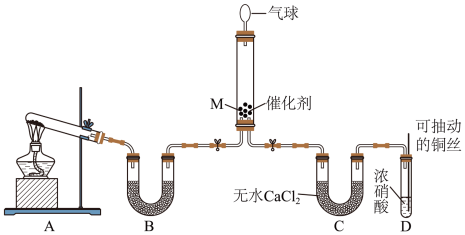
 ,反应的化学方程式为
,反应的化学方程式为②在装置
 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为③工厂里常采用
 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:④用不同浓度的
 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量)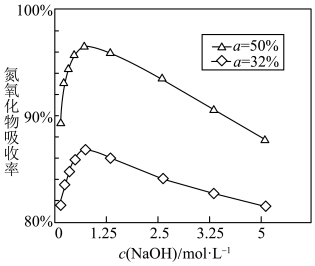
 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(4)
 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
您最近一年使用:0次
名校
6 . 氮是自然界中生物体生命活动不可缺少的重要元素,其化合物种类丰富。
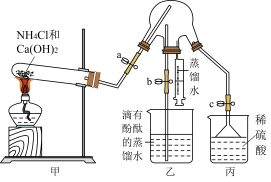
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题: 的电子式为
的电子式为___________ 。
(2)试管内发生反应的化学方程式为___________ 。
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是___________ 。
②一段时间后, 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为___________ 。
③为提高乙装置中实验的成功率,将盛放有___________ 的干燥管连接在甲、乙装置之间。
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。___________ (填“ⅰ”“ⅱ”或“ⅲ”)。
(5)写出“氧化炉”中反应的化学方程式___________ 。
(6)“吸收塔”排出的尾气中会含有NO、 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整:______ 。
 ___________
___________ 。
。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题:
 的电子式为
的电子式为(2)试管内发生反应的化学方程式为
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是
②一段时间后,
 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为③为提高乙装置中实验的成功率,将盛放有
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。
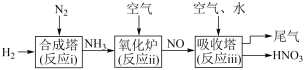
(5)写出“氧化炉”中反应的化学方程式
(6)“吸收塔”排出的尾气中会含有NO、
 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整: ___________
___________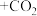 。
。
您最近一年使用:0次
7 . 菠菜富含铁元素, 岁青少年每日合理摄入铁量为
岁青少年每日合理摄入铁量为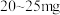 。某化学小组针对菠菜中含铁量进行如下实验。
。某化学小组针对菠菜中含铁量进行如下实验。
(一)实验目的: 菠菜含铁量是否满足青少年日常所需。
菠菜含铁量是否满足青少年日常所需。
(二)实验方案:
I.取适量新鲜菠菜,剪碎后在研钵中研磨,并分成三等份。实验操作和现象记录如下:
(1)灼烧菠菜时,不需要用到下列仪器中的_________(填序号)。
(2) 的电子式为
的电子式为_________ ;实验三中 参与的最主要反应的离子方程式为
参与的最主要反应的离子方程式为__________________ 。可选用_________ 替换实验三中的 和盐酸。
和盐酸。
(3)实验中, 溶液用来检测
溶液用来检测_________ 离子。
Ⅱ.菠菜中含铁量的测定,实验步骤如下:
①取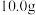 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
②向灰分中加入 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
③将合并液定容成 待测液,测得铁离子的浓度为
待测液,测得铁离子的浓度为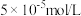 。
。
(4)根据实验数据计算菠菜含铁量为_________ 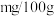 。
。 菠菜含铁量
菠菜含铁量_________ (填“能”或“不能”)满足 岁青少年日常所需。
岁青少年日常所需。
 岁青少年每日合理摄入铁量为
岁青少年每日合理摄入铁量为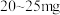 。某化学小组针对菠菜中含铁量进行如下实验。
。某化学小组针对菠菜中含铁量进行如下实验。(一)实验目的:
 菠菜含铁量是否满足青少年日常所需。
菠菜含铁量是否满足青少年日常所需。(二)实验方案:
I.取适量新鲜菠菜,剪碎后在研钵中研磨,并分成三等份。实验操作和现象记录如下:
实验 | 操作步骤 | 现象 |
实验一 | 适量蒸馏水浸泡,过滤,取滤液,加 溶液后加入适量 溶液后加入适量 ,再次加入 ,再次加入 溶液 溶液 | 均无明显现象 |
实验二 | 充分灼烧,加适量盐酸浸泡,取滤液,加 溶液 溶液 | 极浅的红色 |
实验三 | 充分灼烧,加适量盐酸、 浸泡,取滤液,加 浸泡,取滤液,加 溶液 溶液 | 较深的红色 |
| A.蒸发皿 | B.坩埚 | C.酒精灯 | D.坩埚钳 |
 的电子式为
的电子式为 参与的最主要反应的离子方程式为
参与的最主要反应的离子方程式为 和盐酸。
和盐酸。(3)实验中,
 溶液用来检测
溶液用来检测Ⅱ.菠菜中含铁量的测定,实验步骤如下:
①取
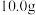 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。②向灰分中加入
 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并。③将合并液定容成
 待测液,测得铁离子的浓度为
待测液,测得铁离子的浓度为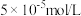 。
。(4)根据实验数据计算菠菜含铁量为
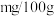 。
。 菠菜含铁量
菠菜含铁量 岁青少年日常所需。
岁青少年日常所需。
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
解题方法
8 . A、B、C、D、E为原子序数依次增大的短周期主族元素,A与E同主族,A与C组成的的一种化合物为最常见的温室气体,D+核外电子排布与C2-相同。试回答( 涉及的物质或微粒均用化学式表示):
提示:硝酸是一种易挥发的强酸。
(1)元素E在元素周期表中的位置是_______ ;
(2)与元素D的简单离子所含电子数和质子数都相同的微粒是_______ (写出一种即可);
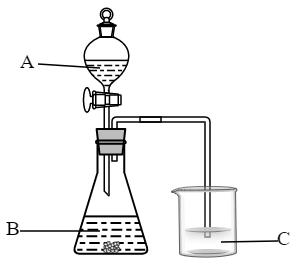
(3)A、B和E最高价氧化物对应的水化物中,酸性最强的是_______ ,若用如图装置验证这三种酸的酸性强弱,则烧杯C中可观察到有白色沉淀(H2SiO3)生成。该实验装置存在不足,影响到实验目的的达成,改进方法是_______ ;
(4)用电子式表示D2C的形成过程:_______ 。
提示:硝酸是一种易挥发的强酸。
(1)元素E在元素周期表中的位置是
(2)与元素D的简单离子所含电子数和质子数都相同的微粒是
(3)A、B和E最高价氧化物对应的水化物中,酸性最强的是

(4)用电子式表示D2C的形成过程:
您最近一年使用:0次
名校
9 . 下列编号代表元素周期表中的一部分元素,用化学用语回答下列问题:

(1)碳元素在周期表中的位置为_______ ,其最高价氧化物的电子式为_______ 。
(2)①⑨形成的化合物的化学键类型为_______ ,③⑧形成的化合物的电子式为_______ ,④形成的单质的结构式为_______ 。
(3)②⑥的最高价氧化物的水化物发生反应的离子方程式为_______ 。
(4)②③最高价氧化物对应的水化物碱性较强的是_______ 。(写化学式)
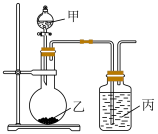
(5)现拟用如下装置,证明元素的非金属性强弱: ,请选用合适的试剂完成实验。
,请选用合适的试剂完成实验。

(1)碳元素在周期表中的位置为
(2)①⑨形成的化合物的化学键类型为
(3)②⑥的最高价氧化物的水化物发生反应的离子方程式为
(4)②③最高价氧化物对应的水化物碱性较强的是
(5)现拟用如下装置,证明元素的非金属性强弱:
 ,请选用合适的试剂完成实验。
,请选用合适的试剂完成实验。
| 实验试剂 | 甲: ;丙 ;丙 |
| 可得出结论的实验现象 |
您最近一年使用:0次
名校
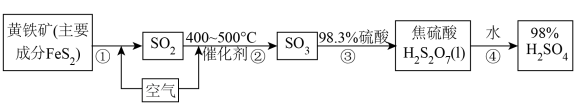
10 . 工业上用黄铁矿为原料制备硫酸的流程如图所示:
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为___________ 。
(2)已知: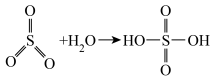 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式___________ 。
(3)写出步骤①的化学方程式___________ 。
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因___________ 。
(5)下列说法正确的是___________ 。
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象___________ 。(供选择的试剂:KSCN溶液、稀硫酸、稀盐酸、KMnO4溶液、品红溶液、NaOH溶液)
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为
(2)已知:
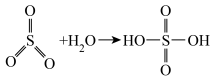 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式(3)写出步骤①的化学方程式
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因
(5)下列说法正确的是
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象
您最近一年使用:0次



