解题方法
1 . 如图是氮元素的几种价态与物质类别的对应关系。回答下列问题:
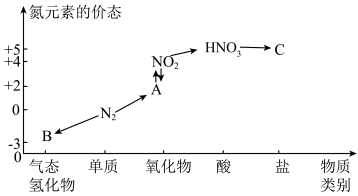
(1)写出 的一种用途:
的一种用途:___________ 。
(2)B物质的电子式为:___________ 。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为___________ 。
(4)实验室制取物质B的化学方程式为___________ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___________ 。
(6)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入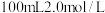 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________  。
。

(1)写出
 的一种用途:
的一种用途:(2)B物质的电子式为:
(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为(4)实验室制取物质B的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
(6)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生
 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入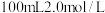 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
名校
2 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系: 的电子式为
的电子式为________ ;将 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为________ 。
(2)S粉与热的Z浓溶液反应可转化为________ ,反应的化学方程式为________ 。
(3)配平下列反应:_____
____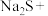 ____
____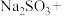 ____
____ ____
____ ____
____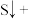 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。________ 。
②C的作用是________ ,装置D中试管口放置的棉花应浸有一种液体,这种液体是________ 。
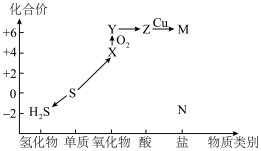
 的电子式为
的电子式为 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为(2)S粉与热的Z浓溶液反应可转化为
(3)配平下列反应:
____
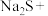 ____
____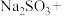 ____
____ ____
____ ____
____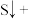 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
| A.X能使溴水褪色,证明X有漂白性 | B.将X通入 溶液中有白色沉淀生成 溶液中有白色沉淀生成 |
C.硫在过量的 中燃烧可以生成Y 中燃烧可以生成Y | D.若N为钠盐,则N与Z的稀溶液反应可生成 |
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。

②C的作用是
您最近一年使用:0次
3 . 酸碱中和反应是以水溶液为载体的反应体系中最基础、最常见的反应,其反应实质为:H++OH_H2O。在DIS数字化实验系统的应用下,我们能在电脑上采集实验数据,并绘制成直观的图像,便于我们更好地分析实验、研究课题。
I.试剂配制:配制480mL0.100mol·L-1的NaOH溶液。
(1)NaOH的电子式为___________ 。
(2)除烧杯、胶头滴管、玻璃棒以外,还需用到的玻璃仪器有________ ,在使用前,必须检查该仪器是否________ 。若用NaOH固体配置,则需用电子天平称取NaOH的质量为_________ g。
(3)下图所示是配制溶液过程中的四个步骤,回答下列问题:
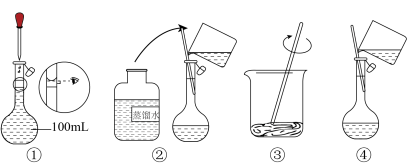
①图示四个步骤正确的先后顺序应是___________ ;
A.①②③④ B.③④②① C.③②④① D.③④①②
②步骤①为定容,在此过程中若俯视刻度线,则可能导致得到的溶液浓度___________ ;若使用的容量瓶未洗净,残留有上一次配制的相同溶液,则会导致浓度___________ 。
A.偏高 B.偏低 C.无影响
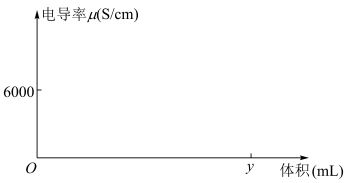
II.实验小组将电导率传感器插入40mLxmol∙L-1H2SO4溶液中,向溶液中匀速滴入I中配得的NaOH稀溶液,得到的电导率与溶液体积图像如图所示。(已知:溶液导电性越强,电导率值越大)

(4)B点曲线突然变化的原因是___________ 。
(5)根据图像,计算得到x的值为___________ 。(保留两位有效数字)
(6)小沐同学认为该图像与理论有出入:曲线AB的下降趋势应当逐渐变缓
①你是否认同这种说法?说明理由。___________
②针对实验数据与理论不符的情况,下列做法中可行的是___________ 。(不定项)
A.篡改数据,使其与理论相符
B.将实验重复多次,再进行对比分析
C.更换一套实验装置,再进行多次实验
(7)现将实验所用的酸和碱替换,使用其他种类的酸和碱再探究酸碱中和导电率与体积的对应关系。
①向0.1mol∙L-1氨水中,匀速滴入等浓度的醋酸溶液,下列图像可能正确的是___________ 。

②向ymL0.1mol∙L-1Ba(OH)2溶液中,匀速滴入等浓度的H2SO4溶液,预测曲线的变化趋势,绘制在下图中___________ 。(只需表示出变化趋势与关键点即可)
I.试剂配制:配制480mL0.100mol·L-1的NaOH溶液。
(1)NaOH的电子式为
(2)除烧杯、胶头滴管、玻璃棒以外,还需用到的玻璃仪器有
(3)下图所示是配制溶液过程中的四个步骤,回答下列问题:

①图示四个步骤正确的先后顺序应是
A.①②③④ B.③④②① C.③②④① D.③④①②
②步骤①为定容,在此过程中若俯视刻度线,则可能导致得到的溶液浓度
A.偏高 B.偏低 C.无影响
II.实验小组将电导率传感器插入40mLxmol∙L-1H2SO4溶液中,向溶液中匀速滴入I中配得的NaOH稀溶液,得到的电导率与溶液体积图像如图所示。(已知:溶液导电性越强,电导率值越大)

(4)B点曲线突然变化的原因是
(5)根据图像,计算得到x的值为
(6)小沐同学认为该图像与理论有出入:曲线AB的下降趋势应当逐渐变缓
①你是否认同这种说法?说明理由。
②针对实验数据与理论不符的情况,下列做法中可行的是
A.篡改数据,使其与理论相符
B.将实验重复多次,再进行对比分析
C.更换一套实验装置,再进行多次实验
(7)现将实验所用的酸和碱替换,使用其他种类的酸和碱再探究酸碱中和导电率与体积的对应关系。
①向0.1mol∙L-1氨水中,匀速滴入等浓度的醋酸溶液,下列图像可能正确的是

②向ymL0.1mol∙L-1Ba(OH)2溶液中,匀速滴入等浓度的H2SO4溶液,预测曲线的变化趋势,绘制在下图中

您最近一年使用:0次
名校
4 . 如图是氮元素的几种价态与物质类别的对应关系。回答下列问题:
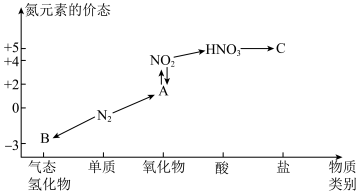
(1)B物质的电子式为:_______ 。
(2)实验室制取物质B的化学方程式为_______ 。
(3)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。
(4)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入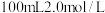 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为_______  。
。

(1)B物质的电子式为:
(2)实验室制取物质B的化学方程式为
(3)浓硝酸与木炭在加热条件下反应的化学方程式为
(4)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生
 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入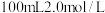 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
名校
解题方法
5 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)硫元素在周期表中的位置为_____ ;H2S的电子式为_____ 。
(2)根据A对应的化合价和物质类别,A为_____ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有_____ 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_____ ,反应的离子方程式为_____ 。
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:_____ 。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的化学方程式:_____ 。

(1)硫元素在周期表中的位置为
(2)根据A对应的化合价和物质类别,A为
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的化学方程式:
您最近一年使用:0次
2021高一·全国·专题练习
6 . Ⅰ.使用正确的化学用语填空。
(1)写出下列物质的电子式:
氮气___________ ;过氧化钠___________ ;四氯化碳___________ 。
(2)写出下列物质的结构式:
二氧化碳___________ ;过氧化氢___________ ;次氯酸___________ 。
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:___________ 。
②原子半径由大到小的顺序:___________ 。
③离子半径由大到小的顺序:___________ 。
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F___________ Cl- ②Fe2+___________ Fe3+ ③O2-___________ Mg2+。
(1)写出下列物质的电子式:
氮气
(2)写出下列物质的结构式:
二氧化碳
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:
②原子半径由大到小的顺序:
③离子半径由大到小的顺序:
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F
您最近一年使用:0次
解题方法
7 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。如图是氮元素的几种价态与物质类别的对应关系。回答下列问题:
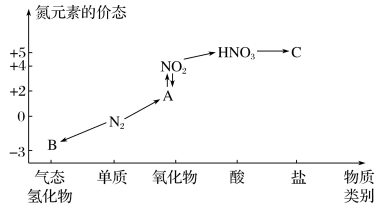
(1)写出氮气生成A的化学方程式:_______ 。
(2)物质B的电子式为_______ 。在催化剂和加热的条件下,由物质B生成物质A是工业制硝酸的重要反应,其化学方程式为_______ 。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。
(4)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。
(5)实验室中,检验溶液中含有 的操作方法是
的操作方法是_______ 。

(1)写出氮气生成A的化学方程式:
(2)物质B的电子式为
(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为(4)浓硝酸与木炭在加热条件下反应的化学方程式为
(5)实验室中,检验溶液中含有
 的操作方法是
的操作方法是
您最近一年使用:0次
名校
8 . 易混易错题组
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气_______ 过氧化钠 _________ 四氯化碳________
(2)写出下列物质的结构式
二氧化碳________ 过氧化氢 _________ 次氯酸________
(学法题)正确书写化合物的电子式需要注意的问题是_____________
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:___________
②原子半径由大到小的顺序为:___________
③离子半径由大到小的顺序为:___________
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-________ Cl- ②Fe2+________ Fe3+ ③O2-_________ Mg2+
(学法题)粒子半径大小比较方法(两点即可)___________
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气
(2)写出下列物质的结构式
二氧化碳
(学法题)正确书写化合物的电子式需要注意的问题是
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:
②原子半径由大到小的顺序为:
③离子半径由大到小的顺序为:
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-
(学法题)粒子半径大小比较方法(两点即可)
您最近一年使用:0次
解题方法
9 . A、B、C、D、E、F为短周期元素, 原子序数依次增大。非金属元素A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。E+与D2-具有相同的电子层结构。A单质在F单质中燃烧,产物溶于水得到一种强酸M。回答下列问题:
(1)画出E的离子结构示意图___________ 。
(2)F在周期表中的位置是___________ 。
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为___________ 。
(4)由这些元素组成的物质,相关信息如下:
①a的电子式为___________ 。 写出其与水反应的化学方程式:___________ 。
②b的一种常见用途为___________ 。
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为___________ 。
(1)画出E的离子结构示意图
(2)F在周期表中的位置是
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为
(4)由这些元素组成的物质,相关信息如下:
| 物质 | 组成和结构信息 |
| a | 由 A、E组成的离子化合物 |
| b | 由D、E组成的含非极性键的离子化合物,阴阳离子数之比为1:2 |
| c | 化学式为BDF2的共价化合物 |
②b的一种常见用途为
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为
您最近一年使用:0次
名校
解题方法
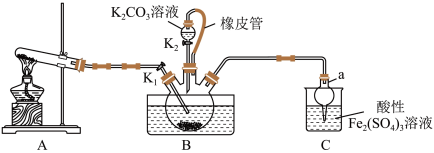
10 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: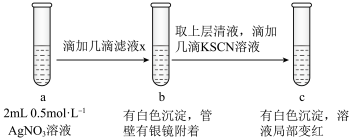
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次



