1 . 工业上利用氧化铝基废催化剂(主要成分为Al2O3,少量Pd)回收Al2(SO4)3及Pd 流程如图:

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为________ 。
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是_________ (填字母)
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式______ (已知氯钯酸为弱酸)
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式________ 。
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。_______
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量__________ [列式表示,其中(NH4)2PdCl6相对分子质量为355]。
④实验结束时,发现硬质试管右端有少量白色固体,可能是____ (填化学式),这种情况导致实验结果_________ (填“偏高”、“偏低”、“无影响”)

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量
④实验结束时,发现硬质试管右端有少量白色固体,可能是
您最近一年使用:0次
2020-01-01更新
|
503次组卷
|
2卷引用:2019年湖南省郴州市高三第一次教学质量监测化学试题
名校
2 . KMnO4是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿(主要成分MnO2,还有Fe2O3、Al2O3、SiO2等)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得KMnO4(反应条件已经省略)。
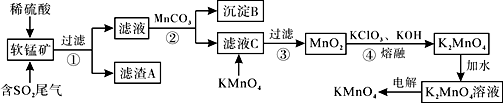
已知:Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。回答下列问题:
(1)K2MnO4中Mn的化合价为___________ 。
(2)滤渣A的成分是_________ ,析出沉淀B时,首先析出的物质是_________ 。
(3)步骤2中加入MnCO3的作用为_______________ 。
(4)滤液C中加入KMnO4时发生反应的离子方程式是_________________ 。
(5)步骤4中反应的化学方程式是_______________ 。
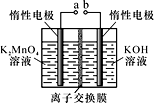
(6)电解制备KMnO4的装置如图所示。b与电源的______ 极相连,电解液中最好选择_______ 离子交换膜(填“阳”或“阴”)。电解时,阳极的电极反应式为_________ 。

已知:Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。回答下列问题:
(1)K2MnO4中Mn的化合价为
(2)滤渣A的成分是
(3)步骤2中加入MnCO3的作用为
(4)滤液C中加入KMnO4时发生反应的离子方程式是
(5)步骤4中反应的化学方程式是
(6)电解制备KMnO4的装置如图所示。b与电源的

您最近一年使用:0次
2019-01-25更新
|
1214次组卷
|
2卷引用:四川省绵阳市2019届高三上学期第二次(1月)诊断性考试理科综合化学试题
名校
3 . 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
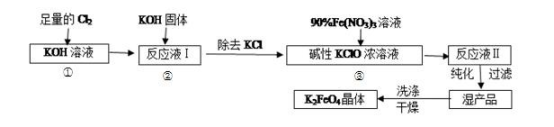

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③K2FeO4在水溶液中易水解:4FeO42+10H2O 4Fe(OH)3(胶体)+8OH-+3O2↑
4Fe(OH)3(胶体)+8OH-+3O2↑
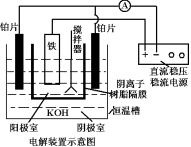
回答下列问题:实验室可利用如图装置完成流程①和②
(1)写出工业上制取 Cl2 的化学方程式_____ ;恒压滴液漏斗支管的作用_____ ,两水槽中的水为__________ (填“热水”或“冷水”).
(2)反应一段时间后,停止通氯气,再往仪器 a 中加入浓 KOH 溶液的目的是_____ ;
A.为下一步反应提供碱性的环境
B.使 KClO3 转化为 KClO
C.与溶液 I 中过量的Cl2继续反应,生成更多的KClO
D.KOH 固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出 K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子方程式为:_________________ 。
(4)用重结晶法提纯粗产品:将粗产品先用 KOH 稀溶液溶解,再加入饱和的 KOH溶液,冷却结晶,过滤,用少量异丙醇洗涤,最后低温真空干燥。
①洗涤粗品时选用异丙醇而不用水的理由是_____________ 。
②如何判断 K2FeO4 晶体已经洗涤干净________________ 。
(5)从环境保护的角度看,制备 K2FeO4 较好的方法为电解法,其装置如图电解过程中阳极的电极反应式为___________ 。
(6)FeO42-在水溶液中的存在形态如图所示。下列说法正确的是______________ 。
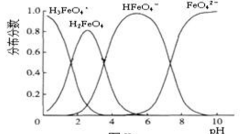
A.不论溶液的酸碱性如何变化,铁元素都有 4 种存在形态
B.向 pH=10的这种溶液中加硫酸至 pH=2,HFeO4-的分布分数逐渐 增大
C.向 pH=6 的这种溶液中加 KOH 溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42- +H2O



已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③K2FeO4在水溶液中易水解:4FeO42+10H2O
 4Fe(OH)3(胶体)+8OH-+3O2↑
4Fe(OH)3(胶体)+8OH-+3O2↑回答下列问题:实验室可利用如图装置完成流程①和②
(1)写出工业上制取 Cl2 的化学方程式
(2)反应一段时间后,停止通氯气,再往仪器 a 中加入浓 KOH 溶液的目的是
A.为下一步反应提供碱性的环境
B.使 KClO3 转化为 KClO
C.与溶液 I 中过量的Cl2继续反应,生成更多的KClO
D.KOH 固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出 K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子方程式为:
(4)用重结晶法提纯粗产品:将粗产品先用 KOH 稀溶液溶解,再加入饱和的 KOH溶液,冷却结晶,过滤,用少量异丙醇洗涤,最后低温真空干燥。
①洗涤粗品时选用异丙醇而不用水的理由是
②如何判断 K2FeO4 晶体已经洗涤干净
(5)从环境保护的角度看,制备 K2FeO4 较好的方法为电解法,其装置如图电解过程中阳极的电极反应式为
(6)FeO42-在水溶液中的存在形态如图所示。下列说法正确的是

A.不论溶液的酸碱性如何变化,铁元素都有 4 种存在形态
B.向 pH=10的这种溶液中加硫酸至 pH=2,HFeO4-的分布分数逐渐 增大
C.向 pH=6 的这种溶液中加 KOH 溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42- +H2O
您最近一年使用:0次
2019-01-22更新
|
856次组卷
|
2卷引用:【全国百强校】天津市第一中学2019届高三上学期第三次月考化学试题
4 . Ⅰ.化合物 Mg5Al3(OH)19(H2O)4 可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据___________ 。
(2)用离子方程式表示除去固体产物中 Al2O3 的原理___________
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理_____________ 。
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:
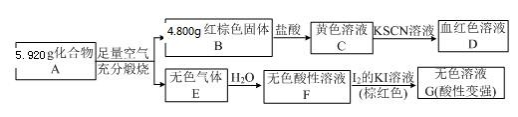
请回答:
(4)A的化学式为_____ 。C 中呈黄色的离子对应元素在元素周期表中的位置为__________ 。
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为_____ 。写出该反应的离子方程式_________ 。
(6)写出F→G反应的化学方程式____________ 。
 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3(1)写出该化合物作阻燃剂的两条依据
(2)用离子方程式表示除去固体产物中 Al2O3 的原理
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:

请回答:
(4)A的化学式为
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为
(6)写出F→G反应的化学方程式
您最近一年使用:0次
2019-01-22更新
|
413次组卷
|
2卷引用:【全国百强校】天津市第一中学2019届高三上学期第三次月考化学试题
18-19高三·江苏南通·阶段练习
名校
5 . 下列有关化学用语表示正确的是
A.质量数为37的氯原子: |
B.对硝基甲苯的结构简式: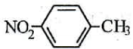 |
C.NH3的电子式: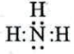 |
| D.碳酸氢钠的电离方程式NaHC03=Na++H++C032- |
您最近一年使用:0次
18-19高三·江苏南通·阶段练习
名校
6 . 用化学用语表示Cl2+H2O HClO+HCl中的相关微粒,其中正确的是
HClO+HCl中的相关微粒,其中正确的是
 HClO+HCl中的相关微粒,其中正确的是
HClO+HCl中的相关微粒,其中正确的是A.Cl-的结构示意图: | B.HClO的电子式: |
C.H2O的结构式: | D.中子数为20的氯原子: 2017Cl |
您最近一年使用:0次
7 . 示踪原子法是研究化学反应的重要方法之一,下列化学方程式正确的是
| A.2Na2O2+2H218O= 4NaOH+18O2 ↑ |
| B.2KMnO4+5H218O2 +3H2SO4= K2SO4+2MnSO4+ 518O2↑+8H2O |
C.CH3C18OOH + CH3OH CH3CO18OCH3+H2O CH3CO18OCH3+H2O |
| D.6H37Cl+ NaClO3==NaCl+37Cl2+3H2O |
您最近一年使用:0次
名校
8 . 按要求填空:
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式________ ,其单质与NaOH反应的化学方程式为____________________________________________________ 。
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是___________________ ,原子半径由大到小的顺序是__________________ 。
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ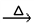 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:_____________ ,______________ ;比较C和D的稳定性的强弱:_____________________ (用化学式表示)。
(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是_______ (填序号),既有离子键又有非极性键的是______ (填序号);既有离子键又有极性键的是______ (填序号)。
(5)下列原子: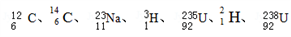 中共有
中共有____ 种元素,__ 种核素。
(6)写出下列物质或微粒的电子式:
①CO2__________ ②KCl_____________ ③H2O2_______________ ④N2_____________ ;
⑤用电子式表示MgCl2的形成过程_________________________________________________ 。
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
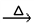 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是
(5)下列原子:
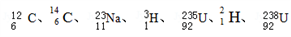 中共有
中共有(6)写出下列物质或微粒的电子式:
①CO2
⑤用电子式表示MgCl2的形成过程
您最近一年使用:0次
名校
9 . 过氧化铬(CrO5)的结构为: ,由此可推知CrO5中氧元素的化合价应该是
,由此可推知CrO5中氧元素的化合价应该是
 ,由此可推知CrO5中氧元素的化合价应该是
,由此可推知CrO5中氧元素的化合价应该是| A.全部-1价 | B.4/5为-1价,1/5为-2价 |
| C.全部-2价 | D.4/5为-2价,1/5为-1价 |
您最近一年使用:0次
2017-05-04更新
|
1542次组卷
|
2卷引用:四川省南充市高级中学2016-2017学年高一4月检测考试化学试题
10 . 原子序数由小到大排列的四种短周期元素X、Y、 Z、W, 四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)M元素是__________ (填元素符号)。
(2)Z、W形成的气态氢物的稳定性为_______ >________ 。(填化学式)
(3)写出M完全燃烧生成的氧化物的电子式________ ,该氧化物与水反应的离子方程式________ 。
(4)由X、Y、Z、W四种元素中的三种组成的—种强酸,该强酸的稀溶液能与铜反应,离子方程式为_______ 。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1molA能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是_______ (填化学式)。写出该气体B与氯水反应的离子方程式____________________ 。
(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C,1mol C中含有6mol结晶水。对化合物C进行下实验:a.取C的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;b.另取C的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。C的化学式为______________________________ 。
(1)M元素是
(2)Z、W形成的气态氢物的稳定性为
(3)写出M完全燃烧生成的氧化物的电子式
(4)由X、Y、Z、W四种元素中的三种组成的—种强酸,该强酸的稀溶液能与铜反应,离子方程式为
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1molA能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是
(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C,1mol C中含有6mol结晶水。对化合物C进行下实验:a.取C的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;b.另取C的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。C的化学式为
您最近一年使用:0次



