1 . 废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:
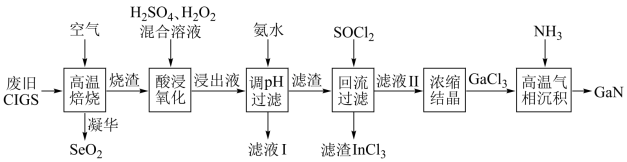
回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为_______ ;在化合物 中镓(Ga)和铟(In)均为+3价,则Cu的化合价为
中镓(Ga)和铟(In)均为+3价,则Cu的化合价为_______ 。
(2)“酸浸氧化”得蓝色溶液,则该过程发生的主要氧化还原反应的化学方程式为_______ 。
(3)氢氧化铜沉淀可溶于氨水,则滤液I中的阴离子主要有_______ 和_______ 两种。
(4)滤渣加入 混合前需要洗涤、干燥,并用试剂
混合前需要洗涤、干燥,并用试剂_______ 和_______ 来检验滤渣中的 是否洗净。
是否洗净。
(5)滤渣加入 可反生反应:
可反生反应: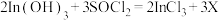 ;对物质X的性质有如下判断,你认为不正确的是 。
;对物质X的性质有如下判断,你认为不正确的是 。
(6)“高温气相沉积”过程中发生的化学反应方程式为_______ 。
 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:
回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为
 中镓(Ga)和铟(In)均为+3价,则Cu的化合价为
中镓(Ga)和铟(In)均为+3价,则Cu的化合价为(2)“酸浸氧化”得蓝色溶液,则该过程发生的主要氧化还原反应的化学方程式为
(3)氢氧化铜沉淀可溶于氨水,则滤液I中的阴离子主要有
(4)滤渣加入
 混合前需要洗涤、干燥,并用试剂
混合前需要洗涤、干燥,并用试剂 是否洗净。
是否洗净。(5)滤渣加入
 可反生反应:
可反生反应: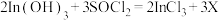 ;对物质X的性质有如下判断,你认为不正确的是 。
;对物质X的性质有如下判断,你认为不正确的是 。| A.有弱酸性 | B.可使溴水褪色 |
C.与 溶液反应得白色沉淀 溶液反应得白色沉淀 | D.与烧碱溶液反应可生成两种盐 |
您最近一年使用:0次
2022-05-13更新
|
240次组卷
|
3卷引用:广东省实验中学2023-2024学年高三上学期第一次阶段考试化学试题
广东省实验中学2023-2024学年高三上学期第一次阶段考试化学试题湖北省鄂州市部分高中教科研协作体2021-2022学年高一下学期期中考试化学试题(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)
名校
解题方法
2 . 下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
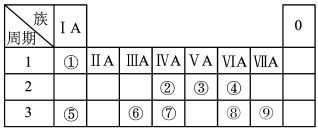
(1)画出元素⑦的原子结构示意图_____________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______________ (填化学式)。
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:_______________ 。
(4)写出元素⑤形成的过氧化物的电子式__________________ ;
(5)由表中元素形成的常见物质 X、Y、Z、M、N 可发生以下反应:
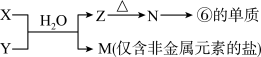
X 溶液与 Y 溶液反应的离子方程式为_____ 。

(1)画出元素⑦的原子结构示意图
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:
(4)写出元素⑤形成的过氧化物的电子式
(5)由表中元素形成的常见物质 X、Y、Z、M、N 可发生以下反应:

X 溶液与 Y 溶液反应的离子方程式为
您最近一年使用:0次
解题方法
3 . 二硫化钼(MoS2)被誉为“固体润滑剂之王”,利用低品质的辉钼矿(含MoS2、SiO2以及CuFeS2等杂质)制备高纯二硫化钼的一种生产工艺如图:
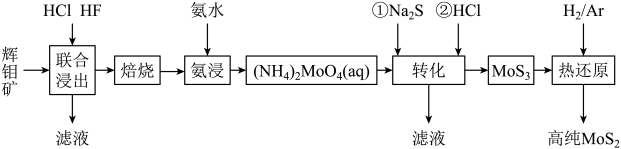
回答下列问题:
(1)(NH4)2MoO4中Mo的化合价为_____ 。
(2)“联合浸出”中HF除去的杂质化学式为_____ ,“焙烧”时MoS2转化为MoO3的化学方程式为_____ 。
(3)“转化”中加入Na2S后,(NH4)2MoO4转化为(NH4)2MoS4,写出(NH4)2MoS4与盐酸生成MoS3的离子方程式_____ 。
(4)由图分析产生MoS3沉淀的流程中应选择的最优温度和时间是_____ ,利用化学平衡原理分析低于或高于最优温度时,MoS3的产率均下降的原因_____ 。
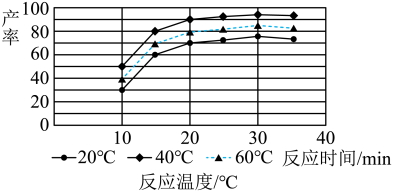
(5)高纯MoS2中存在极微量非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+的物质的量之比为_____ 。
(6)已知Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8,不纯的Na2MoO4溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(溶液体积变化忽略),则当SO42-完全沉淀时,溶液中c(MoO42-)<_____ mol/L(保留2位有效数字)

回答下列问题:
(1)(NH4)2MoO4中Mo的化合价为
(2)“联合浸出”中HF除去的杂质化学式为
(3)“转化”中加入Na2S后,(NH4)2MoO4转化为(NH4)2MoS4,写出(NH4)2MoS4与盐酸生成MoS3的离子方程式
(4)由图分析产生MoS3沉淀的流程中应选择的最优温度和时间是

(5)高纯MoS2中存在极微量非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+的物质的量之比为
(6)已知Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8,不纯的Na2MoO4溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(溶液体积变化忽略),则当SO42-完全沉淀时,溶液中c(MoO42-)<
您最近一年使用:0次
名校
4 . 铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工业流程如下:
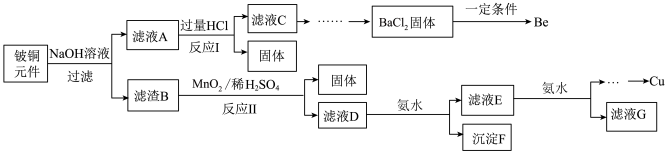
已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
(1)用NaOH溶液溶解铍铜元件步骤中提高溶解率的措施是_______ 。(至少写出两种)滤液A的主要成分除NaOH外,还有_____ (填化学式)。
(2)写出反应I中含铍化合物与过量盐酸反应的离子方程式_______ ,写出反应I中生成固体的化学方程式:________ 。
(3)滤液C中含NaCl、BeCl2和少量HCl。为提纯BeCl2,最合理的实验步骤顺序为____ (填字母)。
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH
d.加入适量的HCl e.洗涤 f.过滤
(4)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:______ 。
(5)该小组从1kg该种旧铍铜元件中回收得到433g Cu,则该流程Cu的产率为_______ (保留三位有效数字)。

已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
| 难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)用NaOH溶液溶解铍铜元件步骤中提高溶解率的措施是
(2)写出反应I中含铍化合物与过量盐酸反应的离子方程式
(3)滤液C中含NaCl、BeCl2和少量HCl。为提纯BeCl2,最合理的实验步骤顺序为
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH
d.加入适量的HCl e.洗涤 f.过滤
(4)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:
(5)该小组从1kg该种旧铍铜元件中回收得到433g Cu,则该流程Cu的产率为
您最近一年使用:0次



