名校
1 . 已知烷烃A的密度是相同条件下H2密度的15倍。
(1)烷烃A的电子式为___________ 。
(2)烷烃A与丙烷C3H8互为___________ 。
a.同系物 b.同位素
c.同分异构体 d.同素异形体
(3)A与Cl2发生反应生成一氯代物的化学方程式为___________ 。
(4)A燃烧的化学方程式为___________ 。
(1)烷烃A的电子式为
(2)烷烃A与丙烷C3H8互为
a.同系物 b.同位素
c.同分异构体 d.同素异形体
(3)A与Cl2发生反应生成一氯代物的化学方程式为
(4)A燃烧的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . Ⅰ.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氯化镁;⑦ ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)④的电子式为___________ 。
(3)用电子式表示⑥的形成过程___________ 。
(4)除去③中少量②的操作是___________ ,化学方程式为___________ 。
(5)⑦中含有的化学键为___________ 。
(6)⑨在水溶液中的电离方程式为___________ 。
Ⅱ.写出下列反应的离子方程式(已知还原性: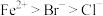 ):
):
(7)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)___________ ;
(8)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶___________ 。
 ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的操作是
(5)⑦中含有的化学键为
(6)⑨在水溶液中的电离方程式为
Ⅱ.写出下列反应的离子方程式(已知还原性:
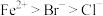 ):
):(7)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)(8)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶
您最近一年使用:0次
解题方法
3 . 下列化学用语或图示表达不正确的是
| A.HClO的结构式为:H-O-Cl | B.CO2的电子式: |
C.溴乙烷的分子模型: | D.Na+的结构示意图: |
您最近一年使用:0次
名校
4 . 下列化学用语表示正确的是
| A.乙烯的结构简式:CH2CH2 | B.H2O的电子式: |
C.氧原子的结构示意图: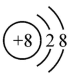 | D.K2SO4的电离方程式:K2SO4=2K++SO |
您最近一年使用:0次
2021-11-12更新
|
140次组卷
|
4卷引用:天津市红桥区2020-2021学年高一下学期期末考试化学试题
天津市红桥区2020-2021学年高一下学期期末考试化学试题江苏省盐城市上冈高级中学2021-2022学年高二上学期期中考试化学(必修)试题江苏省扬州市宝应县2021-2022学年高二上学期期中检测化学(必修)试题(已下线)专题04 认识有机化合物 乙烯与有机高分子材料-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
解题方法
5 . A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一、请用化学用语回答下列问题:
(1)F在元素周期表中的位置为___________ 。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,该反应的化学方程式为___________ 。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为___________ 。写出在空气中长期放置生成H的化学反应方程式为:___________ 。H的溶液与稀硫酸反应产生的现象为___________ 。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为___________ 。
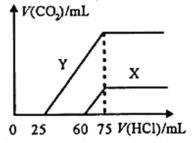
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.4mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为___________ ;原NaOH溶液的物质的量浓度为___________ ;由曲线X、Y可知,两次实验通入的CO2的体积比为___________ 。
(1)F在元素周期表中的位置为
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,该反应的化学方程式为
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.4mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为

您最近一年使用:0次
名校
6 . 下列化学用语表述正确的是
| A.S2Cl2结构式为Cl—S—S—Cl | B.S2-结构示意图为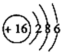 |
C.PCl3电子式为: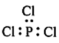 | D.CO2分子的比例模型: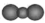 |
您最近一年使用:0次
2021-11-12更新
|
265次组卷
|
3卷引用:天津市五校联考2021-2022学年高三上学期期中考试化学试题
解题方法
7 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:

(1)④、⑤、⑧的简单离子半径由大到小的顺序是___________ 。
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是___________ 。
(3)①与③能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的电子式为___________ 。
(4)工业制⑥的单质时,电解其氧化物而不电解其氯化物的原因是___________ 。
(5)②在空气中燃烧形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
(6)元素X与⑦同一主族,X原子比⑦原子多一个电子层,X的原子结构示意图为___________ ,其氢化物的化学式为___________ 。

(1)④、⑤、⑧的简单离子半径由大到小的顺序是
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①与③能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的电子式为
(4)工业制⑥的单质时,电解其氧化物而不电解其氯化物的原因是
(5)②在空气中燃烧形成化合物的化学式是
(6)元素X与⑦同一主族,X原子比⑦原子多一个电子层,X的原子结构示意图为
您最近一年使用:0次
8 . Ⅰ. 化学家侯德榜创立了中国的制碱工艺,促进了世界制碱技术的发展。下图是纯碱工艺的简化流程:
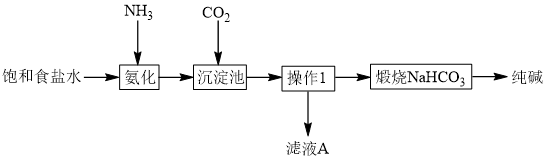
(1)写出 的电子式
的电子式_______ ,操作1的名称是_______ 。
(2)用离子方程式表示纯碱工艺中 的生成
的生成_______ 。
(3)滤液 中最主要的两种离子是
中最主要的两种离子是_______ 、_______ 。
(4)某纯碱样品因煅烧不充分而含少量 ,取质量为
,取质量为 的纯碱样品,充分加热后质量为
的纯碱样品,充分加热后质量为 ,则此样品中碳酸氢钠的质量分数为
,则此样品中碳酸氢钠的质量分数为_______ 。
Ⅱ. 医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量。
(5)配平以下离子方程式并填上合适的微粒:_______ 。
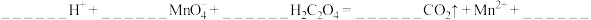
(6)测定血钙的含量取 血液用蒸馏水稀释后,向其中加入足量
血液用蒸馏水稀释后,向其中加入足量 溶液,反应生成
溶液,反应生成 沉淀,过滤并洗涤沉淀,将沉淀用豨硫酸溶解得到
沉淀,过滤并洗涤沉淀,将沉淀用豨硫酸溶解得到 后,再与定量的
后,再与定量的 溶液恰好完全反应。溶解沉淀时
溶液恰好完全反应。溶解沉淀时_______ (填“能”或“不能”)使用稀盐酸。
(7)上述实验中若消耗了 的
的 溶液
溶液 ,则
,则 该血液中含钙
该血液中含钙_______  。
。

(1)写出
 的电子式
的电子式(2)用离子方程式表示纯碱工艺中
 的生成
的生成(3)滤液
 中最主要的两种离子是
中最主要的两种离子是(4)某纯碱样品因煅烧不充分而含少量
 ,取质量为
,取质量为 的纯碱样品,充分加热后质量为
的纯碱样品,充分加热后质量为 ,则此样品中碳酸氢钠的质量分数为
,则此样品中碳酸氢钠的质量分数为Ⅱ. 医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量。
(5)配平以下离子方程式并填上合适的微粒:
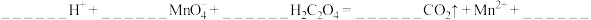
(6)测定血钙的含量取
 血液用蒸馏水稀释后,向其中加入足量
血液用蒸馏水稀释后,向其中加入足量 溶液,反应生成
溶液,反应生成 沉淀,过滤并洗涤沉淀,将沉淀用豨硫酸溶解得到
沉淀,过滤并洗涤沉淀,将沉淀用豨硫酸溶解得到 后,再与定量的
后,再与定量的 溶液恰好完全反应。溶解沉淀时
溶液恰好完全反应。溶解沉淀时(7)上述实验中若消耗了
 的
的 溶液
溶液 ,则
,则 该血液中含钙
该血液中含钙 。
。
您最近一年使用:0次
真题
9 . CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应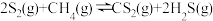 ,回答下列问题:
,回答下列问题:
(1)CH4的电子式为___________ ,CS2分子的立体构型为___________ 。
(2)某温度下,若S8完全分解成气态S2。在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为___________ 。
②当以下数值不变时,能说明该反应达到平衡的是___________ (填序号)。
a.气体密度b.气体总压c.CH4与S2体积比d.CS2的体积分数
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为___________ (填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条件下进行此反应,不采用低于600℃的原因是___________ 。___________ 。
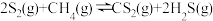 ,回答下列问题:
,回答下列问题:(1)CH4的电子式为
(2)某温度下,若S8完全分解成气态S2。在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为
②当以下数值不变时,能说明该反应达到平衡的是
a.气体密度b.气体总压c.CH4与S2体积比d.CS2的体积分数
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为

您最近一年使用:0次
2021-09-07更新
|
5936次组卷
|
4卷引用:2021年新高考天津化学高考真题
2021年新高考天津化学高考真题2021年天津高考化学试题变式题13-16(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习陕西省洛南中学2023-2024学年高三下学期第十次模拟考试理综试题-高中化学
名校
解题方法
10 . 化学用语的书写和使用应符合规范要求。下列化学用语不正确的是
A.Cl-的结构示意图: | B.羟基的电子式: |
| C.重水的分子式:H218O | D.HClO的结构式:H—O—Cl |
您最近一年使用:0次



