名校
解题方法
1 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4L 中含有分子数为 中含有分子数为 |
B.18g 分子中含有的中子数目为 分子中含有的中子数目为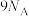 |
C.标准状况下,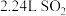 与 与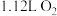 充分反应,生成的 充分反应,生成的 分子数目为0.1NA 分子数目为0.1NA |
D.150mL18 mol·L 硫酸与足量Cu共热,生成的 硫酸与足量Cu共热,生成的 的数目为 的数目为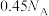 |
您最近一年使用:0次
2 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol/L的NaHCO3溶液中, 数目小于 数目小于 |
B.11.2LCO2含π键数目为 |
C.1molNH4Cl含有的共价键数目为 |
D.18g重水(D2O)中所含质子数为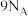 |
您最近一年使用:0次
名校
3 . I.神舟十七号载人航天飞船于2023年10月26日成功发射,飞船搭载的是中国研制的长征二号F遥十七运载火箭,采用四氧化二氮(N2O4)和偏二甲肼(C2H8N2)作为推进剂,二者反应生成二氧化碳、水蒸气和氮气。
(1)偏二甲肼的摩尔质量为___________ 。
(2)四氧化二氮能与水反应生成亚硝酸和___________ (写化学式)。
(3)四氧化二氮和偏二甲肼反应的化学方程式为:2N2O4+C2H8N2 2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是
2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是___________ 。
(4)已知N2、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO2的质量为___________ 。
II.二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
(5)将二氧化氯通入紫色石蕊试液中,溶液褪色的理由是___________ 。
(6)设NA为阿伏加德罗常数的值,现有10g质量分数为64%的甲醇(CH3OH)水溶液,则该溶液所含氢原子数目为___________ 。
(7)假设CO2和ClO2在标准状况下均为气体,则反应CH3OH+NaClO3+H2SO4 → CO2↑+ClO2↑+Na2SO4 +H2O(未配平)中转移的电子数目为0.6NA时,该反应产生标准状况下气体的体积为___________ 。
(1)偏二甲肼的摩尔质量为
(2)四氧化二氮能与水反应生成亚硝酸和
(3)四氧化二氮和偏二甲肼反应的化学方程式为:2N2O4+C2H8N2
 2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是
2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是(4)已知N2、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO2的质量为
II.二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
(5)将二氧化氯通入紫色石蕊试液中,溶液褪色的理由是
(6)设NA为阿伏加德罗常数的值,现有10g质量分数为64%的甲醇(CH3OH)水溶液,则该溶液所含氢原子数目为
(7)假设CO2和ClO2在标准状况下均为气体,则反应CH3OH+NaClO3+H2SO4 → CO2↑+ClO2↑+Na2SO4 +H2O(未配平)中转移的电子数目为0.6NA时,该反应产生标准状况下气体的体积为
您最近一年使用:0次
名校
4 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 mol·L-1 Na2SO4溶液中含钠离子的数目为2NA |
| B.标准状况下,22.4 L盐酸中含有NA个HCl分子 |
| C.1 mol Na被完全氧化生成Na2O2,失去2NA个电子 |
| D.常温常压下,8 g O2含有4NA个电子 |
您最近一年使用:0次
名校
5 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2 L Cl2溶于水,溶液中Cl-,ClO-和HClO的微粒数之和为NA |
| B.常温常压下,4.4gCO2与足量Na2O2充分反应,生成的O2分子数为0.1NA |
| C.标准状况下,11.2L CH4和C2H4混合气体中所含氢原子总数为2NA |
| D.7.8 g Na2O2固体中含有的阴离子数为0.2NA |
您最近一年使用:0次
名校
6 . NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,22.4LSO3中含有SO3的分子数为NA |
| B.1mol N2和3 molH2充分反应转移电子数为6NA |
| C.1molNO中含有氮原子数为NA |
| D.0.1mol/L Na2SO4溶液中含有的氧原子数为0.4NA |
您最近一年使用:0次
名校
7 . 设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.常温常压下,50g46%的乙醇水溶液中,含O-H键的总数为3NA |
| B.标准状况下,22.4L乙烷中含有的极性键的数目为6NA |
| C.90g葡萄糖分子中含羟基的数目为3NA |
| D.在浓硫酸、加热的条件下,0.5mol乙酸与足量乙醇充分反应,生成的乙酸乙酯分子数为0.5NA |
您最近一年使用:0次
名校
解题方法
8 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,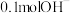 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为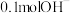 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近一年使用:0次
名校
解题方法
9 . 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A. 与足量 与足量 反应生成 反应生成 和 和 混合物,失去电子的数目为 混合物,失去电子的数目为 |
B.常温常压下,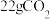 气体中含有的原子数为 气体中含有的原子数为 |
C. 与足量的铁反应,转移的电子数为 与足量的铁反应,转移的电子数为 |
D. 的 的 溶液中含 溶液中含 的数目为 的数目为 |
您最近一年使用:0次
名校
解题方法
10 . 向amLBaCl2、AlCl3和FeCl3的混合液A中;逐滴加入Na2SO4和NaOH的混合液B;产生沉淀的物质的量n与加入溶液B的体积关系如图所示;下列叙述正确的是
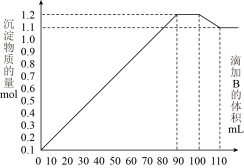
| A.溶液B中,硫酸钠和氢氧化钠的物质的量浓度之比为1:2 |
| B.溶液B中,Na+的物质的量浓度为3mol/L |
| C.当加入溶液B的体积>100mL时,溶液中才开始出现Na[Al(OH)4] |
| D.A溶液中Ba2+、Al3+和Fe3+的物质的量浓度之比为10:2:1 |
您最近一年使用:0次



