1 . 用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.2.24 L CO2中含有的原子数为0.3NA___________
2.常温下,11.2 L甲烷气体含有的甲烷分子数为0.5NA___________
3.标准状况下,含NA个Cl2分子的气体体积约为22.4 L___________
4.标准状况下,22.4 L SO3中含有SO3分子数为NA___________
5.标准状况下,22.4 L氧气、氮气和CO的混合气体中含有2NA个原子___________
6.用惰性电极电解饱和食盐水,若线路中通过NA个电子,则阴极产生11.2 L气体___________
1.2.24 L CO2中含有的原子数为0.3NA
2.常温下,11.2 L甲烷气体含有的甲烷分子数为0.5NA
3.标准状况下,含NA个Cl2分子的气体体积约为22.4 L
4.标准状况下,22.4 L SO3中含有SO3分子数为NA
5.标准状况下,22.4 L氧气、氮气和CO的混合气体中含有2NA个原子
6.用惰性电极电解饱和食盐水,若线路中通过NA个电子,则阴极产生11.2 L气体
您最近一年使用:0次
名校
解题方法
2 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是_______。
的说法中,不正确的是_______。
(4)请配平下述方程式,高铁酸钠 是一种新型的净水剂,可以通过此反应制取:
是一种新型的净水剂,可以通过此反应制取:

___
(5)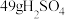 中含有
中含有_______ molH。
(6) 含
含 0.4mol,则
0.4mol,则 的摩尔质量是
的摩尔质量是_______ g/mol。
(7)32g某气体氧化物 标准状况下的体积为11.2L,该气体的物质的量为
标准状况下的体积为11.2L,该气体的物质的量为_______ mol,摩尔质量是_______ g/mol。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气  通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放  ,即可达到卫生标准 ,即可达到卫生标准 |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是_______。
的说法中,不正确的是_______。| A.是强氧化性的盐 | B.固体保存需要防潮 |
| C.其消毒和净化水的原理相同 | D.其净水优点有:作用快、安全性好、无异味 |
 是一种新型的净水剂,可以通过此反应制取:
是一种新型的净水剂,可以通过此反应制取:
(5)
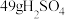 中含有
中含有(6)
 含
含 0.4mol,则
0.4mol,则 的摩尔质量是
的摩尔质量是(7)32g某气体氧化物
 标准状况下的体积为11.2L,该气体的物质的量为
标准状况下的体积为11.2L,该气体的物质的量为
您最近一年使用:0次
2022-12-07更新
|
102次组卷
|
2卷引用:四川省内江市资中县第二中学2022-2023学年高二上学期期中考试化学试题
3 . I.根据硫及化合物相关性质回答以下问题:
(1)将 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
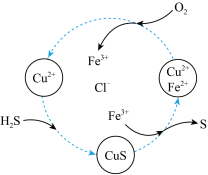
(2)过量的锌与一定量㳖 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为___________ 。使一定质量的Zn与 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为___________ g。
Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是___________ (用文字或者方程式表示)。
(4)将 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是___________ 。已知:pH越小表示溶液中 越大。
越大。
(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。
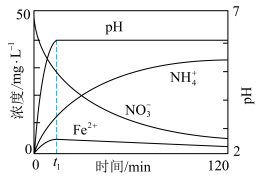
 前该反应的离子方程式是
前该反应的离子方程式是___________ 。
(1)将
 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
A. 和 和 反应的离子方程式为: 反应的离子方程式为: |
B. 在转化过程中发生的反应为: 在转化过程中发生的反应为: |
C.整个反应过程中溶液的pH值变小(不考虑产生的 的稀释效果) 的稀释效果) |
D.提高混合气体中 的比例可防止生成的硫单质中混有 的比例可防止生成的硫单质中混有 |
 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是
(4)将
 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是 越大。
越大。(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。

 前该反应的离子方程式是
前该反应的离子方程式是
您最近一年使用:0次
2023-08-07更新
|
198次组卷
|
2卷引用:四川省资阳中学2022-2023学年高一下学期4月月考化学试题
名校
解题方法
4 . 现有以下几种物质:①NaCl ②Ba(OH)2 ③CH4 ④醋酸(CH3COOH) ⑤NaHSO4 ⑥CO2 ⑦氨水 ⑧氢氧化铁胶体 ⑨FeCl3溶液。
回答下列问题:
(1)上述物质中属于电解质的是________ (填编号)。
(2)标准状况下,4.8g③与________ L⑥含有相同数目的原子。
(3)⑤溶于水的电离方程式为________ 。
(4)下列关于⑧和⑨的说法正确的是________ (填标号)。
A.⑧能产生丁达尔效应,而⑨不能
B.分散质微粒都可以通过滤纸
C.加入硫酸都会先产生沉淀,后溶解
D.将⑦滴加到⑨中可以制备⑧
(5)将少量⑥通入②溶液中,反应的离子方程式为________ 。
回答下列问题:
(1)上述物质中属于电解质的是
(2)标准状况下,4.8g③与
(3)⑤溶于水的电离方程式为
(4)下列关于⑧和⑨的说法正确的是
A.⑧能产生丁达尔效应,而⑨不能
B.分散质微粒都可以通过滤纸
C.加入硫酸都会先产生沉淀,后溶解
D.将⑦滴加到⑨中可以制备⑧
(5)将少量⑥通入②溶液中,反应的离子方程式为
您最近一年使用:0次
2020-11-17更新
|
86次组卷
|
2卷引用:山东省日照市莒县2020-2021学年高一11月模块考试化学试题
2023高三·全国·专题练习
解题方法
5 . NA为阿伏加德罗常数的值。下列说法错误的是___________ 。
A.25℃、101kPa下,28L氢气中质子的数目为2.5NA
B.1L1mol/LHCl溶液中,HCl分子的数目为NA
C.标准状况下,2.24LC2H5OH所含氢原子数为0.6NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
E.1.12LC2H4所含极性共价键的数目为0.2NA
F.0.1mol·L-1HClO4溶液中含有的H+数为0.1NA
G.11.2LNO与11.2LO2混合后的分子数目为NA
H.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
A.25℃、101kPa下,28L氢气中质子的数目为2.5NA
B.1L1mol/LHCl溶液中,HCl分子的数目为NA
C.标准状况下,2.24LC2H5OH所含氢原子数为0.6NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
E.1.12LC2H4所含极性共价键的数目为0.2NA
F.0.1mol·L-1HClO4溶液中含有的H+数为0.1NA
G.11.2LNO与11.2LO2混合后的分子数目为NA
H.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
您最近一年使用:0次
解题方法
6 . 用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
您最近一年使用:0次
7 . 用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA。(_______)
2.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,转移的电子数目为0.2NA。(_______)
3.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA。(_______)
4.1 mol Na2O2与足量CO2充分反应转移的电子数为2NA。(_______)
5.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移电子的数目不小于3NA。(_______)
6.1 mol Cl2参加反应转移电子数一定为2NA。(_______)
7.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数小于2NA。(_______)
8.0.3 mol NO2与足量的水反应转移电子数目为0.2NA。(_______)
1.5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA。(_______)
2.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,转移的电子数目为0.2NA。(_______)
3.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA。(_______)
4.1 mol Na2O2与足量CO2充分反应转移的电子数为2NA。(_______)
5.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移电子的数目不小于3NA。(_______)
6.1 mol Cl2参加反应转移电子数一定为2NA。(_______)
7.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数小于2NA。(_______)
8.0.3 mol NO2与足量的水反应转移电子数目为0.2NA。(_______)
您最近一年使用:0次
8 . 设NA代表阿伏加 德罗常数的数值,判定下列说法是否正确
1.22.4L(标准状况)氩气含有的质子数为18NA__________
2.标准状况下,11.2 LCH4和C2H4混合物中含氢原子数目为2NA__________
3.标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA__________
4.1mol的CO和N2混合气体中含有的质子数为14NA__________
5.标准状况下,5.6LCO2气体中含有的氧原子数目为0.5NA__________
6.1.6g由O2和O3组成的混合物中含有的O原子数目为0.1NA__________
7.常温常压下,8g O2含有的电子数为4NA__________
8.常温常压下,22.4LNO2和CO2的混合气体中O原子数目为2 NA__________
9.标准状况下,22.4LCCl4中含有的CCl4分子数为NA__________
10.常温常压下,18 g H2O中含有的原子总数为3NA__________
11.标准状况下,11.2LCH3CH2OH中含有的分子数目为0.5NA__________
12.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA__________
1.22.4L(标准状况)氩气含有的质子数为18NA
2.标准状况下,11.2 LCH4和C2H4混合物中含氢原子数目为2NA
3.标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
4.1mol的CO和N2混合气体中含有的质子数为14NA
5.标准状况下,5.6LCO2气体中含有的氧原子数目为0.5NA
6.1.6g由O2和O3组成的混合物中含有的O原子数目为0.1NA
7.常温常压下,8g O2含有的电子数为4NA
8.常温常压下,22.4LNO2和CO2的混合气体中O原子数目为2 NA
9.标准状况下,22.4LCCl4中含有的CCl4分子数为NA
10.常温常压下,18 g H2O中含有的原子总数为3NA
11.标准状况下,11.2LCH3CH2OH中含有的分子数目为0.5NA
12.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA
您最近一年使用:0次
解题方法
9 . (1)“民以食为天,食以安为先”。近年来屡屡发生的 劣质奶粉、苏丹红、多宝鱼等食品安全事件严重威胁消费者的健康和生命安全。下列有关蛋白质的说法正确的是____________ (填序号)。
A.蛋白质是重要的营养物质,也是提供人体所需能最的主要物质
B.蛋白质在淀粉酶的作用下,可水解成葡萄糖等
C.蛋白质水解的最终产物是氨基酸
(2)奶粉中蛋白质含量的国家标准是:每100 g婴幼儿奶粉中含蛋白质12〜25 g。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨, 由氨的量计算出氮的量,再由氮的量求出蛋白质的含量(蛋白质含氮量按16%计算)。某市质检局取100 g市场中的某个品牌的奶粉样品进行检验。该样品进行反应后生成的 和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉
和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉__________ (填“属于”或“不属于”)合格奶粉。
A.蛋白质是重要的营养物质,也是提供人体所需能最的主要物质
B.蛋白质在淀粉酶的作用下,可水解成葡萄糖等
C.蛋白质水解的最终产物是氨基酸
(2)奶粉中蛋白质含量的国家标准是:每100 g婴幼儿奶粉中含蛋白质12〜25 g。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨, 由氨的量计算出氮的量,再由氮的量求出蛋白质的含量(蛋白质含氮量按16%计算)。某市质检局取100 g市场中的某个品牌的奶粉样品进行检验。该样品进行反应后生成的
 和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉
和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉
您最近一年使用:0次
2020-04-09更新
|
306次组卷
|
5卷引用:课时3 糖类、油脂和蛋白质——A学习区 夯实基础(鲁科版(2019)第二册)
课时3 糖类、油脂和蛋白质——A学习区 夯实基础(鲁科版(2019)第二册)课时2 糖类、油脂、蛋白质在生产、生活中的应用——A学习区 夯实基础(人教版必修2)课时2 蛋白质——A学习区 夯实基础(人教版(2019)第二册)必修第二册RJ第7章第四节 基本营养物质 课时2 蛋白质(已下线)考点41 蛋白质-备战2023年高考化学一轮复习考点帮(全国通用)
10 . (1)0.5molCH4含_________ 个电子。
(2)下列物质既能导电,又属于电解质的是_______ 。
A NaCl溶液 B铁丝 C稀硫酸 D熔融的氢氧化钠 E 盐酸 F 硫酸
(3)同温同压下,甲容器中HCl气体和乙容器中的NH3所含原子个数相等,则甲乙两容器的体积之比为________ 。
(4)现配制500ml 0.3mol/L稀硫酸溶液,需用量筒量取质量分数为49%,密度为1.5g/cm3的浓硫酸_________ ml。
(5)①20℃、101kPa下,1g氢气和14g氮气的体积相同;
②常温常压下,16g氧气和臭氧的混合气体中含有的质子数为8NA
③0.1L 0.5mol/LCH3CH2OH溶液中含有氢原子数为0.3NA
④常温常压下,28gCO的体积大于22.4L;
⑤分子总数相等的NO2和CO2,所含氧原子数均为2NA。
以上说法正确的是_________________ 。
(2)下列物质既能导电,又属于电解质的是
A NaCl溶液 B铁丝 C稀硫酸 D熔融的氢氧化钠 E 盐酸 F 硫酸
(3)同温同压下,甲容器中HCl气体和乙容器中的NH3所含原子个数相等,则甲乙两容器的体积之比为
(4)现配制500ml 0.3mol/L稀硫酸溶液,需用量筒量取质量分数为49%,密度为1.5g/cm3的浓硫酸
(5)①20℃、101kPa下,1g氢气和14g氮气的体积相同;
②常温常压下,16g氧气和臭氧的混合气体中含有的质子数为8NA
③0.1L 0.5mol/LCH3CH2OH溶液中含有氢原子数为0.3NA
④常温常压下,28gCO的体积大于22.4L;
⑤分子总数相等的NO2和CO2,所含氧原子数均为2NA。
以上说法正确的是
您最近一年使用:0次



