解题方法
1 . 如图是一些常见含氯产品,根据情况回答下列问题。

(1)下列有关氯单质和氯水的说法正确的是________ (填序号)。
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)用化学方程式表示漂白粉的漂白原理________________________ ;
(3)向FeSO4溶液中滴加氯水,溶液变为黄色,写出反应的离子方程式_____
(4)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因________________________ (用离子方程式表示)。
(5)一定量铁粉与氯气充分反应后,加适量水,完全溶解后无固体剩余,此时所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的质量之比是________________________

(1)下列有关氯单质和氯水的说法正确的是
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)用化学方程式表示漂白粉的漂白原理
(3)向FeSO4溶液中滴加氯水,溶液变为黄色,写出反应的离子方程式
(4)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因
(5)一定量铁粉与氯气充分反应后,加适量水,完全溶解后无固体剩余,此时所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的质量之比是
您最近一年使用:0次
2020-01-26更新
|
196次组卷
|
3卷引用:山东省济宁市2019-2020学年高一上学期期末考试化学试题
2 . 高锰酸钾是一种典型的强氧化剂。完成下列填空:
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
② MnO +CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:___________
___________MnO +___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
+___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为___________ g。需要的玻璃仪器有___________
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(4)用软锰矿制备K2MnO4的化学方程式是:___________ 。
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为___________ 。
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO
 +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)② MnO
 +CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
___________MnO
 +___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
+___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(4)用软锰矿制备K2MnO4的化学方程式是:
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
名校
3 . 纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,其水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:_____ 。
(2)实验室中用过氧化氢制取氧气的化学方程式为____ ,当生成标准状况下1.12 L O2时,转移电子为___ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:___________ 。
(4)同学们用0.1000 mol·L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量。
①写出该反应的离子方程式____________ 。
②滴定到达终点的现象是____________ 。
③用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
则试样中过氧化氢的浓度为____ mol·L-1。
④若滴定前尖嘴中有气泡,滴定后消失,则测定结果____ (填“偏低”、“偏高”或“不变”)。
(5)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确___________ 。
(1)写出过氧化氢的电子式:
(2)实验室中用过氧化氢制取氧气的化学方程式为
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:
(4)同学们用0.1000 mol·L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量。
①写出该反应的离子方程式
②滴定到达终点的现象是
③用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 17.10 | 19.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为
④若滴定前尖嘴中有气泡,滴定后消失,则测定结果
(5)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确
您最近一年使用:0次
解题方法
4 . 氮及其化合物与生产生活关系密切。请完成下列填空:
(1)肼由N、H两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1:2。肼的分子式为_________ 。1mol的肼分子中含有的电子总数为_____ NA(NA为阿伏伽德罗常数的值)。16g肼分子中所含的氮原子数与标准状况下____ L N2中所含的氮原子数相等。
(2)在相同温度和压强下,体积相同的两个容器中分别盛有N2和O2。下列说法不正确的是____ (填序号)。
A.N2和O2的密度之比为7:8 B.两容器内的气体具有相同的分子数
C.两容器内的气体具有相同的原子数 D.两容器内的气体具有相同的质子数
(1)肼由N、H两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1:2。肼的分子式为
(2)在相同温度和压强下,体积相同的两个容器中分别盛有N2和O2。下列说法不正确的是
A.N2和O2的密度之比为7:8 B.两容器内的气体具有相同的分子数
C.两容器内的气体具有相同的原子数 D.两容器内的气体具有相同的质子数
您最近一年使用:0次
解题方法
5 . 随着科学技术的进步,硫及其化合物的研究越来越深入。
(1)共生工程可以促进化学工业的发展,并改善环境。
①下列有关环境问题的说法错误的是________ (填序号字母)。
a.空气中SO2浓度过高会加重呼吸系统和心脑血管疾病
b.SO2、NOx、CO2的大量排放都会造成酸雨
c.氮的氧化物和碳氢化合物大量排放可能引发光化学烟雾
d.“静电除尘”、“燃煤固硫”、“低碳经济”都能改善空气质量
②发电厂产生的SO2尾气中的可直接用氨水吸收,变废为宝。若用15L 2.0 mol 氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为
氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为________ 。
③利用发电厂产生的SO2制成以水为电解质的SO2质子交换膜燃料电池,该电池电动势为1. 06V。电池工作时负极反应式为________ 。
(2)将发电厂产生的SO2通入含有Na2S、Na2CO3的废液中可制得Na2S2O3·5H2O,通入SO2过程中的现象是:通了一段时间后,产生气体并析出沉淀,沉淀量逐渐增多;沉淀量逐渐减少并形成清液;停止通SO2,过滤后母液经蒸发浓缩,冷却得Na2S2O3·5H2O晶体(提示:)。上述过程中析出沉淀时发生的氧化还原反应的化学方程式为:________ 。调节废液中Na2S和Na2CO3的物质的量之比为________ ,时可以恰好完全反应生成Na2S2O3·5H2O。
(1)共生工程可以促进化学工业的发展,并改善环境。
①下列有关环境问题的说法错误的是
a.空气中SO2浓度过高会加重呼吸系统和心脑血管疾病
b.SO2、NOx、CO2的大量排放都会造成酸雨
c.氮的氧化物和碳氢化合物大量排放可能引发光化学烟雾
d.“静电除尘”、“燃煤固硫”、“低碳经济”都能改善空气质量
②发电厂产生的SO2尾气中的可直接用氨水吸收,变废为宝。若用15L 2.0 mol
 氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为
氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为③利用发电厂产生的SO2制成以水为电解质的SO2质子交换膜燃料电池,该电池电动势为1. 06V。电池工作时负极反应式为
(2)将发电厂产生的SO2通入含有Na2S、Na2CO3的废液中可制得Na2S2O3·5H2O,通入SO2过程中的现象是:通了一段时间后,产生气体并析出沉淀,沉淀量逐渐增多;沉淀量逐渐减少并形成清液;停止通SO2,过滤后母液经蒸发浓缩,冷却得Na2S2O3·5H2O晶体(提示:)。上述过程中析出沉淀时发生的氧化还原反应的化学方程式为:
您最近一年使用:0次
6 . 化学计量在化学中占有重要地位,请回答下列问题:
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g。
①两种气体总的物质的量为 。② C与O原子个数比为 。
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
①下列的相关说法正确的是 (填序号)。
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
② 盐酸的物质的量浓度 ,合金中镁的质量分数 。
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g。
①两种气体总的物质的量为 。② C与O原子个数比为 。
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 8.8 | 17.6 | 22.0 |
| 气体体积/L | 2.24 | 4.48 | 4.48 |
①下列的相关说法正确的是 (填序号)。
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
② 盐酸的物质的量浓度 ,合金中镁的质量分数 。
您最近一年使用:0次
10-11高三·安徽·阶段练习
7 . 为《京都议定书》2012年第一承诺期到期后的温室气体减排问题,世界各国都做出了不同的努力。随着新能源的开发和利用,CH3OH这个物质逐渐进入人们的视野,越来越受到人们的关注。

(1)下图是由CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示。下列相关说法正确的是( )
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-510kJ/mol
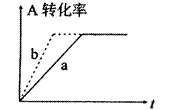
(2)由(1)推断,CO(g)+2H2(g) CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是
CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
A.增大CO的浓度 B.缩小容器的容积
C.加入催化剂 D.升高温度
(3)由甲醇和氧气以及强碱做电解质溶液的新型燃料电池,正在逐步推广使用,假定放电过程中,甲醇完全氧化产生二氧化碳被充分吸收生成CO32-。该电池的负极反应的离子方程式为_________________________ ,放电过程中电池里溶液的pH将_________ (填“下降”、“上升”或“不变”);若有16克甲醇被完全氧化产生电能,并利用该过程中释放的电能电解足量的硫酸铜溶液,假设能量的利用率为80%。则得到氧气的物质的量是____________ 。
(4)某同学将甲醇完全燃烧生成CO2气体通入200mL 0.1 mol/L的石灰水后,得到lg沉淀,那么通入的CO2的体积可能为(标态)____________ 。

(1)下图是由CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示。下列相关说法正确的是
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-510kJ/mol
(2)由(1)推断,CO(g)+2H2(g)
 CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是
CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是
A.增大CO的浓度 B.缩小容器的容积
C.加入催化剂 D.升高温度
(3)由甲醇和氧气以及强碱做电解质溶液的新型燃料电池,正在逐步推广使用,假定放电过程中,甲醇完全氧化产生二氧化碳被充分吸收生成CO32-。该电池的负极反应的离子方程式为
(4)某同学将甲醇完全燃烧生成CO2气体通入200mL 0.1 mol/L的石灰水后,得到lg沉淀,那么通入的CO2的体积可能为(标态)
您最近一年使用:0次



