解题方法
1 . 某水培植物的营养液中各离子的物质的量浓度如表所示(不考虑其他离子):
则x的值为
| 离子 |  |  |  |  |
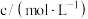 |  | 0.016 | 0.02 | 0.05 |
| A.0.014 | B.0.018 | C.0.054 | D.0.086 |
您最近一年使用:0次
2 . 根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为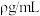 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与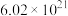 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
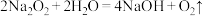 ,
,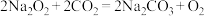 表示。若生成标况下
表示。若生成标况下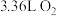 ,转移电子的数目为
,转移电子的数目为(4)现有
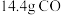 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为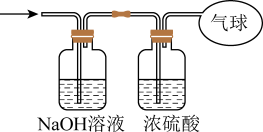
您最近一年使用:0次
3 . 现有下列物质:①铜丝②FeCl3溶液③氯化氢气体④NaHSO4固体⑤干冰⑥ 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体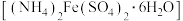 ⑧稀氨水
⑧稀氨水
(1)上述物质中属于电解质的是___________ (填序号,下同),能够导电的是___________ 。写出属于酸式盐的物质溶于水的电离方程式___________ 。
(2)②与⑧在溶液中反应的离子方程式为___________ 。
(3)硫酸亚铁铵晶体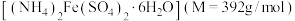 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制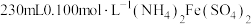 溶液,回答问题:
溶液,回答问题:
①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需___________ 。
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体___________ g。
③下列操作将导致所配制的溶液浓度偏高的是___________ (填选项)。
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是___________ mol·L-1(列出计算式)。
 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体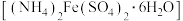 ⑧稀氨水
⑧稀氨水(1)上述物质中属于电解质的是
(2)②与⑧在溶液中反应的离子方程式为
(3)硫酸亚铁铵晶体
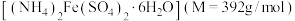 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制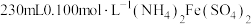 溶液,回答问题:
溶液,回答问题:①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体
③下列操作将导致所配制的溶液浓度偏高的是
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是
您最近一年使用:0次
名校
4 . 下列关于物质的量浓度表述正确的是
A.将7.8g  溶于水,配成100g溶液,所得溶液质量分数为7.8% 溶于水,配成100g溶液,所得溶液质量分数为7.8% |
B.质量分数为3.65%的200g盐酸溶液中,含 分子的数目为 分子的数目为 |
C.将25g胆矾( )溶于75克水中,可得到质量分数为16% )溶于75克水中,可得到质量分数为16% 的溶液 的溶液 |
D.将7.1g  通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 |
您最近一年使用:0次
名校
解题方法
5 . 计算题
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为___________ mol/L。
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是___________ L。(用含字母的式子表示,NA表示阿伏伽德罗常数)
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为___________ g。
(4)在VL硫酸铁溶液中,含有agFe3+,取出 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为
(4)在VL硫酸铁溶液中,含有agFe3+,取出
 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
6 . 回答下列问题
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是___________ ,属于混合物的是___________ (填编号)
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下, 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为___________ 。
②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为___________ mL。
③相同体积的 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为
①配平该反应:_______

②当有32g硫单质完全反应时,生成氧化产物的物质的量是___________ mol。
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下,
 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入
 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为③相同体积的
 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为

①配平该反应:

②当有32g硫单质完全反应时,生成氧化产物的物质的量是
您最近一年使用:0次
7 . 某氯化钠注射液标签如图,下列说法正确的是
| 氯化钠注射液 【规格】 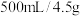 【适应症】各种原因所致的失水等 【用法】静脉滴注 |
A.该注射液中 的物质的量浓度为 的物质的量浓度为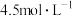 |
| B.用洁净的铂丝蘸取该注射液在酒精灯上灼烧,火焰会呈紫色 |
| C.该注射液中阴离子所带的负电荷总量等于阳离子所带的正电荷总量 |
| D.用光束来照射该注射液,会产生丁达尔效应 |
您最近一年使用:0次
解题方法
8 . 根据所学知识,回答下列问题:
(1)下图是中学化学中常用于混合物的分离和提纯的装置:
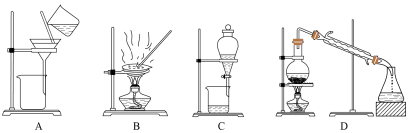
①分离花生油和水的混合物,选择装置_____ (填字母,下同)。
②提纯粗盐,并得到氯化钠晶体,选择装置_____ 。
③用 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置_____ 。
④除去自来水中的 等杂质,选择装置
等杂质,选择装置_____ 。
(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为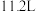 的
的 的质量为
的质量为_____ g。
②标准状况下, 某气体的质量为
某气体的质量为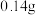 ,则其摩尔质量为
,则其摩尔质量为_____  。
。
③等物质的量的 和
和 中氢原子个数比是
中氢原子个数比是_____ 。
④ 的
的 溶液中含有的
溶液中含有的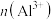 是
是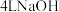 溶液中
溶液中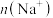 的两倍,则
的两倍,则
_____  。
。
(1)下图是中学化学中常用于混合物的分离和提纯的装置:

①分离花生油和水的混合物,选择装置
②提纯粗盐,并得到氯化钠晶体,选择装置
③用
 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置④除去自来水中的
 等杂质,选择装置
等杂质,选择装置(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为
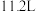 的
的 的质量为
的质量为②标准状况下,
 某气体的质量为
某气体的质量为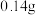 ,则其摩尔质量为
,则其摩尔质量为 。
。③等物质的量的
 和
和 中氢原子个数比是
中氢原子个数比是④
 的
的 溶液中含有的
溶液中含有的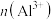 是
是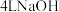 溶液中
溶液中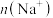 的两倍,则
的两倍,则
 。
。
您最近一年使用:0次
9 . 完成下列填空:
(1)标准状况下,5.6LA气体的质量是11g,则A的相对分子质量为__________ 。
(2)标准状况下, 个
个 分子所占的体积为
分子所占的体积为__________ L,它与__________ 个 分子含有相同数目的氢原子。
分子含有相同数目的氢原子。
(3)将 溶解在水中,配成500mL溶液,所得溶液中
溶解在水中,配成500mL溶液,所得溶液中 物质的量浓度为
物质的量浓度为__________ mol/L。
(4)同温同压下,相同体积的 和
和 的质子数之比为
的质子数之比为__________ 。
(5)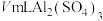 溶液中含
溶液中含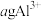 ,取出
,取出 溶液稀释成
溶液稀释成 后,
后, 的物质的量浓度为
的物质的量浓度为__________ mol/L。(用含a、V的代数式表示)
(1)标准状况下,5.6LA气体的质量是11g,则A的相对分子质量为
(2)标准状况下,
 个
个 分子所占的体积为
分子所占的体积为 分子含有相同数目的氢原子。
分子含有相同数目的氢原子。(3)将
 溶解在水中,配成500mL溶液,所得溶液中
溶解在水中,配成500mL溶液,所得溶液中 物质的量浓度为
物质的量浓度为(4)同温同压下,相同体积的
 和
和 的质子数之比为
的质子数之比为(5)
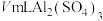 溶液中含
溶液中含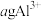 ,取出
,取出 溶液稀释成
溶液稀释成 后,
后, 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
10 . 实验室需要使用240mL0.2mol·L-1 CuSO4溶液(配制过程如图所示),下列说法正确的是
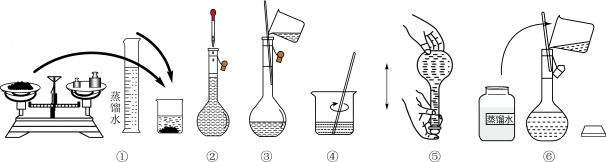

| A.上述操作步骤均规范正确 |
| B.配制操作的正确顺序为①④⑥③②⑤ |
C.若用CuSO4 5H2O固体配制,则需要称量12.5 g CuSO4 5H2O固体配制,则需要称量12.5 g CuSO4 5H2O固体 5H2O固体 |
| D.步骤⑤后发现液面低于刻度线,再加水定容,所配溶液的浓度会偏高 |
您最近一年使用:0次
2023-02-14更新
|
265次组卷
|
4卷引用:陕西省咸阳市实验中学2023-2024学年高一上学期段性检测(三)化学试题



