1 . 现有一份Fe2(SO4)3和(NH4)2SO4的混合溶液,向该溶液中加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液的体积关系如图。

(1)Ba(OH)2溶液的物质的量浓度为___________ mol·L-1。
(2)该混合溶液中Fe2(SO4)3和(NH4)2SO4物质的量之比为___________ 。

(1)Ba(OH)2溶液的物质的量浓度为
(2)该混合溶液中Fe2(SO4)3和(NH4)2SO4物质的量之比为
您最近一年使用:0次
2017-09-26更新
|
245次组卷
|
3卷引用:浙江省丽水衢州湖州三地市2018届高三9月教学质量检测化学试题
名校
解题方法
2 . Ⅰ.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH30.4mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量之差为17.3g。

(1)甲室中HCl、N2的质量之比为__________________ 。
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“________ ’’处(填数字,不考虑固体物质产生的压强),此时体系的平均相对分子质量为________ 。
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
(1)表中硫酸的质量分数为________ (不写单位,用含c1、ρ1,的代数式表示)。
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________ mol•L-1。
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度__________ 0.6c2 mol•L-1(填“大于”、“小于”或“等于”)(设混合后溶液的体积变化忽略不计)
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
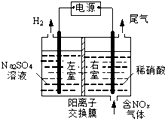
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:_________________________________ 。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为________ mol。

(1)甲室中HCl、N2的质量之比为
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量浓度/mol•L-1 | 溶液的密度/g•cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为
您最近一年使用:0次
名校
3 . 碳及其化合物广泛存在于自然界中,试回答下列问题:
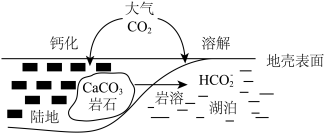
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为_____________ 。
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O H2CO3 K=10-2.8
H2CO3 K=10-2.8
②H2CO3 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,
③HCO3- H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,
若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=_____ 。
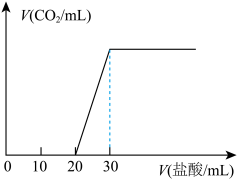
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为______________ (不用写出H+),湖水中无机碳的浓度为_______ mol/L。
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g) CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
①P1______ P2(填“大于”、“小于”或“等于”);
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为______ 。
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_______ 。
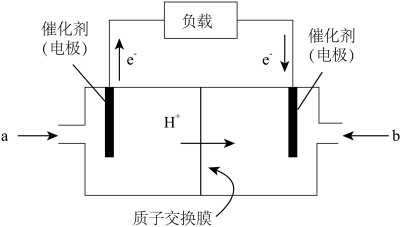
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:__________ 。
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O
 H2CO3 K=10-2.8
H2CO3 K=10-2.8②H2CO3
 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,③HCO3-
 H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g)
 CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。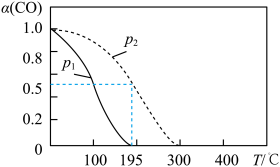
①P1
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:
您最近一年使用:0次
2017-04-18更新
|
1023次组卷
|
3卷引用:2017届江西省宜春市高三第二次模拟考试化学试卷
4 . 如图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_______ mol/L.
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的_________ .
A、溶液中H+的物质的量浓度 B、溶液中HCl的质量
C、溶液中H+的数目 D、溶液的密度
(3)若现有1L 1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施最合理的是____________ .
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0.5L
C、往原溶液加入5mol/L盐酸0.6L,再稀释至2L
D、往原溶液加入1L 3mol/L盐酸混合均匀.
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的
A、溶液中H+的物质的量浓度 B、溶液中HCl的质量
C、溶液中H+的数目 D、溶液的密度
(3)若现有1L 1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施最合理的是
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0.5L
C、往原溶液加入5mol/L盐酸0.6L,再稀释至2L
D、往原溶液加入1L 3mol/L盐酸混合均匀.
您最近一年使用:0次
2017-03-20更新
|
848次组卷
|
2卷引用:2017届浙江省温州中学高三3月高考模拟化学试卷
解题方法
5 . 已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________ ,剩余Fe2+的物质的量为________ 。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________ ,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________ 。
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是_________________________________________________ 。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________ ;上述所有反应共消耗Cl2________ mol。
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
1191次组卷
|
2卷引用:云南省文山州2018届高三毕业生复习统一检测理综化学试题
6 . 目前,我国采用“接触法”制硫酸,设备如图所示:
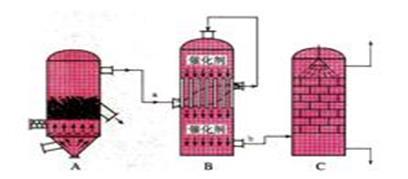
(1)图中设备A的名称是______________ ,该设备中主要反应的化学方程式为____________ 。
(2)有关接触法制硫酸的下列说法中,不正确的是______________________
(3)用18 mol/L 的浓硫酸配制100 mL 3.6 mol/L 稀硫酸,所需浓硫酸的体积是_______ 。

(1)图中设备A的名称是
(2)有关接触法制硫酸的下列说法中,不正确的是
| A.二氧化硫的接触氧化在接触室中发生 |
| B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫 |
| C.B装置中反应的条件之一为较高温度是为了提高SO2的转化率 |
| D.硫酸工业中在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
(3)用18 mol/L 的浓硫酸配制100 mL 3.6 mol/L 稀硫酸,所需浓硫酸的体积是
您最近一年使用:0次



