名校
解题方法
1 . 化学计量在生产和科研中应用广泛。回答下列问题:
(1) 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为___________ ,其质子的物质的量为___________ 。
(2)某气态氧化物的化学式为 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)若 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为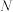 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为___________ (用含字母的代数式表示)。
(4)标准状况下将a LX气体(摩尔质量为 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________ 。
(5)将 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为___________ (忽略混合前后溶液体积的变化)。
(6)某混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
___________ 。
(1)
 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为(2)某气态氧化物的化学式为
 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为(3)若
 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为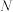 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为(4)标准状况下将a LX气体(摩尔质量为
 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)将
 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为(6)某混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
您最近一年使用:0次
2023-09-21更新
|
227次组卷
|
2卷引用:河南省部分名校2023-2024学年高三上学期核心模拟考试(一)化学试题
2 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
解题方法
3 . 单质硫在热的NaOH溶液中发生如下反应:3S+6NaOH 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。
请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=____ 。
(2)NaClO溶液的物质的量浓度为____ mol·L-1 (写出计算过程)。
 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=
(2)NaClO溶液的物质的量浓度为
您最近一年使用:0次
2022-04-16更新
|
407次组卷
|
2卷引用:浙江省宁波市2022届高三下学期高考模拟考试(二模)化学试题
4 . 以下方法常用于对废水中的苯酚进行定量测定:取 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.
(1)消耗 的物质的量为
的物质的量为________ .
(2)废水中苯酚的物质的量浓度为_______ (写出简要计算过程).
 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.(1)消耗
 的物质的量为
的物质的量为(2)废水中苯酚的物质的量浓度为
您最近一年使用:0次
5 . 确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别加入30.0 mL某浓度的稀硫酸中,充分反应后, 每组样品剩余固体的质量与原样品质量的关系如图所示。

(1)该混合物中,n(Fe2O3):n(Cu)=___________ 。
(2)稀硫酸的物质的量浓度为___________ 。

(1)该混合物中,n(Fe2O3):n(Cu)=
(2)稀硫酸的物质的量浓度为
您最近一年使用:0次
2021-05-29更新
|
958次组卷
|
5卷引用:【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)
【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00147】(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题浙江省舟山市舟山中学2022-2023学年高一上学期12月质量检测化学试题
解题方法
6 . 为确定某碱式碳酸镁 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸(
的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 为
为 ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
(1)98%的硫酸溶液物质的量浓度是___________ ;
(2)根据实验测定的数据,求出碱式碳酸镁化学式中X、Y、Z的比值(要求写出计算过程)___________ 。
 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸(
的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 为
为 ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:(1)98%的硫酸溶液物质的量浓度是
(2)根据实验测定的数据,求出碱式碳酸镁化学式中X、Y、Z的比值(要求写出计算过程)
您最近一年使用:0次
2021-05-04更新
|
718次组卷
|
4卷引用:浙江省台州市2021届高三4月选考科目教学质量评估试题(二模)化学试题
浙江省台州市2021届高三4月选考科目教学质量评估试题(二模)化学试题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题浙江省杭州市富阳区场口中学、桐庐富春中学2021-2022学年高二下学期(3月)检测化学试题
7 . 标准状况下,向多份等量的NaOH固体中,分别加入一定体积的1.00mol/L (NH4)2Fe(SO4)2溶液充分反应,反应产生的NH3随(NH4)2Fe(SO4)2溶液体积的变化如图所示(假设生成的NH3全部逸出):

请计算:
(1)a的值为_______ L。
(2)每份NaOH固体的物质的量_______ mol(写出计算过程)。

请计算:
(1)a的值为
(2)每份NaOH固体的物质的量
您最近一年使用:0次
8 . 已知粗盐水中含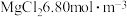 ,含
,含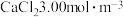 。向粗盐水中加入
。向粗盐水中加入 除Mg2+:MgCl2+Ca(OH)2→Mg(OH)2↓+CaCl2。然后加入
除Mg2+:MgCl2+Ca(OH)2→Mg(OH)2↓+CaCl2。然后加入 除
除 。
。
(1)处理上述粗盐水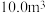 ,至少需要加
,至少需要加
________  。(保留三位有效数字)
。(保留三位有效数字)
(2)如果用碳酸化尾气(含 体积分数为0.100、
体积分数为0.100、 体积分数0.0400)代替碳酸钠,发生如下反Ca2++2NH3+CO2+H2O→CaCO3↓+2
体积分数0.0400)代替碳酸钠,发生如下反Ca2++2NH3+CO2+H2O→CaCO3↓+2 。处理上述
。处理上述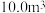 粗盐水至少需要通入标准状况下
粗盐水至少需要通入标准状况下________ 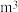 碳酸化尾气。(需列式计算,保留三位有效数字)
碳酸化尾气。(需列式计算,保留三位有效数字)
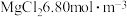 ,含
,含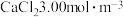 。向粗盐水中加入
。向粗盐水中加入 除Mg2+:MgCl2+Ca(OH)2→Mg(OH)2↓+CaCl2。然后加入
除Mg2+:MgCl2+Ca(OH)2→Mg(OH)2↓+CaCl2。然后加入 除
除 。
。(1)处理上述粗盐水
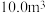 ,至少需要加
,至少需要加
 。(保留三位有效数字)
。(保留三位有效数字)(2)如果用碳酸化尾气(含
 体积分数为0.100、
体积分数为0.100、 体积分数0.0400)代替碳酸钠,发生如下反Ca2++2NH3+CO2+H2O→CaCO3↓+2
体积分数0.0400)代替碳酸钠,发生如下反Ca2++2NH3+CO2+H2O→CaCO3↓+2 。处理上述
。处理上述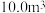 粗盐水至少需要通入标准状况下
粗盐水至少需要通入标准状况下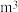 碳酸化尾气。(需列式计算,保留三位有效数字)
碳酸化尾气。(需列式计算,保留三位有效数字)
您最近一年使用:0次
2010·上海·二模
9 . 过碳酸钠是一种有多用途的新型氧系漂白剂,化学式可表示为aNa2CO3·bH2O2。现将一定质量的过碳酸钠粉末溶于水配成稀溶液,再向其中加入适量MnO2粉末,充分反应后生成672mL气体(标准状况)。反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100mL溶液A。现向三份体积为10mL、浓度为c mol/L的稀硫酸中分别逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
(1)计算稀硫酸的物质的量浓度___ 。
(2)通过计算确定过碳酸钠的化学式___ 。
(3)工业上常以所含活性氧的质量分数[w(活性氧)= ×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品___ 。(已知:2Na2S2O3+I2→Na2S4O6+2NaI)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 10.0 | 20.0 | 30.0 |
| 生成气体的体积/mL(标准状况) | 89.6 | 179.2 | 224 |
(1)计算稀硫酸的物质的量浓度
(2)通过计算确定过碳酸钠的化学式
(3)工业上常以所含活性氧的质量分数[w(活性氧)=
 ×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
您最近一年使用:0次
2010·上海·二模
解题方法
10 . 将Cu与CuO的混合物22.4g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解,冷却后将混合液稀释至1000mL,测得c(Cu2+)=0.3mol/L。试计算:
(1)反应过程中放出的气体在标准状况下的体积___ (不考虑气体在溶液中的溶解)。
(2)溶液稀释后,c(H+)是多少___ ?
(1)反应过程中放出的气体在标准状况下的体积
(2)溶液稀释后,c(H+)是多少
您最近一年使用:0次



