1 . 回答下列问题:
(1)标准状况下,5.6LCO物质的量是______ ,质量______ 。相同质量的CO和CO2所含原子个数比是_____ 。20gNaOH溶于水得到0.5升溶液其物质的量浓度为______ mol•L-1。
(2)NH4NO3是______ (填电解质或非电解质),写出硫酸铁的电离方程式______ 。
(3)写出将碳酸氢钠溶液与稀盐酸混合,反应的离子方程式为______ ;向氯化亚铁溶液中通入氯气的离子方程式是______ 。
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式(未配平)表示为:
_______ClO-+_______Fe3++_______OH-=_______FeO +_______Cl-+_______H2O
+_______Cl-+_______H2O
请配平上述反应方程式______ ;上述反应中氧化剂是______ ,还原剂是______ 。
(1)标准状况下,5.6LCO物质的量是
(2)NH4NO3是
(3)写出将碳酸氢钠溶液与稀盐酸混合,反应的离子方程式为
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式(未配平)表示为:
_______ClO-+_______Fe3++_______OH-=_______FeO
 +_______Cl-+_______H2O
+_______Cl-+_______H2O请配平上述反应方程式
您最近一年使用:0次
2 . 已知某市售“84”消毒液的有效成分为NaClO,其溶质的质量分数为30%,密度为1.49g/cm3。使用“84”消毒液时,通常需加水稀释100倍。回答下列问题:
(1)市售“84”消毒液中c(NaClO)=______ mol•L-1。
(2)实际使用时,将“84”消毒液与醋酸(CH3COOH)混合使用可增强其消毒能力。某消毒小组人员将浓度约为18mol•L-1的浓醋酸配制成500mL0.2mol•L-1稀醋酸,用于增强“84”消毒液的消毒能力。
①本实验中,所用的玻璃仪器除量筒、烧杯、胶头滴管外,还需要用到的其他仪器有______ 、______ 。
②根据计算得知,得用量筒量取浓醋酸的体积为______ mL。
③下列操作中,会导致所配溶液的物质的量浓度偏低的有______ (填标号)
A.将溶液往容量瓶中转移时,有少量液体溅出
B.未洗涤稀释浓醋酸的烧杯
C.容量瓶未干燥即用来配制溶液
D.定容时俯视刻度线
E.定容后经振荡、摇匀、静置后,发现液面下降,再加入适量的蒸馏水
(3)NaClO是“84”消毒掖的有效成分,因吸收空气中CO2使消毒杀菌能力增强,其中发生的化学反应的规律是:______与______反应生成______和______(填物质类别名称)______ 。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原因是NaClO将H2O2氧化产生的O2促进藻类快速生长。该反应说明氧化性:NaClO______ H2O2的(填“>”或“<”)。
(1)市售“84”消毒液中c(NaClO)=
(2)实际使用时,将“84”消毒液与醋酸(CH3COOH)混合使用可增强其消毒能力。某消毒小组人员将浓度约为18mol•L-1的浓醋酸配制成500mL0.2mol•L-1稀醋酸,用于增强“84”消毒液的消毒能力。
①本实验中,所用的玻璃仪器除量筒、烧杯、胶头滴管外,还需要用到的其他仪器有
②根据计算得知,得用量筒量取浓醋酸的体积为
③下列操作中,会导致所配溶液的物质的量浓度偏低的有
A.将溶液往容量瓶中转移时,有少量液体溅出
B.未洗涤稀释浓醋酸的烧杯
C.容量瓶未干燥即用来配制溶液
D.定容时俯视刻度线
E.定容后经振荡、摇匀、静置后,发现液面下降,再加入适量的蒸馏水
(3)NaClO是“84”消毒掖的有效成分,因吸收空气中CO2使消毒杀菌能力增强,其中发生的化学反应的规律是:______与______反应生成______和______(填物质类别名称)
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原因是NaClO将H2O2氧化产生的O2促进藻类快速生长。该反应说明氧化性:NaClO
您最近一年使用:0次
解题方法
3 . 环境友好安全型的“绿色”引爆炸药,其中一种可表示为Na2R,它保存在水中可以失去活性,爆炸后不会产生危害性残留物。已知10mLNa2R溶液含Na+的数目为N,该Na2R溶液的物质的量浓度为
| A.N×10-2mol•L-1 | B. mol•L-1 mol•L-1 |
C. mol•L-1 mol•L-1 | D. mol•L-1 mol•L-1 |
您最近一年使用:0次
解题方法
4 . 下列有关溶液物质的量浓度的计算中正确的有
①从1L0.1mol/LNaCl溶液中取出250mL,剩余溶液中c(Cl-)=0.075mol/L
②配制480mL0.10mol/L的CuSO4溶液,需称取12.5g胆矾
③将4.48LHCl通入水中配成500mL溶液,所得溶液中c(HCl)=0.4mol/L
④将30mL0.5mol/L的Na2SO4溶液加水稀释到500mL,稀释后溶液中c(Na+)=0.06mol/L
①从1L0.1mol/LNaCl溶液中取出250mL,剩余溶液中c(Cl-)=0.075mol/L
②配制480mL0.10mol/L的CuSO4溶液,需称取12.5g胆矾
③将4.48LHCl通入水中配成500mL溶液,所得溶液中c(HCl)=0.4mol/L
④将30mL0.5mol/L的Na2SO4溶液加水稀释到500mL,稀释后溶液中c(Na+)=0.06mol/L
| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
名校
5 . 工业烟气含有 ,可以用
,可以用 溶液进行绿色化处理后再排放。设
溶液进行绿色化处理后再排放。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,可以用
,可以用 溶液进行绿色化处理后再排放。设
溶液进行绿色化处理后再排放。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.6.4 g  含有的电子数目为0.3 含有的电子数目为0.3 |
B.1 L 1   溶液中 溶液中 的数目为2 的数目为2 |
C.22.4 L (标准状况)与足量氧气反应,转移电子数目为2 (标准状况)与足量氧气反应,转移电子数目为2 |
D.1  溶液最多能吸收 溶液最多能吸收 的数目为0.1 的数目为0.1 |
您最近一年使用:0次
2023-02-27更新
|
1548次组卷
|
7卷引用:西安市第八十三中学2022-2023学年高一下学期第一次月考化学试题
解题方法
6 . 下列溶液中 物质的量浓度最大的是
物质的量浓度最大的是
 物质的量浓度最大的是
物质的量浓度最大的是A. 的 的 溶液 溶液 | B. 的 的 溶液 溶液 |
C.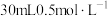 的 的 溶液 溶液 | D.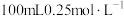 的 的 溶液 溶液 |
您最近一年使用:0次
解题方法
7 . 将5.3gNa2CO3固体配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为
| A.0.05mol/L | B.0.1mol/L | C.0.2mol/L | D.0.3mol/L |
您最近一年使用:0次
2023-02-17更新
|
180次组卷
|
3卷引用:四川省南充市 2022-2023 学年高一上学期期末考试化学试题
四川省南充市 2022-2023 学年高一上学期期末考试化学试题(已下线)第05讲 物质的量浓度-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)广东省惠州市龙门县高级中学2023-2024学年高一上学期12月月考化学试题
名校
8 . 下列叙述正确的是
A. 的食盐水中含氯化钠分子 的食盐水中含氯化钠分子 |
B.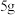 98%的硫酸(密度为 98%的硫酸(密度为 )与 )与 的硫酸浓度相等 的硫酸浓度相等 |
C.标准状况下, 氯化氢气体溶于 氯化氢气体溶于 水中,所得溶液物质的量浓度为 水中,所得溶液物质的量浓度为 |
D. 氢氧化钠溶于水配成物质的量浓度为 氢氧化钠溶于水配成物质的量浓度为 的溶液,所得溶液体积为 的溶液,所得溶液体积为 |
您最近一年使用:0次
名校
9 . 在 和
和 的混合溶液中,测得
的混合溶液中,测得 的浓度为
的浓度为 ,加入等体积
,加入等体积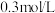 的
的 溶液恰好使
溶液恰好使 完全沉淀,则最终所得混合溶液中
完全沉淀,则最终所得混合溶液中 的浓度为(忽略反应前后溶液密度的变化)
的浓度为(忽略反应前后溶液密度的变化)
 和
和 的混合溶液中,测得
的混合溶液中,测得 的浓度为
的浓度为 ,加入等体积
,加入等体积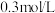 的
的 溶液恰好使
溶液恰好使 完全沉淀,则最终所得混合溶液中
完全沉淀,则最终所得混合溶液中 的浓度为(忽略反应前后溶液密度的变化)
的浓度为(忽略反应前后溶液密度的变化)A. | B. | C.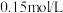 | D. |
您最近一年使用:0次
2023-02-16更新
|
418次组卷
|
4卷引用:吉林省长春市实验中学2022-2023学年高一上学期期末考试化学试题
吉林省长春市实验中学2022-2023学年高一上学期期末考试化学试题辽宁省大连市一0三中学2022-2023学年高一下学期3月月考化学试题(已下线)第06讲 物质的量浓度的相关计算-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)第12讲 物质的量浓度的相关计算-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
2023高三·全国·专题练习
10 .  溶液中,
溶液中, 的数目为
的数目为 。( )
。( )
 溶液中,
溶液中, 的数目为
的数目为 。( )
。( )
您最近一年使用:0次



