名校
解题方法
1 . 下列溶液中氯离子浓度最大的是
| A.1 mol•L﹣1的AlCl3 | B.2 mol•L﹣1的CaCl2 |
| C.2 mol•L﹣1的NH4Cl | D.1 mol•L﹣1的KCl |
您最近一年使用:0次
2 . 下列关于1molHCl的说法中,错误的是(NA表示阿伏加德罗常数的值)
| A.质量为36.5g |
| B.含氢原子数为NA |
| C.体积约为22.4L |
| D.溶于水后,所得1L溶液的物质的量浓度为1mol/L |
您最近一年使用:0次
3 . 化学与人类生产、生活密切相关,利用所学知识进行填空(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)下列物质能导电且属于电解质的是___________(填字母)。
(2)NaH可在野外作生氢剂,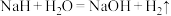 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)标准状况下,44.8L 对应的物质的量是
对应的物质的量是___________ ,其含有的共价键类型为___________ 键。(填极性或者非极性)
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是___________ (填化学式)
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为_______ 。
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(1)下列物质能导电且属于电解质的是___________(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
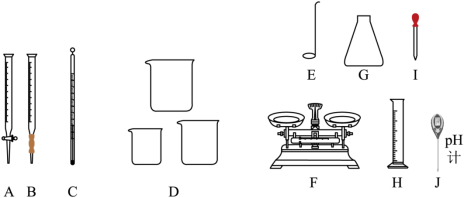
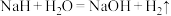 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)标准状况下,44.8L
 对应的物质的量是
对应的物质的量是(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
您最近一年使用:0次
名校
解题方法
4 . 某同学利用如下实验仪器及试剂完成酸碱中和反应反应热的测定实验。
仪器如下:
试剂:pH=1的盐酸、pH=1的醋酸、NaOH固体、酚酞、石蕊、蒸馏水。
回答下列有关问题:
(1)由于两瓶酸的标签已脱落,请利用上述仪器和试剂设计实验来确认哪一瓶是盐酸,实验方案:___________ 。
(2)①配制250mLNaOH溶液:由于缺少___________ (填仪器名称),无法准确配制0.1000mol·L-1的NaOH溶液。
②用中和滴定法测定新配制的NaOH溶液的物质的量浓度,其操作可分解为如下几步:
a.检查滴定管是否漏水;
b.取20.00mL的待测液于锥形瓶中,并滴加几滴指示剂;
c.用标准溶液润洗装标准溶液的滴定管,用待测液润洗装待测液的滴定管;
d.装标准溶液和待测液并调整液面(记录初读数);
e.用蒸馏水洗涤玻璃仪器;
f.进行滴定操作。
正确的操作顺序为___________ 。(填字母序号)
③选用0.1000mol·L-1的盐酸为标准溶液、___________ 作指示剂;滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视___________ ;直到___________ 为止。滴定结果如下所示:
则新配制的NaOH溶液的物质的量浓度为___________ mol·L-1.
(3)完成酸碱中和反应反应热的测定实验(溶液的密度均视为1g·mL-1,反应后生成溶液的比热容c=4.2J·g-1·°C-1):取碎纸条、硬纸板以及D、E、H组装好实验装置,实验中取50mLpH=1的盐酸与50mL新配制的NaOH溶液进行反应,若测得反应前后温差为0.67°C,经计算该实验中酸碱中和生成1mol水时放出的热量为56.28kJ,该数值与理论值(理论值为57.3kJ)有偏差,其原因可能是___________ (填字母序号)。
A.采用铜制搅拌棒
B.量筒量取NaOH溶液时仰视读数
C.分多次将NaOH溶液倒入装有盐酸的小烧杯中
D.测完HCl溶液的温度后,用水把温度计上的酸冲洗干净,擦干后,过一段时间再测量NaOH溶液的温度
仪器如下:

试剂:pH=1的盐酸、pH=1的醋酸、NaOH固体、酚酞、石蕊、蒸馏水。
回答下列有关问题:
(1)由于两瓶酸的标签已脱落,请利用上述仪器和试剂设计实验来确认哪一瓶是盐酸,实验方案:
(2)①配制250mLNaOH溶液:由于缺少
②用中和滴定法测定新配制的NaOH溶液的物质的量浓度,其操作可分解为如下几步:
a.检查滴定管是否漏水;
b.取20.00mL的待测液于锥形瓶中,并滴加几滴指示剂;
c.用标准溶液润洗装标准溶液的滴定管,用待测液润洗装待测液的滴定管;
d.装标准溶液和待测液并调整液面(记录初读数);
e.用蒸馏水洗涤玻璃仪器;
f.进行滴定操作。
正确的操作顺序为
③选用0.1000mol·L-1的盐酸为标准溶液、
| 次数 | 盐酸溶液起始读数 | 盐酸溶液终点读数 |
| 第一次 | 0.10mL | 23.75mL |
| 第二次 | 0.80mL | 24.40mL |
| 第三次 | 0.30mL | 23.85mL |
(3)完成酸碱中和反应反应热的测定实验(溶液的密度均视为1g·mL-1,反应后生成溶液的比热容c=4.2J·g-1·°C-1):取碎纸条、硬纸板以及D、E、H组装好实验装置,实验中取50mLpH=1的盐酸与50mL新配制的NaOH溶液进行反应,若测得反应前后温差为0.67°C,经计算该实验中酸碱中和生成1mol水时放出的热量为56.28kJ,该数值与理论值(理论值为57.3kJ)有偏差,其原因可能是
A.采用铜制搅拌棒
B.量筒量取NaOH溶液时仰视读数
C.分多次将NaOH溶液倒入装有盐酸的小烧杯中
D.测完HCl溶液的温度后,用水把温度计上的酸冲洗干净,擦干后,过一段时间再测量NaOH溶液的温度
您最近一年使用:0次
5 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.1.7 g NH3中含有的质子数约为6.02×1023 |
| B.1 mol N2与3 mol H2反应生成的NH3分子数为2NA |
| C.标准状况下,2.24 L CCl4含有的共价键数为0.4NA |
D.0.1 mol/L NH4Cl溶液中的NH 数约为0.1NA 数约为0.1NA |
您最近一年使用:0次
2024-03-17更新
|
348次组卷
|
2卷引用:湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . 下列溶液中Cl-的物质的量浓度最大的是
| A.250mL 1mol/L AlCl3溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.300mL 5mol/L KClO3溶液 | D.200mL 2mol/L MgCl2溶液 |
您最近一年使用:0次
7 . 有一水溶液含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 ,现取两份100 mL的该溶液分别进行如下实验(已知:
,现取两份100 mL的该溶液分别进行如下实验(已知: )
)
(1)第一份加足量NaOH溶液,加热,收集到标准状况下的气体1120mL。
(2)第二份加足量 溶液,得沉淀6.63g,再用足量盐酸洗涤、干燥后得沉淀质量为4.66g。
溶液,得沉淀6.63g,再用足量盐酸洗涤、干燥后得沉淀质量为4.66g。
根据上述实验,下列推测正确的是
 、
、 、
、 、
、 、
、 、
、 ,现取两份100 mL的该溶液分别进行如下实验(已知:
,现取两份100 mL的该溶液分别进行如下实验(已知: )
)(1)第一份加足量NaOH溶液,加热,收集到标准状况下的气体1120mL。
(2)第二份加足量
 溶液,得沉淀6.63g,再用足量盐酸洗涤、干燥后得沉淀质量为4.66g。
溶液,得沉淀6.63g,再用足量盐酸洗涤、干燥后得沉淀质量为4.66g。根据上述实验,下列推测正确的是
A.原溶液中肯定存在的离子为 、 、 、 、 、 、 |
B.原溶液中 的物质的量浓度一定为 的物质的量浓度一定为 |
C.原溶液中一定不存在 |
D.原溶液中 的物质的量浓度为 的物质的量浓度为 |
您最近一年使用:0次
2023-12-21更新
|
532次组卷
|
6卷引用:湖南省衡阳市衡阳县2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
8 . 将KCl、 、
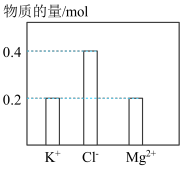
、 溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
 、
、 溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
溶于水配成混合溶液,溶液体积为1L,部分离子物质的量如图所示,下列说法错误的是
A.该混合溶液中 的物质的量为0.1mol 的物质的量为0.1mol |
B.若将该混合溶液加水稀释至体积为5L,稀释后溶液中 的物质的量浓度为 的物质的量浓度为 |
C.若向该混合溶液中逐滴加入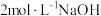 溶液至 溶液至 恰好完全沉淀,需NaOH溶液50mL 恰好完全沉淀,需NaOH溶液50mL |
D.该混合溶液中由 电离出的 电离出的 浓度为 浓度为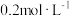 |
您最近一年使用:0次
2023-12-01更新
|
476次组卷
|
8卷引用:湖南省株洲市第二中学2023-2024学年高一下学期第二次阶段性测试化学试题
湖南省株洲市第二中学2023-2024学年高一下学期第二次阶段性测试化学试题 河北省名校强基联盟2023-2024学年高一上学期11月期中联考化学试题(已下线)【精品卷】2.3.3 物质的量浓度课堂例题-人教版2023-2024学年必修第一册陕西省西安市航天中学2023~2024学年高一上学期第三次月考化学试题 安徽省合肥市第一中学2023-2024学年高一上学期素质拓展训练(三)化学试题 江西省上饶市广信二中2023-2024学年高一上学期期中考试化学试卷江西省上饶市万年县第一中学2023-2024学年高一上学期第二次月考化学试题安徽省桐城中学2023-2024学年高一下学期开学检测化学试题
名校
9 . 下列叙述正确的是
A. 在标准状况下体积约为33.6L 在标准状况下体积约为33.6L |
B.常温常压下, 气体中含分子数为 气体中含分子数为 |
| C.等质量的氧气和臭气,所含电子数不相等 |
| D.80gNaOH溶解于1L水中,所得溶液物质的量浓度为2mol/L |
您最近一年使用:0次
2023-11-09更新
|
262次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一上学期期中考试化学试题
名校
10 . 下列说法正确的是
A.将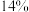 的 的 溶液蒸发掉 溶液蒸发掉 水后,变为 水后,变为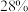 的 的 溶液 溶液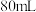 ,该 ,该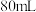 溶液的物质的量浓度为 溶液的物质的量浓度为 |
B.把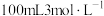 的 的 溶液与 溶液与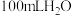 混合后,硫酸的物质的量浓度变为 混合后,硫酸的物质的量浓度变为 |
C.某 溶液的密度为 溶液的密度为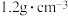 , , 的质量分数为 的质量分数为 , , 该溶液中 该溶液中 的物质的量为 的物质的量为 |
D.已知 氨水的密度为 氨水的密度为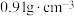 , , 氨水的密度为 氨水的密度为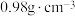 ,若将上述两溶液等体积混合,所得氨水的质量分数大于 ,若将上述两溶液等体积混合,所得氨水的质量分数大于 |
您最近一年使用:0次
2023-10-11更新
|
309次组卷
|
3卷引用:湖南省常德市汉寿县第一中学2022-2023学年高一上学期期中考试化学试题



