名校
解题方法
1 . 铅丹( )可用作防锈涂料,它与浓盐酸反应的化学方程式为:
)可用作防锈涂料,它与浓盐酸反应的化学方程式为: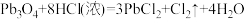 。设
。设 为阿伏加德罗常数值。下列说法不正确的是
为阿伏加德罗常数值。下列说法不正确的是
 )可用作防锈涂料,它与浓盐酸反应的化学方程式为:
)可用作防锈涂料,它与浓盐酸反应的化学方程式为: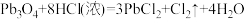 。设
。设 为阿伏加德罗常数值。下列说法不正确的是
为阿伏加德罗常数值。下列说法不正确的是A.标准状况下,22.4L H2O中,含有H原子数目大于2 |
B.1L 12 的浓盐酸与足量 的浓盐酸与足量 反应生成的 反应生成的 分子数少于1.5 分子数少于1.5 |
C.标准状况下,22.4L  溶于水所得溶液中含HClO分子数为 溶于水所得溶液中含HClO分子数为 |
D.反应中消耗137g  ,转移的电子数目为0.4 ,转移的电子数目为0.4 |
您最近一年使用:0次
名校
2 . 计算题
I.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量为_______ 。(写出计算过程,下同)
(2)反应后ZnCl2的物质的量浓度_______ 。
(3)生成H2的体积(标准状况)_______ 。
II.实验室用密度为 、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为_______ 。
I.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量为
(2)反应后ZnCl2的物质的量浓度
(3)生成H2的体积(标准状况)
II.实验室用密度为
 、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。(4)该浓盐酸中溶质的物质的量浓度为
您最近一年使用:0次
解题方法
3 . 计算题(写计算过程)
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量______ ?(写出计算过程,下同)
(2)反应后ZnCl2的物质的量浓度______ ?
(3)生成H2的体积(标准状况)_______ ?
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为_______ ?
(5)用该浓盐酸配制250mL1.0mol L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是________ ?
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量
(2)反应后ZnCl2的物质的量浓度
(3)生成H2的体积(标准状况)
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为
(5)用该浓盐酸配制250mL1.0mol
 L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是
您最近一年使用:0次
4 . 化学计量在化学中占有重要地位,回答下列问题:
(1)0.2 molSO2的质量是______________ g,在标准状况下的体积约为_______________ L。
(2)将4.0 gNaOH固体溶于水配成100mL溶液,
①该溶液中NaOH的物质的量浓度为_________________ 。
②从该溶液中取出10mL,其中NaOH的物质的量浓度为________________ ,含NaOH的质量为________________ 。
(3)配制100mL0.5mol L-1氯化钠溶液,需要2.0mol
L-1氯化钠溶液,需要2.0mol L-1的氯化钠溶液的体积是
L-1的氯化钠溶液的体积是________________ mL。
(4)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是________________ 。
(5)含0.4 molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是________________ 。
(6)0.2 molNH3与________________ gH2O具有相同的氢原子数。
(1)0.2 molSO2的质量是
(2)将4.0 gNaOH固体溶于水配成100mL溶液,
①该溶液中NaOH的物质的量浓度为
②从该溶液中取出10mL,其中NaOH的物质的量浓度为
(3)配制100mL0.5mol
 L-1氯化钠溶液,需要2.0mol
L-1氯化钠溶液,需要2.0mol L-1的氯化钠溶液的体积是
L-1的氯化钠溶液的体积是(4)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是
(5)含0.4 molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(6)0.2 molNH3与
您最近一年使用:0次
2023-12-12更新
|
138次组卷
|
2卷引用:宁夏吴忠市青铜峡市2023-2024学年高一上学期12月月考化学试题
名校
解题方法
5 . 食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035 g/mL。用标准NaOH溶液可以测定食醋中醋酸的浓度,以检测白醋是否符合国家标准。某品牌白醋的醋酸浓度测定过程如图所示,回答下列问题:

(1)某同学用酸碱中和滴定法测定市售食用白醋醋酸浓度,当醋酸与氢氧化钠恰好完全反应时,测得溶液中 ,则应该选
,则应该选___________ 作指示剂(填“酚酞”、“甲基橙”或“石蕊”)。(已知室温下醋酸的 )
)
(2)该滴定达到终点时的现象是___________ 。
(3)某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为___________ mL。

(4)用标准的0.06000mol/L NaOH溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
则该白醋中醋酸的物质的量浓度为___________ mol/L,该白醋___________ (填“符合”或“不符合”)国家标准。
(5)下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是_______ (填编号)。
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中振摇时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失

(1)某同学用酸碱中和滴定法测定市售食用白醋醋酸浓度,当醋酸与氢氧化钠恰好完全反应时,测得溶液中
 ,则应该选
,则应该选 )
)(2)该滴定达到终点时的现象是
(3)某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为

(4)用标准的0.06000mol/L NaOH溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 mL | 0.02 | 25.01 |
| 2 | 25.00 mL | 0.70 | 25.71 |
| 3 | 25.00 mL | 0.50 | 24.2 |
(5)下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中振摇时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
您最近一年使用:0次
名校
6 . 按要求解答问题。
(1)已知标准状况下,气体A的密度为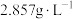 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为___________ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为___________ 。
(3)相同条件下,体积比为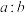 和质量比为
和质量比为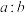 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是___________ 和___________ 。
(4)在标准状况下,将
 气体溶于
气体溶于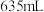 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:
①所得盐酸的质量分数和物质的量浓度分别是___________ 、___________ 。
②取这种盐酸 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度___________ 。
③在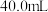

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过___________ mL。
(1)已知标准状况下,气体A的密度为
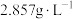 ,则气体A的相对分子质量约为
,则气体A的相对分子质量约为(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入
 A气体,Y中充入
A气体,Y中充入
 气体,X与Y内的压强之比是4:11,则A的摩尔质量为
气体,X与Y内的压强之比是4:11,则A的摩尔质量为(3)相同条件下,体积比为
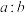 和质量比为
和质量比为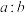 的
的 和
和 的混合气体,其平均摩尔质量分别是
的混合气体,其平均摩尔质量分别是(4)在标准状况下,将

 气体溶于
气体溶于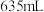 水中,所得盐酸的密度为
水中,所得盐酸的密度为 。试计算:
。试计算:①所得盐酸的质量分数和物质的量浓度分别是
②取这种盐酸
 ,稀释至
,稀释至 ,所得稀盐酸的物质的量浓度
,所得稀盐酸的物质的量浓度③在
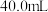

 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生 气体,加入稀盐酸的体积最多不超过
气体,加入稀盐酸的体积最多不超过
您最近一年使用:0次
名校
解题方法
7 . 已知:①H2O ②Cu ③NO ④SiO2 ⑤稀硫酸 ⑥氢氧化钡 ⑦饱和FeCl3溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝。
根据上述提供的物质,回答下列问题:
(1)属于纯净物的是___________ ,属于电解质的是___________ 。(填数字序号)
(2)发生中和反应的离子方程式为H++OH-=H2O,该离子反应对应的化学方程式有___________ 。
(3)实验室制备少量Fe(OH)3胶体发生反应的离子方程式为___________ 。
(4)实验室配制0.5 mol·L-1 245 mL ⑩的溶液,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管、___________ ,需要用托盘天平称取溶质的质量为___________ g,从配制好的溶液中取出100 mL,其中含有的SO 数目为
数目为___________ (设NA为阿伏加德罗常数的值)。
根据上述提供的物质,回答下列问题:
(1)属于纯净物的是
(2)发生中和反应的离子方程式为H++OH-=H2O,该离子反应对应的化学方程式有
(3)实验室制备少量Fe(OH)3胶体发生反应的离子方程式为
(4)实验室配制0.5 mol·L-1 245 mL ⑩的溶液,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管、
 数目为
数目为
您最近一年使用:0次
名校
解题方法
8 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为_______ (保留两位有效数字)
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液(必须用到容量瓶)。下列说法正确的是_______(填序号)。

(3)若实验遇下列情况,则所配溶液的物质的量浓度是:(用“偏低”,“偏高,“不变”回答)
Ⅰ.定容时俯视刻度线_______ ;
Ⅱ.定容时水多用胶头滴管吸出_______ 。
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为_______ mol·L-1,需用浓硫酸的体积为_______ mL。
②写出稀硫酸与“84消毒液”反应的化学方程式_______ 。

(1)该“84消毒液”的物质的量浓度约为
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液(必须用到容量瓶)。下列说法正确的是_______(填序号)。

| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| D.需要称量NaClO固体的质量为143.0g |
Ⅰ.定容时俯视刻度线
Ⅱ.定容时水多用胶头滴管吸出
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为
②写出稀硫酸与“84消毒液”反应的化学方程式
您最近一年使用:0次
2023-04-30更新
|
174次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题
名校
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.50℃, 的 的 溶液中含有 溶液中含有 的数目为 的数目为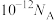 |
B. 的 的 溶液中含 溶液中含 分子的数目为 分子的数目为 |
C. 和 和 于密闭容器中充分反应后,分子总数为 于密闭容器中充分反应后,分子总数为 |
D.浓度均为 的 的 溶液和 溶液和 溶液中, 溶液中, 数目均为 数目均为 |
您最近一年使用:0次
2023-04-28更新
|
779次组卷
|
4卷引用:宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题
解题方法
10 . 设NA是阿伏加德罗常数的值。下列说法正确的是
| A.39gNa2S和Na2O2组成的混合物中,含有阴离子的数目为NA |
| B.将2molNO和lmolO2混合,所得混合气体的分子总数为2NA |
| C.31g白磷含P-P键数为1.5NA |
| D.0.1mol/L的NaOH水溶液中含有Na+数目为0.01NA |
您最近一年使用:0次



