1 . 钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,该过程表示为: ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是A. 的可能结构为 的可能结构为 | B.钠加入液氨中溶液的导电性增强 |
C. 具有强还原性 具有强还原性 | D. 在液氨体系中会产生 在液氨体系中会产生 |
您最近一年使用:0次
名校
2 . 已知: ;
; 。现有常温下由水电离出的
。现有常温下由水电离出的 均为
均为 的4种溶液:①HCl溶液②
的4种溶液:①HCl溶液② 溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
 ;
; 。现有常温下由水电离出的
。现有常温下由水电离出的 均为
均为 的4种溶液:①HCl溶液②
的4种溶液:①HCl溶液② 溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是A.等体积的①、③溶液分别与足量铝粉反应,生成 的量③多 的量③多 |
B.向等体积溶液中分别加水稀释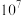 倍后,溶液的pH:④≈③≈②≈① 倍后,溶液的pH:④≈③≈②≈① |
C.四种溶液以体积比 混合后,所得溶液显中性 混合后,所得溶液显中性 |
| D.等体积的四种溶液导电能力顺序:④≈②>①≈③ |
您最近一年使用:0次
3 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。
(1)请完成该离子方程式并配平___________ 。
(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 开不是最佳方法,其原因是
开不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ 填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列:___________ (填序号)反应中 表现出的性质相同。
表现出的性质相同。
A.
B.
C.
(6) 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:___________ 。
____ _____
_____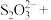 _____
_____ ____
____ ____
____ ______
______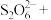 _____
_____
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 开不是最佳方法,其原因是
开不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列: 表现出的性质相同。
表现出的性质相同。A.

B.

C.

(6)
 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:____
 _____
_____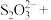 _____
_____ ____
____ ____
____ ______
______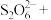 _____
_____
您最近一年使用:0次
名校
4 . 有三种物质A、B、C,其中一种是碱,其余两种是盐。它们均可溶于水,电离只产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是___________ ,X___________ (填“是”或“不是”)电解质。
(2)C在水中的电离方程式为___________ 。鉴别C溶液中阴离子的实验操作方法___________ 。
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:___________ 。
②B溶液与C溶液反应至溶液呈中性:___________ 。
| 阳离子 | Na+、H+、Ba2+ |
| 阴离子 | OH–、CO 、SO 、SO |
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请回答下列问题:
(1)X的名称是
(2)C在水中的电离方程式为
(3)写出以下水溶液中反应的离子方程式。
①A溶液与B溶液反应生成无色气体X:
②B溶液与C溶液反应至溶液呈中性:
您最近一年使用:0次
5 . 一些非水溶剂,会发生类似水的自耦解离: ,
, ,
, ;据此推测下列反应方程式书写错误的是
;据此推测下列反应方程式书写错误的是
 ,
, ,
, ;据此推测下列反应方程式书写错误的是
;据此推测下列反应方程式书写错误的是A. (液态 (液态 中) 中) |
B. (液态 (液态 中) 中) |
C. (液氨中) (液氨中) |
D. |
您最近一年使用:0次
2023-07-15更新
|
406次组卷
|
2卷引用:湖北省恩施州教育联盟022-2023学年高二下学期7月期末考试化学试题
名校
解题方法
6 . 根据题目填写内容
(1)下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是_______ 。
检验②中金属阳离子的实验方法是______________________________ (填实验操作的名称)。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_____________ 。
Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是_____________ 。
(3)酸性条件下,高锰酸钾可与草酸(H2C2O4)溶液发生反应,其反应如下,补上产物,配平化学方程式,并用单线桥法标出电子转移的方向和数目_____________ 。
____KMnO4+____H2C2O4+____H2SO4→____K2SO4+____MnSO4+____CO2+________
(4)①0.5mol C2H6O的质量是____ 克,含____ 个C2H6O分子,含____ mol氢原子,与____ g H2O分子中的氢的原子数目相同。
②在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为____ 。
③有K2SO4和Al2(SO)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1, 的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为____ 。
(1)下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
能导电的是
检验②中金属阳离子的实验方法是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是
(3)酸性条件下,高锰酸钾可与草酸(H2C2O4)溶液发生反应,其反应如下,补上产物,配平化学方程式,并用单线桥法标出电子转移的方向和数目
____KMnO4+____H2C2O4+____H2SO4→____K2SO4+____MnSO4+____CO2+________
(4)①0.5mol C2H6O的质量是
②在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为
③有K2SO4和Al2(SO)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,
 的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
您最近一年使用:0次
名校
7 . 对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
I.现有以下物质:①H2O ②Cu ③BaSO4 ④Fe(OH)3胶体 ⑤CH3CH2OH(酒精) ⑥CO2 ⑦稀硫酸 ⑧NaOH溶液
(1)以上物质中属于混合物的是___________ (填序号,下同)
(2)属于电解质的是___________ ,属于非电解质的是___________ ,属于强电解质的是___________ 。
(3)加入___________ 可使④Fe(OH)3胶体产生聚沉。
(4)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是___________。
(5)有同学认为所有酸碱中和反应均可表示为H+ + OH- = H2O。请举个例子反驳上述观点(用离子方程式表示)___________ 。
(6)K2Cr2O7 +HCl → KCl +CrCl3+Cl2↑+ H2O。请配平该方程式并用双线桥标明电子转移方向和数目:___________ 。
I.现有以下物质:①H2O ②Cu ③BaSO4 ④Fe(OH)3胶体 ⑤CH3CH2OH(酒精) ⑥CO2 ⑦稀硫酸 ⑧NaOH溶液
(1)以上物质中属于混合物的是
(2)属于电解质的是
(3)加入
(4)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是___________。
| A.能全部透过滤纸 | B.有丁达尔效应 |
| C.所得液体为胶体 | D.所得物质一定是悬浊液 |
(6)K2Cr2O7 +HCl → KCl +CrCl3+Cl2↑+ H2O。请配平该方程式并用双线桥标明电子转移方向和数目:
您最近一年使用:0次
名校
解题方法
8 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。
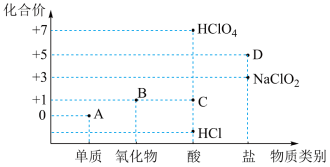
(1)已知D可用于实验室制 ,其阳离子为
,其阳离子为 。A、B、C、D四种物质中,属于电解质的是
。A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)B溶于氢氧化钠溶液,可生成“84”消毒液的有效成分,则B属于_______ (填“酸性”或“碱性”)氧化物。
(3)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则D分解的化学方程式为_______ 。
(4)浓HCl与D可制得单质A,请写出相应的化学方程式并用双线桥法表示电子转移的方向与数目_______ 。
(5) 是一种高效的消毒剂和漂白剂。工业用Mathieson法制备
是一种高效的消毒剂和漂白剂。工业用Mathieson法制备 的流程如下:
的流程如下:
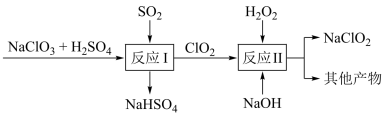
反应I中氧化剂与氧化产物的物质的量之比为_______ ;反应II的离子方程式是_______ 。

(1)已知D可用于实验室制
 ,其阳离子为
,其阳离子为 。A、B、C、D四种物质中,属于电解质的是
。A、B、C、D四种物质中,属于电解质的是(2)B溶于氢氧化钠溶液,可生成“84”消毒液的有效成分,则B属于
(3)D在400℃时分解只生成两种盐,其中一种是无氧酸盐;另一种盐M的阴阳离子个数比为1:1,则D分解的化学方程式为
(4)浓HCl与D可制得单质A,请写出相应的化学方程式并用双线桥法表示电子转移的方向与数目
(5)
 是一种高效的消毒剂和漂白剂。工业用Mathieson法制备
是一种高效的消毒剂和漂白剂。工业用Mathieson法制备 的流程如下:
的流程如下:
反应I中氧化剂与氧化产物的物质的量之比为
您最近一年使用:0次
名校
解题方法
9 . 对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
(1)现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸 ⑧氯水。以上物质中属于混合物的是_______ (填序号,下同),属于电解质的是_______ 。④中逐滴滴加⑦,可观察到的现象是_______ 。
(2)有同学认为所有强酸和强碱中和反应均可表示为H++OH-=H2O。请举出一例反驳上述观点_______ (用离子方程式表示)。
(3)⑧号物质——氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空。(a、b、c、d中重合部分代表物质间反应,且氯水足量)

①d过程中观察到的现象是_______ ,可证明氯水中存在_______ 微粒。
②c过程中的离子方程式_______ ;b过程的离子方程式_______ 。
③氯水久置过程中发生的变化,用化学反应方程式表示为_______ 。
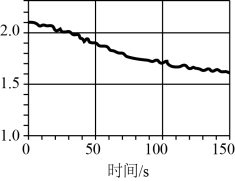
④数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。下图是将传感器插入盛有氯气的广口中测定光照氯水过程所得到的图像,该图像表示的意义是_______ 。
A.氯离子浓度随时间的变化
B.氧气体积分数随时间的变化
C.氯水的 随时间的变化
随时间的变化
D.氯水导电能力随时间的变化
E.氯气的溶解度随时间的变化
(1)现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸 ⑧氯水。以上物质中属于混合物的是
(2)有同学认为所有强酸和强碱中和反应均可表示为H++OH-=H2O。请举出一例反驳上述观点
(3)⑧号物质——氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空。(a、b、c、d中重合部分代表物质间反应,且氯水足量)

①d过程中观察到的现象是
②c过程中的离子方程式
③氯水久置过程中发生的变化,用化学反应方程式表示为
④数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。下图是将传感器插入盛有氯气的广口中测定光照氯水过程所得到的图像,该图像表示的意义是

A.氯离子浓度随时间的变化
B.氧气体积分数随时间的变化
C.氯水的
 随时间的变化
随时间的变化D.氯水导电能力随时间的变化
E.氯气的溶解度随时间的变化
您最近一年使用:0次
2022-12-13更新
|
250次组卷
|
2卷引用:湖北省襄阳市第六中学2023-2024学年高一上学期10月月考化学试题
名校
解题方法
10 . 通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。已知:氨气能与水反应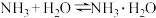 下列判断不正确的是
下列判断不正确的是
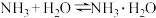 下列判断不正确的是
下列判断不正确的是| A.A、B、E中的一种肯定含有金属元素 | B.A为电解质,B为非电解质 |
| C.A和B中所含元素可以组成盐类物质 | D.能够确定该白色沉淀的化学组成 |
您最近一年使用:0次
2021-10-17更新
|
677次组卷
|
2卷引用:湖北省东南新高考联盟2021-2022学年高一上学期10月联考化学试题



