名校
解题方法
1 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,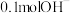 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为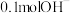 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近一年使用:0次
解题方法
2 . 生活离不开化学,家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①漂白粉;②NaClO;③Cl2;④Na2CO3;⑤小苏打(NaHCO3);⑥生铁;⑦甲烷。回答下列问题:
(1)漂白液的有效成分NaClO在水溶液的电离方程式:___________ 。
(2)厨卫用品的主要成分(括号内的物质):是电解质的有___________ (填序号,下同),是非电解质的有___________ 。
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为___________ g。
(4)实验室制Cl2的化学方程式___________ ,收集到33.6L(折算到标准状态)氯气时该反应总共转移的电子数___________ 。
(1)漂白液的有效成分NaClO在水溶液的电离方程式:
(2)厨卫用品的主要成分(括号内的物质):是电解质的有
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为
(4)实验室制Cl2的化学方程式
您最近一年使用:0次
解题方法
3 . 填空题。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是_______ (填序号,下同);属于混合物的是_______ ;属于电解质的是_______ ;属于非电解质的是_______ 。
(2)3.4克NH3中所含氢原子数目与标准状况下约______ LH2S所含氢原子数目相等。
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为_______ 。
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为_______ 。
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为_______ ;氢原子总数之比为_______ ;体积之比为_______ ;密度之比为_______ 。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是
(2)3.4克NH3中所含氢原子数目与标准状况下约
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为
您最近一年使用:0次
4 . 分类法是进行化学研究的重要方法。不同的标准可以把物质和反应分为不同的类别。回答下列问题:
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是___________ (填序号);属于非电解质的是___________ (填序号);③在水中的电离方程式为___________ 。
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是___________ (填标号)。

A. B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg
(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式___________ 。
②完善下面的化学方程式,并配平___________ 。

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素( )。写出发生反应的离子方程式
)。写出发生反应的离子方程式___________ 。
(4)在20.00ml 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用
 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式②完善下面的化学方程式,并配平

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素(
 )。写出发生反应的离子方程式
)。写出发生反应的离子方程式(4)在20.00ml
 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________A. | B. | C. | D.V |
您最近一年使用:0次
名校
5 . 根据要求,完成下列各题:
(1)把含有 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为___________ 。
(2)某气态氧化物化学式为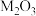 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为___________ 。
(3)标准状况下,把11.2L 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是___________ g。
(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有___________ ,属于非电解质的有___________ ,能导电的有___________ 。(填序号)
(1)把含有
 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为(2)某气态氧化物化学式为
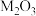 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为(3)标准状况下,把11.2L
 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤
 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
您最近一年使用:0次
2023-12-23更新
|
153次组卷
|
2卷引用:山东省菏泽第一中学2023-2024学年高一上学期期中考试化学试题 (A)
6 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。
(1)请完成该离子方程式并配平___________ 。
(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 开不是最佳方法,其原因是
开不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ 填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列:___________ (填序号)反应中 表现出的性质相同。
表现出的性质相同。
A.
B.
C.
(6) 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:___________ 。
____ _____
_____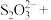 _____
_____ ____
____ ____
____ ______
______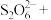 _____
_____
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 开不是最佳方法,其原因是
开不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列: 表现出的性质相同。
表现出的性质相同。A.

B.

C.

(6)
 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:____
 _____
_____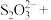 _____
_____ ____
____ ____
____ ______
______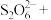 _____
_____
您最近一年使用:0次
7 . 回答下列问题
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是___________ ,属于混合物的是___________ (填编号)
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下, 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为___________ 。
②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为___________ mL。
③相同体积的 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为
①配平该反应:_______

②当有32g硫单质完全反应时,生成氧化产物的物质的量是___________ mol。
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下,
 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入
 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为③相同体积的
 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为

①配平该反应:

②当有32g硫单质完全反应时,生成氧化产物的物质的量是
您最近一年使用:0次
8 . 根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1) 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于NaOH溶液的化学方程式:
溶于NaOH溶液的化学方程式:______ .
(2)现有:①固体KOH ②稀硫酸 ③氦气 ④熔融NaCl ⑤蔗糖 ⑥铜;其中能导电的是______ (填序号,下同);属于电解质的是______ ,属于非电解质的是______ .
(3)写出 在水溶液中的电离方程式
在水溶液中的电离方程式______ .
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物 中含0.6mol
中含0.6mol ,则M的摩尔质量为
,则M的摩尔质量为______ .
(5)标准状况下,与34g的 气体含相同H原子数的
气体含相同H原子数的 的体积为
的体积为______ .
(6)标准状况下,若aL二氧化碳中含有b个氧原子,则阿伏加德罗常数为______ .
(7)实验室使用的浓盐酸的溶质质量分数为36.5%,密度为 ,则该浓盐酸的物质的量浓度为
,则该浓盐酸的物质的量浓度为______ .
(8)一种加碘盐(配料为NaCl和 )中
)中 的含量为
的含量为 ,则每千克该加碘盐中碘的质量为
,则每千克该加碘盐中碘的质量为______ .
(1)
 是普通玻璃的主要成分,与
是普通玻璃的主要成分,与 一样是酸性氧化物,写出
一样是酸性氧化物,写出 溶于NaOH溶液的化学方程式:
溶于NaOH溶液的化学方程式:(2)现有:①固体KOH ②稀硫酸 ③氦气 ④熔融NaCl ⑤蔗糖 ⑥铜;其中能导电的是
(3)写出
 在水溶液中的电离方程式
在水溶液中的电离方程式Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物
 中含0.6mol
中含0.6mol ,则M的摩尔质量为
,则M的摩尔质量为(5)标准状况下,与34g的
 气体含相同H原子数的
气体含相同H原子数的 的体积为
的体积为(6)标准状况下,若aL二氧化碳中含有b个氧原子,则阿伏加德罗常数为
(7)实验室使用的浓盐酸的溶质质量分数为36.5%,密度为
 ,则该浓盐酸的物质的量浓度为
,则该浓盐酸的物质的量浓度为(8)一种加碘盐(配料为NaCl和
 )中
)中 的含量为
的含量为 ,则每千克该加碘盐中碘的质量为
,则每千克该加碘盐中碘的质量为
您最近一年使用:0次
名校
9 . 按要求填写下列空白:
(1) 个
个 的质量为
的质量为___________ g。
(2)标况下, 的摩尔质量为
的摩尔质量为___________ ,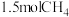 质量为
质量为___________ 。
(3)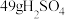 含有
含有___________ 个氢原子,共含有___________ 个原子。
(4)已知标准状况下 的密度为
的密度为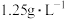 ,X原子最外层有
,X原子最外层有___________ 个电子。
(5)现有下列物质:① 晶体,②石墨,③无水乙醇,④小苏打,⑤熔融
晶体,②石墨,③无水乙醇,④小苏打,⑤熔融 ,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨
,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨ 固体,⑩
固体,⑩ 红褐色胶体其中属于电解质的是:
红褐色胶体其中属于电解质的是:___________ ,能导电的物质是:___________ 。(填序号)
(1)
 个
个 的质量为
的质量为(2)标况下,
 的摩尔质量为
的摩尔质量为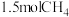 质量为
质量为(3)
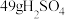 含有
含有(4)已知标准状况下
 的密度为
的密度为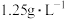 ,X原子最外层有
,X原子最外层有(5)现有下列物质:①
 晶体,②石墨,③无水乙醇,④小苏打,⑤熔融
晶体,②石墨,③无水乙醇,④小苏打,⑤熔融 ,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨
,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨ 固体,⑩
固体,⑩ 红褐色胶体其中属于电解质的是:
红褐色胶体其中属于电解质的是:
您最近一年使用:0次
10 . Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是___________ (填序号,下同)属于电解质的是___________ 。
(3)写出NaClO在水溶液中的电离方程式:___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为___________ 。
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取___________ mL的浓硫酸。
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是___________ 。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是
(3)写出NaClO在水溶液中的电离方程式:
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中
 的物质的量浓度为
的物质的量浓度为(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
您最近一年使用:0次



