解题方法
1 . 常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是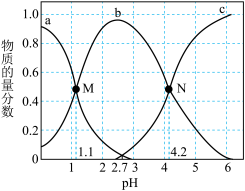
| A.a曲线代表A2-的物质的量分数随pH的变化 |
| B.溶液pH=1时的导电能力强于pH=6时的导电能力 |
| C.H2A第二步电离常数Ka2=10-4.2 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
您最近半年使用:0次
名校
2 . 现有下列10种物质:①铝 ②纯醋酸 ③ ④
④ ⑤
⑤ ⑥红褐色的氢氧化铁胶体 ⑦稀盐酸 ⑧
⑥红褐色的氢氧化铁胶体 ⑦稀盐酸 ⑧ ⑨碳酸钙 ⑩乙醇
⑨碳酸钙 ⑩乙醇
(1)上述物质中能导电的是_________ ,属于电解质的有_____________ (填序号)。
(2)向⑥中逐渐滴加④的溶液,看到的现象是_______________________ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为 ,则该反应的化学方程式为
,则该反应的化学方程式为______________________ 。
(4)⑨和⑦混合反应离子方程式为_________ 。
(5)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率( )随新物质加入体积(V)的变化曲线如图所示。分别与图A、图B曲线变化趋势对应一致的是
)随新物质加入体积(V)的变化曲线如图所示。分别与图A、图B曲线变化趋势对应一致的是_____ (填序号)。
②向饱和石灰水中不断通入
③向硝酸溶液中逐滴加入等浓度的氢氧化钾溶液至恰好完全反应
 ④
④ ⑤
⑤ ⑥红褐色的氢氧化铁胶体 ⑦稀盐酸 ⑧
⑥红褐色的氢氧化铁胶体 ⑦稀盐酸 ⑧ ⑨碳酸钙 ⑩乙醇
⑨碳酸钙 ⑩乙醇(1)上述物质中能导电的是
(2)向⑥中逐渐滴加④的溶液,看到的现象是
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为
 ,则该反应的化学方程式为
,则该反应的化学方程式为(4)⑨和⑦混合反应离子方程式为
(5)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率(
 )随新物质加入体积(V)的变化曲线如图所示。分别与图A、图B曲线变化趋势对应一致的是
)随新物质加入体积(V)的变化曲线如图所示。分别与图A、图B曲线变化趋势对应一致的是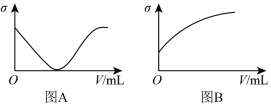
②向饱和石灰水中不断通入

③向硝酸溶液中逐滴加入等浓度的氢氧化钾溶液至恰好完全反应
您最近半年使用:0次
名校
解题方法
3 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,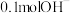 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为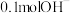 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近半年使用:0次
名校
解题方法
4 . 下列说法正确的是
| A.硫酸的导电能力比盐酸溶液强 |
| B.FeO常用作油漆涂料的颜料 |
C. 、 、 均不溶于水,所以 均不溶于水,所以 、 、 不是电解质 不是电解质 |
| D.氨气溶于水能导电,但氨气不是电解质 |
您最近半年使用:0次
解题方法
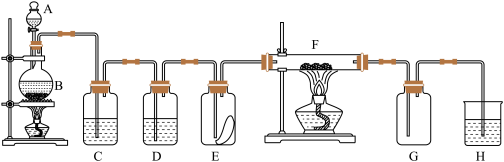
5 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。___________ 。
(2)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(3)E中红色布条是否褪色?___________ (填“是”或“否”),F中的反应产物为___________ 。
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式___________ ,___________ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)___________ 。
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)
您最近半年使用:0次
解题方法
6 . 回答下列问题。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)___________ ;
ⅱ.属于电解质的是___________ ;
ⅲ.属于非电解质的是___________ ;
ⅳ.既不是电解质又不是非电解质的是___________ 。
(2)ⅰ.配平下列离子方程式:___________ 。___________ 。
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中___________ 元素被氧化,氧化剂与氧化产物的个数比为___________ 。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)
ⅱ.属于电解质的是
ⅲ.属于非电解质的是
ⅳ.既不是电解质又不是非电解质的是
(2)ⅰ.配平下列离子方程式:
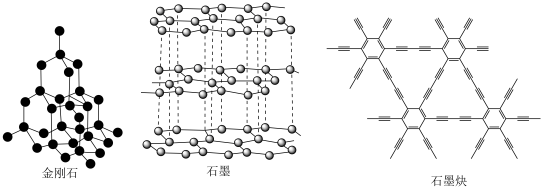
______MnO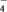 +_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
+_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中
您最近半年使用:0次
解题方法
7 . 下列关于纯净物、混合物、电解质和非电解质的正确组合是
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 浓盐酸 | 天然气 | 硫酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 三氧化硫 |
| C | 胆矾 | 石灰水 | 苛性钾 | 碳酸钙 |
| D | 冰水混合物 | 铝合金 | 氯化钠 | 氢气 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
| A.三种物质均是碳单质 | B.三种物质的化学性质相同 |
| C.三种物质的晶体类型相同 | D.三种物质均能导电 |
您最近半年使用:0次
9 . 氯化钠(NaCl)是一种常见的电解质,下列关于氯化钠的电离的说法正确的是
| A.氯化钠的电离需要通电 |
| B.氯化钠是一种离子化合物 |
| C.家用食盐是一种纯净物 |
| D.高温条件下氯化钠固体会熔化生成钠原子与氯原子 |
您最近半年使用:0次
10 . 回答下列问题。
(1)双氧水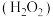 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式:___________ 。鉴于 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:___________ 。
(2)如图是向 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。___________  。
。
②X的值为___________ 。
(3)已知 的高碘酸
的高碘酸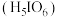 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸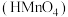 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是___________ (填“强酸”或“弱酸”),理由是___________ 。
(4) 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则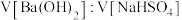 为
为___________ 。
(1)双氧水
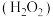 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式: 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:(2)如图是向
 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。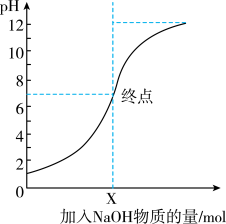
 。
。②X的值为
(3)已知
 的高碘酸
的高碘酸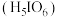 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸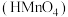 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是(4)
 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则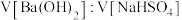 为
为
您最近半年使用:0次



