解题方法
1 . 完成下列问题
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦ 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是___________ (填序号,下同)。
(2)上述状态下物质中不能导电,但属于电解质的是___________
(3)上述物质中属于非电解质的是___________ 。
Ⅱ.储氢纳米碳管研究成功体现了科技的进步,但用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式为: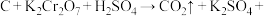
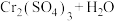 (未配平)。回答下列问题。
(未配平)。回答下列问题。
(4)该反应中,还原剂是___________ (填化学式),被还原的元素是___________ (填元素符号)。
(5) 在该反应中表现出___________(填字母)。
在该反应中表现出___________(填字母)。
(6)配平上述方程式:___________ 。每生成2分子 ,该反应转移
,该反应转移___________ 个电子。
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦
 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是
(2)上述状态下物质中不能导电,但属于电解质的是
(3)上述物质中属于非电解质的是
Ⅱ.储氢纳米碳管研究成功体现了科技的进步,但用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应的化学方程式为:
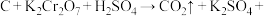
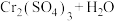 (未配平)。回答下列问题。
(未配平)。回答下列问题。(4)该反应中,还原剂是
(5)
 在该反应中表现出___________(填字母)。
在该反应中表现出___________(填字母)。| A.只有酸性 | B.只有氧化性 | C.酸性和氧化性 | D.酸性和还原性 |
 ,该反应转移
,该反应转移
您最近一年使用:0次
解题方法
2 . 铜及其化合物在生产、生活中具有广泛用途。根据所学知识回答下列问题:
(1)用特殊方法把块状铜加工成直径为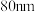 的超细粉末粒子。这种粒子直径处于
的超细粉末粒子。这种粒子直径处于___________ (填标号)分散系中分散质的粒子直径范围内。
a.溶液 b.浊液 c.胶体 d.乳浊液
(2)硫酸铜水溶液具有杀菌作用:
①无水硫酸铜粉末的颜色为___________ 。
② 的俗称为
的俗称为___________ 。
③硫酸铜溶液能导电,则该溶液___________ (填“是”或“不是”)电解质,理由为___________ 。
(3)铜与浓硫酸在加热的条件下发生反应 ;
;
①该反应中 (浓)体现
(浓)体现___________ (填标号)。
a.氧化性 b.还原性 c.酸性
②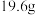 浓硫酸与足量
浓硫酸与足量 发生上述反应,
发生上述反应,___________ (填“能”或“不能”)得到 (标准状况下)
(标准状况下) ,理由为
,理由为___________ (若答能,此问可不填)。
(1)用特殊方法把块状铜加工成直径为
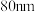 的超细粉末粒子。这种粒子直径处于
的超细粉末粒子。这种粒子直径处于a.溶液 b.浊液 c.胶体 d.乳浊液
(2)硫酸铜水溶液具有杀菌作用:
①无水硫酸铜粉末的颜色为
②
 的俗称为
的俗称为③硫酸铜溶液能导电,则该溶液
(3)铜与浓硫酸在加热的条件下发生反应
 ;
;①该反应中
 (浓)体现
(浓)体现a.氧化性 b.还原性 c.酸性
②
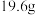 浓硫酸与足量
浓硫酸与足量 发生上述反应,
发生上述反应, (标准状况下)
(标准状况下) ,理由为
,理由为
您最近一年使用:0次
名校
3 . 现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤蔗糖;⑥熔融的NaHSO4;⑦氯化氢。请回答下列问题:(填序号)
(1)以上物质能导电的是__________________ ,属于电解质的是______________ ,属于非电解质的是__________ 。
(2)NaHSO4溶于水时的电离方程式为_______________________________ 。
(3)物质⑦具有________________ (填写“氧化性”“还原性”或者“氧化性和还原性”),在反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是
MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是_____________ (填序号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(4)物质④在氧化还原反应中应该只能表现__________ (填“氧化性”或“还原性”)。
(1)以上物质能导电的是
(2)NaHSO4溶于水时的电离方程式为
(3)物质⑦具有
 MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是
MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(4)物质④在氧化还原反应中应该只能表现
您最近一年使用:0次
4 . 用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。已知:Cl2+H2O=HCl+HClO;2Na+2H2O=2NaOH+H2↑;3NO2+H2O=2HNO3+NO。请根据你所学的知识,按要求填空:
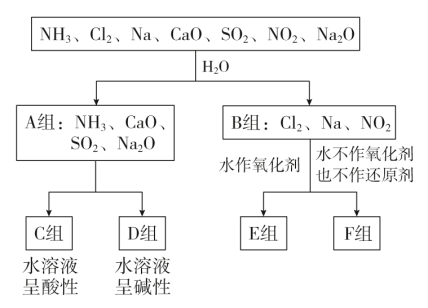
(1)C组中有哪些物质_______ ;F组物质中除了Cl2外还有_______ (填物质名称,下同)。
(2)A组中属于电解质的是_______ ,B组中既不是电解质也不是非电解质的是_______ (填物质名称,下同)。
(3)有反应①2H2O+Cl2+SO2=H2SO4+2HCl,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,针对上述两个反应回答下列问题:
①36g的水的物质的量是_______ , 的摩尔质量是
的摩尔质量是_______ 。
②反应②中浓盐酸表现出的性质是_______ (填字母)。
a.还原性 b.酸性 c.氧化性

(1)C组中有哪些物质
(2)A组中属于电解质的是
(3)有反应①2H2O+Cl2+SO2=H2SO4+2HCl,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,针对上述两个反应回答下列问题:
①36g的水的物质的量是
 的摩尔质量是
的摩尔质量是②反应②中浓盐酸表现出的性质是
a.还原性 b.酸性 c.氧化性
您最近一年使用:0次
名校
5 . 现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤ 固体;⑥蔗糖;⑦浓盐酸;⑧熔融的
固体;⑥蔗糖;⑦浓盐酸;⑧熔融的 ;⑨酒精溶液;⑩
;⑨酒精溶液;⑩ 溶液
溶液
请回答下列问题(填序号)
(1)以上物质能导电的是___________ 。
(2)以上物质属于电解质的是___________ 。
(3)以上物质属于非电解质的是___________ 。
(4)物质④铜在氧化还原反应中应该只能表现___________ (填“氧化性”和“还原性”)。实验室常用高锰酸钾与⑦反应制备 ,请你配平其化学方程式
,请你配平其化学方程式___________ 。
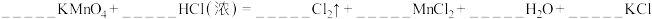
在此反应中,浓盐酸表现的化学性质是___________ 。
(5)向⑩ 溶液中滴加
溶液中滴加 溶液至中性,写出该反应的离子方程式
溶液至中性,写出该反应的离子方程式___________ 。
 固体;⑥蔗糖;⑦浓盐酸;⑧熔融的
固体;⑥蔗糖;⑦浓盐酸;⑧熔融的 ;⑨酒精溶液;⑩
;⑨酒精溶液;⑩ 溶液
溶液请回答下列问题(填序号)
(1)以上物质能导电的是
(2)以上物质属于电解质的是
(3)以上物质属于非电解质的是
(4)物质④铜在氧化还原反应中应该只能表现
 ,请你配平其化学方程式
,请你配平其化学方程式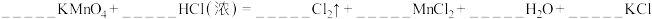
在此反应中,浓盐酸表现的化学性质是
(5)向⑩
 溶液中滴加
溶液中滴加 溶液至中性,写出该反应的离子方程式
溶液至中性,写出该反应的离子方程式
您最近一年使用:0次
6 . (1)在________ 里或________ 状态下能够导电的化合物叫做电解质。电解质溶液之所以能够导电,是由于电解质在溶液中发生了________ ,产生了能够自由移动的离子。
(2)维生素C又称抗坏血酸,在人体中有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有________ (填“氧化性”或“还原性”)。
(2)维生素C又称抗坏血酸,在人体中有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
您最近一年使用:0次
名校
解题方法
7 . (1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________ (填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____ 元酸(填“一”、“二”或“三”)。
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目______ 。
____Fe(OH)3+____ClO-+____OH-=__FeO +___Cl-+______
+___Cl-+______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________ ;当有2mol H3PO4生成,转移的电子数目为____ e-
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式,并用双线桥法标出电子转移方向及数目
____Fe(OH)3+____ClO-+____OH-=__FeO
 +___Cl-+______
+___Cl-+______(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次
名校
8 . 完成下列各小题:
(1)今有五种物质:①铜线 ②熔化的 NaCl ③NaCl 晶体 ④氨气 ⑤液态氯化氢 其中能导电的物质是______ ;属于电解质的是______ ;属于非电解质的是____________ 。
(2)科学家发现,食用虾类等水生甲壳类动物的同时服用维生素 C 容易中毒。这是因为对人体无害的+5 价砷类化合物在维生素 C 的作用下,能够转化为有毒的+3 价的含砷化合物。 通过以上信息填空:
①维生素 C 具有____ (填“氧化性”或“还原性”)。
②上述过程中+5 价砷元素发生______ 反应(填“氧化”或“还原”);3 mol +5 价砷完全转化 为+3 价砷,共转移 _____ 个电子。
(1)今有五种物质:①铜线 ②熔化的 NaCl ③NaCl 晶体 ④氨气 ⑤液态氯化氢 其中能导电的物质是
(2)科学家发现,食用虾类等水生甲壳类动物的同时服用维生素 C 容易中毒。这是因为对人体无害的+5 价砷类化合物在维生素 C 的作用下,能够转化为有毒的+3 价的含砷化合物。 通过以上信息填空:
①维生素 C 具有
②上述过程中+5 价砷元素发生
您最近一年使用:0次
9 . 现有下列物质:①Fe2(SO4)3溶液 ②酒精 ③二氧化硫 ④铜 ⑤过氧化钠 ⑥FeSO4溶液 ⑦CuO ⑧漂白粉,回答下列问题:
(1)在表格空白处填写符合条件物质的序号
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:_______ (用离子方程式表示)。
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为_________ 。
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=______ 。
(5)设计实验证明某溶液含有①、⑥中的两种阳离子_________ 。
(1)在表格空白处填写符合条件物质的序号
| 条件 | 序号 |
| 能导电 | |
| 属于碱性氧化物 | |
| 属于电解质 |
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=
(5)设计实验证明某溶液含有①、⑥中的两种阳离子
您最近一年使用:0次
名校
10 . 化学与人类生活密切相关。现有以下物质:
A. NaHCO3 B. Fe(OH)3 胶体 C. 冰醋酸(固态醋酸) D. 葡萄糖(C6H12O6) E.明矾 F. ClO2 G. Cu H.浓硫酸。
请回答下列问题:
(1)①以上物质中属于电解质的是___________ ; 属于非电解质的是___________ 。 (填字母序号)
②A在水溶液中的电离方程式为___________ 。
(2)葡萄糖注射液标签上的部分内容如图所示:
该注射液中葡萄糖的物质的量浓度为___________ mol/L。(保留两位小数)
(3)实验室用浓硫酸配制500mL lmol/L的H2SO4溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、___________ 、___________ 。 定容时仰视刻度线会导致溶液浓度___________ (填 “偏高”“偏低”或“无影响”)。
(4)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是________
A. NaHCO3 B. Fe(OH)3 胶体 C. 冰醋酸(固态醋酸) D. 葡萄糖(C6H12O6) E.明矾 F. ClO2 G. Cu H.浓硫酸。
请回答下列问题:
(1)①以上物质中属于电解质的是
②A在水溶液中的电离方程式为
(2)葡萄糖注射液标签上的部分内容如图所示:
| 5%葡萄糖注射液 [性状]本品为无色透明溶液。甜味。 [规格] 1000mL: 50g |
(3)实验室用浓硫酸配制500mL lmol/L的H2SO4溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、
(4)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是________
| A.在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性) |
| B.浓硫酸与铜在加热条件下反应生成SO2(酸性和强氧化性) |
| C.蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性) |
| D.浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性) |
您最近一年使用:0次



