1 . 二氧化硫是形成酸雨的“罪魁祸首”,为了保护环境,应减少SO2在大气中的排放。请回答下列问题:
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?_____ 。
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:_____ 。
②NaHSO3:_____ 。
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?_____ 。
②O2是电解质还是非电解质?_____ 。
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++ ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?_____ 。
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:
②NaHSO3:
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?
②O2是电解质还是非电解质?
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++
 ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?
您最近一年使用:0次
名校
2 . 有下列7种物质:
① ②NH4Cl ③
②NH4Cl ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
请回答下列问题:
(1)属于电解质的有_______ (填序号),②物质的电子式为_______ 。
(2)准确配制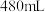 一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、_______ 。
(3)①溶液中加入少量的④反应的离子方程式为_______ 。
(4)将足量的⑧通入BaCl2溶液中,下列说法正确的是_______ 。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入Cl2或NH3,则溶液中均会出现白色沉淀
(5)用含⑧的烟气处理含Cr2O (被还原为Cr3+)的酸性废水时,所发生的离子反应为:
(被还原为Cr3+)的酸性废水时,所发生的离子反应为:_______ 。
(6)关于以上7种物质的说法不正确的有_______。
①
 ②NH4Cl ③
②NH4Cl ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
请回答下列问题:
(1)属于电解质的有
(2)准确配制
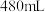 一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、(3)①溶液中加入少量的④反应的离子方程式为
(4)将足量的⑧通入BaCl2溶液中,下列说法正确的是
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入Cl2或NH3,则溶液中均会出现白色沉淀
(5)用含⑧的烟气处理含Cr2O
 (被还原为Cr3+)的酸性废水时,所发生的离子反应为:
(被还原为Cr3+)的酸性废水时,所发生的离子反应为:(6)关于以上7种物质的说法不正确的有_______。
| A.加碘食盐中的“碘”指的是⑥ | B.液态③可做制冷剂 |
| C.⑤和⑧都有漂白性 | D.⑦性质稳定,在自然界中以游离态存在 |
您最近一年使用:0次
解题方法
3 . 某兴趣小组同学在测定溶液的导电性实验时,采用如图所示的串联装置,闭合开关时,发现灯泡不亮。
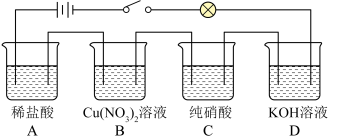
(1)上述四个烧杯中的溶质的电解质类型分别为________________________ 。
(2)上述四个烧杯中________ (填字母)烧杯中的物质发生了电离。
(3)小灯泡不亮的原因是什么______________ ?怎样才能使灯泡亮起来______________ ?
(4)若经过操作灯泡亮起来后,各烧杯等体积溶液中溶质的粒子数目相等,则哪个烧杯的溶液导电能力最强______________ ?

(1)上述四个烧杯中的溶质的电解质类型分别为
(2)上述四个烧杯中
(3)小灯泡不亮的原因是什么
(4)若经过操作灯泡亮起来后,各烧杯等体积溶液中溶质的粒子数目相等,则哪个烧杯的溶液导电能力最强
您最近一年使用:0次
解题方法
4 . 现有以下八种物质:
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液
⑤熔融KNO3 ⑥NaHSO4溶液 ⑦CaCO3固体 ⑧酒精(C2H5OH)
(1)以上物质中能导电的是__________________________ (填写编号,下同)
(2)属于电解质的是__________________
(3)属于非电解质的是_______________
(4)写出下列反应的离子方程式:
③与④反应___________________________________________________
③与⑦反应____________________
(5)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中缓慢通入②至过量,溶液的导电能力的变化为_____________
A.先慢慢增强后又逐渐减弱
B.不变
C.先慢慢减弱后又逐渐增强
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液
⑤熔融KNO3 ⑥NaHSO4溶液 ⑦CaCO3固体 ⑧酒精(C2H5OH)
(1)以上物质中能导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)写出下列反应的离子方程式:
③与④反应
③与⑦反应
(5)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中缓慢通入②至过量,溶液的导电能力的变化为
A.先慢慢增强后又逐渐减弱
B.不变
C.先慢慢减弱后又逐渐增强
您最近一年使用:0次
解题方法
5 . 下列物质:① 晶体②稀盐酸③
晶体②稀盐酸③ 固体④熔融
固体④熔融 ⑤酒精⑥铜⑦
⑤酒精⑥铜⑦ ⑧牛奶⑨液态
⑧牛奶⑨液态 ⑩
⑩ 溶液
溶液
(1)属于分散系的是_______ ;(填序号,下同)
(2)上述状态下能导电的是_______
(3)属于电解质的是_______ ;
(4)属于非电解质的是_______ 。
 晶体②稀盐酸③
晶体②稀盐酸③ 固体④熔融
固体④熔融 ⑤酒精⑥铜⑦
⑤酒精⑥铜⑦ ⑧牛奶⑨液态
⑧牛奶⑨液态 ⑩
⑩ 溶液
溶液(1)属于分散系的是
(2)上述状态下能导电的是
(3)属于电解质的是
(4)属于非电解质的是
您最近一年使用:0次
2023高一上·全国·专题练习
6 . 常见的可拆分物质有:
(1)强酸:___________ 。
(2)强碱:___________ 。
(3)可溶性盐:___________ 。
(4)浓盐酸、浓硝酸在离子方程式中___________ ,浓硫酸___________ 。
(1)强酸:
(2)强碱:
(3)可溶性盐:
(4)浓盐酸、浓硝酸在离子方程式中
您最近一年使用:0次
2023高二上·全国·专题练习
解题方法
7 . 非电解质:在水溶液中和_______ 均以分子形式存在,因而不能导电的化合物。
您最近一年使用:0次
解题方法
8 . 电解质和非电解质
(1)电解质:在水溶液中或熔融状态下能___________ 的___________ 。电解质在水溶液或熔融状态下能产生___________ 的离子。
(2)非电解质:在水溶液中和熔融状态下都___________ 的___________ 。
(1)电解质:在水溶液中或熔融状态下能
(2)非电解质:在水溶液中和熔融状态下都
您最近一年使用:0次
2023高一上·全国·专题练习
解题方法
9 . 几组概念
(1)电解质与非电解质
①定义:在___________ 下能够导电的化合物叫电解质。
②实质:___________ 。
③物质类别:___________ 。
(2)非电解质
①定义:在___________ 下均不导电的化合物叫非电解质。
②实质:___________ 。
③物质类别:___________ 。
(3)强、弱电解质
强电解质与弱电解质比较
(1)电解质与非电解质
①定义:在
②实质:
③物质类别:
(2)非电解质
①定义:在
②实质:
③物质类别:
(3)强、弱电解质
强电解质与弱电解质比较
| 强电解质 | 弱电解质 | |
| 定义 | ||
| 溶液中存在微粒种类 | ||
| 举例 | ①强酸: ②强碱: ③绝大部分盐: | ①弱酸: ②弱碱: ③水 |
您最近一年使用:0次



