名校
解题方法
1 . 数字化实验是利用传感器和信息处理终端进行试验数据的采集与分析。某兴趣小组利用数字化实验测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如下图所示。下列说法正确的是
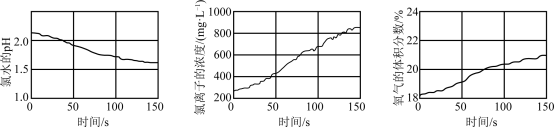

| A.氯水能导电,氯水是电解质 |
| B.氯水光照过程中发生了氧化还原反应 |
| C.新制氯水中没有Cl-,光照过程中生成Cl- |
D.上述实验证明: |
您最近一年使用:0次
2022-01-22更新
|
211次组卷
|
2卷引用:广东省广州市天河区2021-2022学年高一上学期期末考试化学试题
名校
2 . 下列实验能够达到相应目的的是
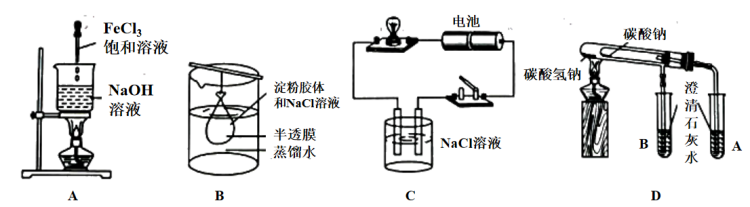

A.图A是将 饱和溶液滴入热 饱和溶液滴入热 溶液中制备氢氧化铁胶体 溶液中制备氢氧化铁胶体 |
| B.图B是一段时间后,若往烧杯中液体滴加硝酸酸化硝酸银有白色沉淀,则半透膜破损 |
| C.图C是可用于证明氯化钠是电解质 |
| D.图D是可用于比较碳酸钠和碳酸氢钠的热稳定性 |
您最近一年使用:0次
2021-11-24更新
|
388次组卷
|
8卷引用:河南省信阳市2021-2022学年高一上学期期中考试化学试题
3 . 按要求填空:
(1)实验室常用洁净的烧杯取少量蒸馏水, 用酒精灯加热至沸腾, 向烧杯中逐滴加入某种物质 M 的水溶液,继续煮沸可制得一种红褐色胶体。
①物质 M 的化学式为___________ 。
②证明有红褐色胶体生成的实验操作及现象是___________ 。
(2)现有 7 种物质:①液态氯化氢②乙醇③熔融的 KNO3 ④铜线⑤NaCl 晶体 ⑥小苏打溶液⑦氨水。
属于电解质的是___________ , 属于非电解质的是___________ 。
(3)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了实验,部分操作如下:
①向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是___________ 。
②氯水经光照后,颜色逐渐消失,并放出的气体是___________ ,溶液的酸性___________ (填“增强”、“不 变”或“减弱”)。
(1)实验室常用洁净的烧杯取少量蒸馏水, 用酒精灯加热至沸腾, 向烧杯中逐滴加入某种物质 M 的水溶液,继续煮沸可制得一种红褐色胶体。
①物质 M 的化学式为
②证明有红褐色胶体生成的实验操作及现象是
(2)现有 7 种物质:①液态氯化氢②乙醇③熔融的 KNO3 ④铜线⑤NaCl 晶体 ⑥小苏打溶液⑦氨水。
属于电解质的是
(3)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了实验,部分操作如下:
①向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是
②氯水经光照后,颜色逐渐消失,并放出的气体是
您最近一年使用:0次
名校
4 . 下列实验不能达到实验目的的是
| A.证明氯化钠是电解质 | B.证明酸性高锰酸钾有氧化性 | C.从食盐水中获取氯化钠 | D.制备氢氧化铁胶体 |
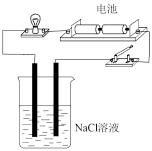 | 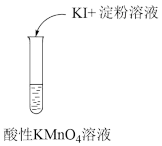 | 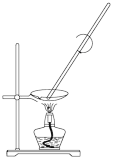 | 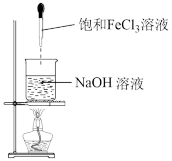 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-07更新
|
290次组卷
|
2卷引用:北京市一零一中2021-2022学年高一上学期期中考试化学试题
名校
解题方法
5 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。现有下列物质:① ②过氧化钠固体 ③熔融的
②过氧化钠固体 ③熔融的 ④
④ ⑤碘水 ⑥
⑤碘水 ⑥ ⑦冰醋酸 ⑧氨水 ⑨小苏打固体 ⑩硫酸亚铁溶液
⑦冰醋酸 ⑧氨水 ⑨小苏打固体 ⑩硫酸亚铁溶液
(1)上述物质可以导电的是___ ,属于电解质的是____ ,属于非电解质的是___ (填序号)
(2)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打与氢氧化钠溶液反应的离子方程式:___________ 。
(3)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:___________ 。
(4)有同学提出疑问:“ 在有水存在时,才能与过氧化钠反应吗?”,设计以下实验加以验证,请回答下列问题。
在有水存在时,才能与过氧化钠反应吗?”,设计以下实验加以验证,请回答下列问题。 后,在通入
后,在通入 之前,应事先将活塞(
之前,应事先将活塞( 、
、 )关闭好,目的是
)关闭好,目的是___________ 。
②试管I内的试剂X是_______ 时,打开活塞 、
、 ,加热试管III约5分钟后,将带火星的木条插入试管II的液面上,可观察到的现象
,加热试管III约5分钟后,将带火星的木条插入试管II的液面上,可观察到的现象________ ,可以证明 与干燥的
与干燥的 不能反应。
不能反应。
③试管I内试剂为 饱和水溶液时,其他操作同②,可观察到
饱和水溶液时,其他操作同②,可观察到_______ 的现象,则可以证明 与潮湿的
与潮湿的 能反应且放出
能反应且放出 。
。
 ②过氧化钠固体 ③熔融的
②过氧化钠固体 ③熔融的 ④
④ ⑤碘水 ⑥
⑤碘水 ⑥ ⑦冰醋酸 ⑧氨水 ⑨小苏打固体 ⑩硫酸亚铁溶液
⑦冰醋酸 ⑧氨水 ⑨小苏打固体 ⑩硫酸亚铁溶液(1)上述物质可以导电的是
(2)小苏打常用于糕点制作,还可治疗胃酸过多等,有多种用途。请写出小苏打与氢氧化钠溶液反应的离子方程式:
(3)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,请你写出过氧化钠与二氧化碳反应的化学方程式:
(4)有同学提出疑问:“
 在有水存在时,才能与过氧化钠反应吗?”,设计以下实验加以验证,请回答下列问题。
在有水存在时,才能与过氧化钠反应吗?”,设计以下实验加以验证,请回答下列问题。
 后,在通入
后,在通入 之前,应事先将活塞(
之前,应事先将活塞( 、
、 )关闭好,目的是
)关闭好,目的是②试管I内的试剂X是
 、
、 ,加热试管III约5分钟后,将带火星的木条插入试管II的液面上,可观察到的现象
,加热试管III约5分钟后,将带火星的木条插入试管II的液面上,可观察到的现象 与干燥的
与干燥的 不能反应。
不能反应。③试管I内试剂为
 饱和水溶液时,其他操作同②,可观察到
饱和水溶液时,其他操作同②,可观察到 与潮湿的
与潮湿的 能反应且放出
能反应且放出 。
。
您最近一年使用:0次
2021-12-18更新
|
196次组卷
|
2卷引用:山东省聊城第一中学2021-2022学年高一上学期期中考试化学试题
名校
6 . 请回答下列问题:
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是___________ 。属于强电解质的是___________ 。属于非电解质的是___________ 。
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体。
(3)NaHSO4 固体溶于水的电离方程式为___________ ;
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为___________ 。
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C___________ ,D ___________ ;
A与C反应的离子方程式___________ ;
A溶液中阴离子的检验方法___________ 。
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用
(3)NaHSO4 固体溶于水的电离方程式为
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO
 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C
A与C反应的离子方程式
A溶液中阴离子的检验方法
您最近一年使用:0次
7 . 常见消毒剂有:①医用酒精;②“84”消毒液(主要成分是NaClO);③漂白粉;④二氧化氯;⑤O3;⑥高铁酸钠。
(1)上述物质中,消毒原理和其他不同的是___________ (填序号,下同)。
(2)上述物质中,其有效成分属于电解质的是___________ 。
(3)臭氧和氧气互为___________ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于___________ 。(填“氧化还原反应”或“非氧化还原反应”)。
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是___________ (用离子方程式表示)。
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:___________ 。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O
(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于___________ 盐,其中Fe的化合价是___________ 。其净水过程中所发生的化学反应主要为:4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH,证明有Fe(OH)3胶体生成的实验操作:___________ 。
(1)上述物质中,消毒原理和其他不同的是
(2)上述物质中,其有效成分属于电解质的是
(3)臭氧和氧气互为
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于
您最近一年使用:0次
解题方法
8 . 回答下列问题:
(1)现有下列物质:①小苏打② 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是_______ (填序号,下同);属于酸性氧化物的是_______ 。属于电解质的是_______ 。溶于水后形成的水溶液不能导电的是_______ 。
(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰( )。
)。
①生石灰属于哪类氧化物:_______ 。
②生石灰可作干燥剂的理由是(用化学方程式表示)_______ 。
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是_______ (填序号)。
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是_______ 。
③证明有氢氧化铁胶体生成的实验操作是_______ 。
(1)现有下列物质:①小苏打②
 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰(
 )。
)。①生石灰属于哪类氧化物:
②生石灰可作干燥剂的理由是(用化学方程式表示)
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是
③证明有氢氧化铁胶体生成的实验操作是
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题
(1)下图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号

①相连的两种物质都是非电解质的是___________ (填分类标准代号),都是氧化物的是___________ 。(填分类标准代号)
②图中相连的两种物质能够相互反应的是___________ (填分类标准代号),所属基本反应类型的___________ 反应。
③向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为___________ 。
④证明该分散系生成的方法是___________ 。向该胶体中逐滴加入稀盐酸,会发生一系列变化:a.先产生红褐色沉淀。利用胶体的___________ 性质;b.随后红褐色沉淀溶解。
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与澄清石灰水反应的离子方程为___________ 。
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,NaHCO3+ HCl = NaCl +H2O+CO2↑及NaHCO3+NaOH = Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的离子方程式为___________ 、___________ 。
(1)下图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号

①相连的两种物质都是非电解质的是
②图中相连的两种物质能够相互反应的是
③向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为
④证明该分散系生成的方法是
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与澄清石灰水反应的离子方程为
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,NaHCO3+ HCl = NaCl +H2O+CO2↑及NaHCO3+NaOH = Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的离子方程式为
您最近一年使用:0次
10 . 根据所学知识,回答下列问题:
(1)下列物质中,属于电解质的是___________ (填序号,下同),可以导电的是___________ 。
① 固体②
固体② ③酒精④
③酒精④ 溶液⑤碳酸钠溶液⑥
溶液⑤碳酸钠溶液⑥ 溶液⑦
溶液⑦ ⑧
⑧ 固体
固体
(2)向上述⑤中逐滴加入⑥,写出发生反应的离子方程式:___________ 。
(3)某实验小组在对(1)中某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液中可能含有 、
、 、
、 、
、 、
、 、
、 ,取该澄清溶液进行以下实验:
,取该澄清溶液进行以下实验:
①用pH试纸检验。结果表明溶液呈强酸性,可以排除___________ 的存在。(填离子符号,下同)
②取出部分溶液逐滴加入NaOH溶液。使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明___________ 的存在。
③取部分②中碱性溶液滴加 溶液,有白色沉淀生成,证明
溶液,有白色沉淀生成,证明___________ 的存在,同时可以排除___________ 的存在。
④综上实验,该澄清溶液中肯定存在的离子是___________ 。
(1)下列物质中,属于电解质的是
①
 固体②
固体② ③酒精④
③酒精④ 溶液⑤碳酸钠溶液⑥
溶液⑤碳酸钠溶液⑥ 溶液⑦
溶液⑦ ⑧
⑧ 固体
固体(2)向上述⑤中逐滴加入⑥,写出发生反应的离子方程式:
(3)某实验小组在对(1)中某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液中可能含有
 、
、 、
、 、
、 、
、 、
、 ,取该澄清溶液进行以下实验:
,取该澄清溶液进行以下实验:①用pH试纸检验。结果表明溶液呈强酸性,可以排除
②取出部分溶液逐滴加入NaOH溶液。使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明
③取部分②中碱性溶液滴加
 溶液,有白色沉淀生成,证明
溶液,有白色沉淀生成,证明④综上实验,该澄清溶液中肯定存在的离子是
您最近一年使用:0次



