名校
1 . 现有下列物质:① 晶体 ②铜丝 ③
晶体 ②铜丝 ③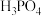 ④二氧化硫 ⑤
④二氧化硫 ⑤ 固体 ⑥
固体 ⑥ 固体 ⑦水 ⑧稀硝酸 ⑨蔗糖
固体 ⑦水 ⑧稀硝酸 ⑨蔗糖
(1)按物质的分类方法填写表格的空白处:(填编号)
(2)某学习小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。
溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。
[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示。

[实验过程与记录]
(3)书写下列两种情况的离子方程式
①向 溶液中逐滴加入
溶液中逐滴加入 溶液至恰好完全沉淀
溶液至恰好完全沉淀_______ 。
②向 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性_______ ,后续继续滴加 溶液
溶液_______ 。
(4)写出 溶液中
溶液中 的电离方程式
的电离方程式_______ 。
 晶体 ②铜丝 ③
晶体 ②铜丝 ③ ④二氧化硫 ⑤
④二氧化硫 ⑤ 固体 ⑥
固体 ⑥ 固体 ⑦水 ⑧稀硝酸 ⑨蔗糖
固体 ⑦水 ⑧稀硝酸 ⑨蔗糖(1)按物质的分类方法填写表格的空白处:(填编号)
| 分类标准 | 能导电的物质 | 电解质 | 非电解质 | 既不是电解质,也不是非电解质 |
| 属于该类的物质 |
(2)某学习小组为证实
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。
溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示。

[实验过程与记录]
| 实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入 的 的 溶液和2滴酚酞溶液,逐滴滴加 溶液和2滴酚酞溶液,逐滴滴加 的 的 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 | ① | ② 溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
(3)书写下列两种情况的离子方程式
①向
 溶液中逐滴加入
溶液中逐滴加入 溶液至恰好完全沉淀
溶液至恰好完全沉淀②向
 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性 溶液
溶液(4)写出
 溶液中
溶液中 的电离方程式
的电离方程式
您最近一年使用:0次
名校
解题方法
2 . 按要求填空:
(1)现有下列物质,请用序号填空:
①硫酸钡 ②固体氢氧化钠 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑤蔗糖 ⑦二氧化硫
上述状态下可导电的是_______ 。属于电解质的是_______ 。属于非电解质的是_______ 。
(2)向50 mL沸水中加入5~6滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用_______ 来证明得到的分散系是氢氧化铁胶体,生成胶体的化学方程式为_______ 。
(3) 固体溶于水的电离方程式为
固体溶于水的电离方程式为_______ 。
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为_______ 。
(5)在常温下,发生下列几种反应:
①
②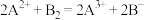
③
反应①~③中的氧化剂和氧化产物的氧化性由强到弱的顺序为_______ ,若某溶液中有 、
、 、
、 共存,加入足量
共存,加入足量 后,离子浓度保持不变的是
后,离子浓度保持不变的是_______ 。
(1)现有下列物质,请用序号填空:
①硫酸钡 ②固体氢氧化钠 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑤蔗糖 ⑦二氧化硫
上述状态下可导电的是
(2)向50 mL沸水中加入5~6滴饱和
 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)
 固体溶于水的电离方程式为
固体溶于水的电离方程式为(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为
(5)在常温下,发生下列几种反应:
①

②
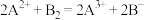
③

反应①~③中的氧化剂和氧化产物的氧化性由强到弱的顺序为
 、
、 、
、 共存,加入足量
共存,加入足量 后,离子浓度保持不变的是
后,离子浓度保持不变的是
您最近一年使用:0次
名校
解题方法
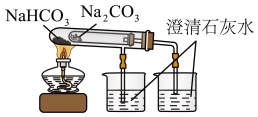
3 . 表中是常见的物质,根据要求完成空格
(1) 在生活中有重要用途,可作食品加工中的
在生活中有重要用途,可作食品加工中的_______ ,将其固体加热可得到上述物质中的另一种盐,写出反应的方程式_______ 。
(2)上述物质的类别有一项错误的是_______ (写序号),熔融状态可以导电的电解质有_______ 种,属于非电解质的是_______ (写序号)。
(3)证明MgO是碱性氧化物可以与上述物质中的酸反应,写出化学方程式_______ 。
(4)写出 在水中的电离方程式
在水中的电离方程式_______ 。
| 物质 | ① | ② | ③ | ④ |
| 类别 | 盐 | 酸 | 氧化物 | 单质 |
| 物质 | ⑤ | ⑥ | ⑦MgO | ⑧ |
| 类别 | 盐 | 碱 | 氧化物 | 酸 |
(1)
 在生活中有重要用途,可作食品加工中的
在生活中有重要用途,可作食品加工中的(2)上述物质的类别有一项错误的是
(3)证明MgO是碱性氧化物可以与上述物质中的酸反应,写出化学方程式
(4)写出
 在水中的电离方程式
在水中的电离方程式
您最近一年使用:0次
解题方法
4 . 依据下列实验事实,所得现象或结论正确的是
| 选项 | 图片 | 实验 | 现象或结论 |
| A | 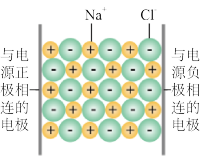 | 测试干燥NaCl固体的导电性 | 干燥的NaCl固体不导电,因为Na+和Cl-按照一定规则紧密地排列着,不能自由移动,所以NaCl固体不是电解质 |
| B |  | 切割钠 | 新切开的钠光亮的表面很快变暗,是因为钠和氧气反应生成了一薄层氧化钠 |
| C | 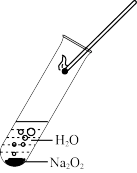 | Na2O2和水反应 | 过氧化钠和水反应放热,产生的气体能使带火星的木条复燃,生成的溶液能使pH试纸先变红后褪色 |
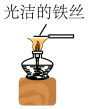
| D |  | 焰色试验:用光洁的铂丝蘸取某溶液在酒精灯外焰灼烧 | 火焰呈黄色,证明原溶液中一定含有Na+,一定没有K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
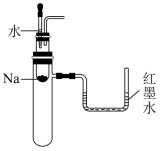
5 . 下列实验装置不能达到实验目的的是
A.验证Na和水反应是否为放热反应 | B.证明氯化钠是电解质 | C.观察 | D.比较 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 实验室有如下物质:①Fe ②酒精 ③CaCO3④熔融的K2SO4 ⑤饱和FeCl3溶液⑥CO 2⑦NH4HCO3 ⑧稀盐酸⑨NaHSO4回答下列问题:
(1)某同学将③④⑨归为一类,他的分类依据是_______ 。
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于电解质的有_______ (填编号,下同)
(3)以上物质能导电的有_______ 。
(4)写出⑦在水中的电离方程式_______ 。
(5)向 溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式
溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式_______ 。
(6)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
①其中操作正确的同学是_______ ;他的操作中涉及到的化学反应方程式为_______ 。
②证明有Fe(OH)3胶体生成的现象是_______ 。
(1)某同学将③④⑨归为一类,他的分类依据是
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于电解质的有
(3)以上物质能导电的有
(4)写出⑦在水中的电离方程式
(5)向
 溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式
溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式(6)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
①其中操作正确的同学是
②证明有Fe(OH)3胶体生成的现象是
您最近一年使用:0次
2022-11-15更新
|
209次组卷
|
3卷引用:甘肃省兰州第一中学2022-2023学年高一上学期期中考试化学试题
名校
7 . 现有下列物质:①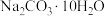 晶体②铜③硫酸溶液④
晶体②铜③硫酸溶液④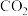 ⑤熔融
⑤熔融 ⑥
⑥ 固体⑦红褐色的氢氧化铁胶体⑧盐酸⑨
固体⑦红褐色的氢氧化铁胶体⑧盐酸⑨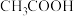 ⑩
⑩ 固体。
固体。
(1)上述物质中既能导电又属于电解质的是_______ 。(填编号)写出⑩在水溶液中的电离方程式_______
(2)仅用上述物质之间的反应
写出能证明④是酸性氧化物的离子方程式______ ;上述物质中有两种物质之间可发生离子反应: ,写出该离子反应对应的其中一个化学方程式
,写出该离子反应对应的其中一个化学方程式_______ 。
(3)制取⑦的化学方程式_______ 。
(4) ,其中水的作用是
,其中水的作用是_______ 。(填“氧化剂”或“还原剂”或“既不是氧化剂也不是还原剂”)
(5)②物质灼烧时,焰色试验为_______ 色。
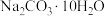 晶体②铜③硫酸溶液④
晶体②铜③硫酸溶液④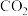 ⑤熔融
⑤熔融 ⑥
⑥ 固体⑦红褐色的氢氧化铁胶体⑧盐酸⑨
固体⑦红褐色的氢氧化铁胶体⑧盐酸⑨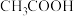 ⑩
⑩ 固体。
固体。(1)上述物质中既能导电又属于电解质的是
(2)仅用上述物质之间的反应
写出能证明④是酸性氧化物的离子方程式
 ,写出该离子反应对应的其中一个化学方程式
,写出该离子反应对应的其中一个化学方程式(3)制取⑦的化学方程式
(4)
 ,其中水的作用是
,其中水的作用是(5)②物质灼烧时,焰色试验为
您最近一年使用:0次
2022-10-28更新
|
354次组卷
|
2卷引用:辽宁省大连市二十四中2021-2022学年高一上学期期中化学试题
名校
解题方法
8 . 央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)现有以下物质:① 溶液;②液氨:③
溶液;②液氨:③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑧铜;⑦
胶体;⑧铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是
;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是_______ (填序号),属于非电解质的是:_______ (填序号)。写出④在该条件下的电离方程式:_______ ,⑧在水溶液条件下的电离方程式:_______ 。
(2)明胶的水浴液和 溶液共同具备的性质是
溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置会产生沉淀 b.分散质粒子可通过滤纸 c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_______ (填序号)。
A. B.
B.  C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的检验方法是
胶体,证明有胶体生成的最常用的检验方法是_______ 。
(5)现有10 明胶的水溶液与5
明胶的水溶液与5
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜进入溶液:
能够透过半透膜进入溶液:_______ 。
(1)现有以下物质:①
 溶液;②液氨:③
溶液;②液氨:③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑧铜;⑦
胶体;⑧铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是
;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是(2)明胶的水浴液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置会产生沉淀 b.分散质粒子可通过滤纸 c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B.  C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和
 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的检验方法是
胶体,证明有胶体生成的最常用的检验方法是(5)现有10
 明胶的水溶液与5
明胶的水溶液与5
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜进入溶液:
能够透过半透膜进入溶液:
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题
(1)现有以下物质①NaCl溶液;②二氧化碳;③纯净的醋酸;④铜;⑤NaOH固体;⑥蔗糖;⑦硫酸钡;⑧水,属于电解质的是:_______ 。(填写序号)
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为_______ 。
②证明红褐色液体是胶体的实验操作是_______ 。
③物质M和红褐色液体的本质区别是_______ 。
(3)在实验室制氯气的反应中:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,氧化剂为
MnCl2+Cl2↑+2H2O,氧化剂为_______ ;氧化产物为_______ ;氧化剂与还原剂的分子个数比值为_______ 。
(4)目前,汽车尾气系统中安装了催化转化器。在催化转化器中汽车尾气中的CO和NO在催化剂的作用下发生反应,生成两种大气中常见的无污染气体。请写出反应的化学方程式:_______ 。
(1)现有以下物质①NaCl溶液;②二氧化碳;③纯净的醋酸;④铜;⑤NaOH固体;⑥蔗糖;⑦硫酸钡;⑧水,属于电解质的是:
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为
②证明红褐色液体是胶体的实验操作是
③物质M和红褐色液体的本质区别是
(3)在实验室制氯气的反应中:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,氧化剂为
MnCl2+Cl2↑+2H2O,氧化剂为(4)目前,汽车尾气系统中安装了催化转化器。在催化转化器中汽车尾气中的CO和NO在催化剂的作用下发生反应,生成两种大气中常见的无污染气体。请写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . I.对下列15种物质进行分类:①KOH,②Ba(OH)2,③(NH4)2SO4,④碘酒,⑤NO,⑥HNO3,⑦葡萄糖,⑧汽油,⑨O3,⑩H2SO4,⑪CH4,⑫石墨,⑬CaCO3,⑭酒精,⑮Fe3O4
(1)属于混合物的是____ (填序号,下同),属于单质的是____ ,属于酸的是____ ,属于碱的是____ ,属于盐的是____ ,属于氧化物的是____ ,属于有机物的是____ 。
II.有下列10种物质:①液态HCl,②NH4Cl,③蔗糖,④Fe,⑤稀硫酸,⑥熔融NaCl,⑦氢氧化钠固体,⑧淀粉溶液,⑨CaO,⑩H2O。回答下列问题:
(2)上述物质中,属于电解质的是____ (填序号,下同),属于非电解质的是____ ,在上述状态下能够导电的是____ 。
(3)写出④和⑤反应的离子方程式:____ 。
(4)写出②在水溶液中的电离方程式:____ 。
(5)如何证明⑧是胶体,请简述操作:____ 。
(1)属于混合物的是
II.有下列10种物质:①液态HCl,②NH4Cl,③蔗糖,④Fe,⑤稀硫酸,⑥熔融NaCl,⑦氢氧化钠固体,⑧淀粉溶液,⑨CaO,⑩H2O。回答下列问题:
(2)上述物质中,属于电解质的是
(3)写出④和⑤反应的离子方程式:
(4)写出②在水溶液中的电离方程式:
(5)如何证明⑧是胶体,请简述操作:
您最近一年使用:0次

 的焰色试验
的焰色试验