解题方法
1 . 为了减少煤燃烧产生的二氧化硫的排放,可以采取各种方法,其中一种方法是使用微生物脱硫技术。煤炭中以FeS2形式存在的硫,在有水和空气存在的条件下,用脱硫微生物起氧化还原作用:在细菌作用下FeS2 中的硫元素首先被氧化最高价态,然后亚铁离子继续被氧化成高价铁离子。
(1)请分别写出上述过程总离子反应方程式___________ 。
(2)某大型电厂使用的煤炭中含有FeS2的质量分数为1.2%,若每月燃烧该种煤炭100万吨,理论上回收硫酸___________ 吨;硫酸铁___________ 吨。
(1)请分别写出上述过程总离子反应方程式
(2)某大型电厂使用的煤炭中含有FeS2的质量分数为1.2%,若每月燃烧该种煤炭100万吨,理论上回收硫酸
您最近一年使用:0次
解题方法
2 .
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象_____ ,写出两步主要反应的离子方程式______
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分_____ 。
(3)第二步失重后的固态残渣是______ ,解释理由______ 。
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分
(3)第二步失重后的固态残渣是
您最近一年使用:0次
解题方法
3 . I.水中溶解氧气的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,反应方程式为2S2O +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 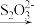 S4O
S4O 。
。
(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:____________________ 。
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为_________ mg·L-1。
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为________ mol/L(保留一位小数),需用量筒量取30%的双氧水_________ mL。
(2)该实验在酸性条件下进行,则实验设计的反应原理是_____________ (用离子方程式表示)。
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为_________ (用含a、b的式子表示)。
 +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 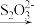 S4O
S4O 。
。(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为
(2)该实验在酸性条件下进行,则实验设计的反应原理是
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
您最近一年使用:0次
名校
4 . 烟道气中的 NO 是主要的大气污染物之一,为了监测其含量,选用如下检测方法:将vL气样通入适量酸化的 H2O2 溶液中,恰好使 NO 完全被氧化成NO3-,加水稀释至 100.00mL。量取20.00mL该溶液,加入v1mLc1mol·L-1FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗 v2mL。回答下列问题:
(1)NO被H2O2氧化为NO3-的离子方程式为:_____ 。
(2)滴定过程中发生下列反应:
3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NO的物质的量为_______ mol。
(3)下列操作会使 NO 测定结果偏高的是_____
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4 标准溶液部分变质
(1)NO被H2O2氧化为NO3-的离子方程式为:
(2)滴定过程中发生下列反应:
3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NO的物质的量为
(3)下列操作会使 NO 测定结果偏高的是
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4 标准溶液部分变质
您最近一年使用:0次
5 . 将1.66 g碳酸钠和氢氧化钠的固体混合物完全溶于水配成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示。

请回答下列问题:
(1)OA段是盐酸与Na2CO3和NaOH发生的反应,反应后溶液中的溶质有_________ (填化学式)。
(2)当到达B点时,产生CO2的体积为________________ mL(标准状况)。
(3)计算原混合物中Na2CO3的质量分数________________ 。(写出必要计算过程,结果保留3位有效数字)

请回答下列问题:
(1)OA段是盐酸与Na2CO3和NaOH发生的反应,反应后溶液中的溶质有
(2)当到达B点时,产生CO2的体积为
(3)计算原混合物中Na2CO3的质量分数
您最近一年使用:0次
2016-12-09更新
|
688次组卷
|
2卷引用:2014-2015河北省邯郸市高一上学期期末考试化学试卷
6 . 某K2CO3与KHCO3的混合物共6.14 g,加热分解后质量减少为5.52 g。
(1)求原混合物中K2CO3的质量分数。(写出计算过程,计算结果精确到0.1%)
(2)若将原混合物溶于200 mL水配成溶液,向溶液中逐滴加入1.0 mol·L-1的稀盐酸。当加入的稀盐酸的体积为 mL时开始产生气体;当加入50 mL稀盐酸时,产生的气体在标准状况下的体积为 mL。
(1)求原混合物中K2CO3的质量分数。(写出计算过程,计算结果精确到0.1%)
(2)若将原混合物溶于200 mL水配成溶液,向溶液中逐滴加入1.0 mol·L-1的稀盐酸。当加入的稀盐酸的体积为 mL时开始产生气体;当加入50 mL稀盐酸时,产生的气体在标准状况下的体积为 mL。
您最近一年使用:0次
10-11高三上·浙江杭州·阶段练习
7 . 金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。
⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平__________________ ;
⑵ 试样中锡的质量分数(假定杂质不参加反应)__________________ 。
⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平
⑵ 试样中锡的质量分数(假定杂质不参加反应)
您最近一年使用:0次



