1 . 将锌粒放入含有 、
、 、
、 三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
(1)请写出反应过程中一定发生反应的化学方程式____ 。
(2)若某次实验后小强对滤液中溶质的成分小强作出了以下猜想: 、
、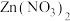 、
、 ,老师说小强的猜想不合理。请你写出该猜想不合理的原因
,老师说小强的猜想不合理。请你写出该猜想不合理的原因________ 。
 、
、 、
、 三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。
三种溶质的溶液中,充分反应后过滤,得到滤渣和滤液。以下是对滤渣或滤液成分的探究。(1)请写出反应过程中一定发生反应的化学方程式
(2)若某次实验后小强对滤液中溶质的成分小强作出了以下猜想:
 、
、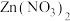 、
、 ,老师说小强的猜想不合理。请你写出该猜想不合理的原因
,老师说小强的猜想不合理。请你写出该猜想不合理的原因
您最近一年使用:0次
名校
解题方法
2 .  四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
已知:A溶液呈强酸性,且A溶液与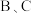 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。
回答下列问题:
(1)写出C的化学式:_____________ , 的电子式:
的电子式:_____________ 。
(2)写出A溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:_____________ 。
(3)A中阴离子的检验操作_____________________________________ 。
(4)请选出适合存放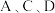 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)
 四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。| 阴离子 | 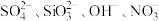 |
| 阳离子 | 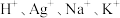 |
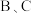 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。回答下列问题:
(1)写出C的化学式:
 的电子式:
的电子式:(2)写出A溶液与
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)A中阴离子的检验操作
(4)请选出适合存放
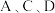 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)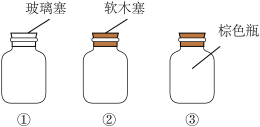
溶液 | A | C |
|
试剂瓶序号 |
您最近一年使用:0次
3 . 已知a、b、c、d、e分别是Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种物质水溶液中的各一种。它们互相反应的情况如下表所示:
“↓”表示生成沉淀;“↑”表示产生气体;“-”表示无明显现象;“/”表示实验未做。
由上表可推知:c是___________ ,e是___________ (均填化学式)。
| a | b | c | d | e | |
| c | ↓ | ↓ | / | ↑ | - |
| b | ↓ | / | ↓ | - | - |
由上表可推知:c是
您最近一年使用:0次
4 . Ⅰ.某无色透明溶液中可能大量存在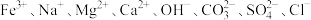 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。
(1)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
Ⅱ.次磷酸 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。
(2)写出白磷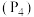 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:_______ ,反应中每消耗 ,转移的电子数为
,转移的电子数为_______ 。
(3)写出 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)工业上利用 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为_______ 。
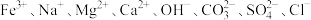 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。(1)根据上述实验现象可知,原溶液中一定存在的离子是
Ⅱ.次磷酸
 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。(2)写出白磷
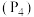 与
与 溶液反应的化学方程式:
溶液反应的化学方程式: ,转移的电子数为
,转移的电子数为(3)写出
 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(4)工业上利用
 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为
您最近一年使用:0次
名校
5 . I.回答下列问题:
(1)填写表格中的空白:___________ 。
II.某化学社团为证实溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应时离子反应。实验装置如图所示: 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性___________ 。继续滴加 溶液
溶液___________ 。
III.某化工厂排出的废水呈酸性,且其中含大量的 、
、 、
、 、
、 、
、 ,为除去废水样品中的
,为除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图:___________ (用离子符号表示)。
(4)上述流程中,试剂c为___________ (写化学式);溶液3所含溶质离子有 、
、___________ 。
(5)“分离操作”的名称是___________ ,需用到的玻璃仪器主要有___________ 。
| 实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入一定浓度的 溶液,逐滴滴加 溶液,逐滴滴加 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 | ___________(填写支持实验结论的证据) |  溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
(1)填写表格中的空白:
II.某化学社团为证实溶液和
 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应时离子反应。实验装置如图所示:
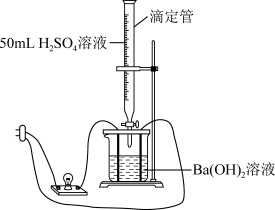
 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性 溶液
溶液III.某化工厂排出的废水呈酸性,且其中含大量的
 、
、 、
、 、
、 、
、 ,为除去废水样品中的
,为除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图: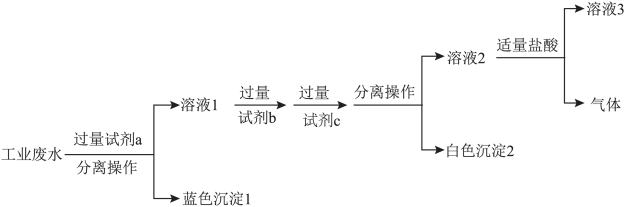
(4)上述流程中,试剂c为
 、
、(5)“分离操作”的名称是
您最近一年使用:0次
名校
6 . 现有失去标签的CaCl2、AgNO3、HCl和Na2CO3四瓶溶液。为了确定这四种溶液成分,将它们编号为A、B、C、D后进行化学实验。实验记录如下:
根据上述实验填空:
(1)A、B、C三瓶溶液分别是_______ 、_______ 、_______ (用化学式表示)。
(2)B和D反应的离子方程式是_______ 。
(3)A和B不发生反应的理由是_______ 。
| 实验顺序 | 实验药品 | 实验现象 |
| 1 | A+B | 无明显现象 |
| 2 | B+D | 有气体生成 |
| 3 | C+B | 有沉淀生成 |
| 4 | A+D |
(1)A、B、C三瓶溶液分别是
(2)B和D反应的离子方程式是
(3)A和B不发生反应的理由是
您最近一年使用:0次
名校
解题方法
7 . NaCl溶液中混有Na2CO3、Na2SO4,为检验两种物质的存在,你先后需要的试剂有___________ 溶液、澄清石灰水和___________ 溶液,请按实验先后顺序写出相应的离子方程式:___________ 、 ___________ 、___________ 。
您最近一年使用:0次
解题方法
8 . Ⅰ.FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。回答下列问题。
(1)按照物质的分类方法,FeCl3应属于_______ (填序号)。
①酸 ②氯化物 ③混合物 ④盐 ⑤电解质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为_____________________ 。
(3)某河道两旁甲、乙两厂,它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是_________ 。
(4)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此H3PO2属于______ (选填“一”、“二”或“三”)元酸。NaH2PO2属于_____ (选填“正盐”或“酸式盐”)。
(1)按照物质的分类方法,FeCl3应属于
①酸 ②氯化物 ③混合物 ④盐 ⑤电解质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)某河道两旁甲、乙两厂,它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、
 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是(4)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此H3PO2属于
您最近一年使用:0次
名校
9 . 聚合硫酸铁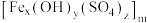 简称PFS,是一种高效絮凝剂,广泛用于水的净化,其中铁元素为+3价。
简称PFS,是一种高效絮凝剂,广泛用于水的净化,其中铁元素为+3价。
(1)聚合硫酸铁PFS化学式中x、y、z之间的等量关系式是______ 。
(2)用聚合硫酸铁PFS进行模拟净化高岭土废水。该高岭土废水净化效果(即浊度去除率)受絮凝剂的投加量及 的影响如图1、图2所示:
的影响如图1、图2所示:

可知聚合硫酸铁PFS最佳投加量是______  ,最佳
,最佳 是
是________ 。
(3)为测定某聚合硫酸铁样品中铁的质量分数,进行如下实验:
a.准确称取 该聚合硫酸铁样品溶于适量的硫酸,配成
该聚合硫酸铁样品溶于适量的硫酸,配成 溶液A。
溶液A。
b.准确量取 溶液A,加入足量铜粉,将
溶液A,加入足量铜粉,将 还原为
还原为 ,充分反应后过滤、洗涤,将滤液和洗涤的滤出液合并配成溶液B。
,充分反应后过滤、洗涤,将滤液和洗涤的滤出液合并配成溶液B。
c.用 的酸性
的酸性 溶液滴加到溶液B中至恰好反应完全,消耗
溶液滴加到溶液B中至恰好反应完全,消耗 溶液
溶液 。
。
反应原理: (未配平),请先配平步骤c中的离子方程式
(未配平),请先配平步骤c中的离子方程式_________ ,并通过计算确定该聚合硫酸铁样品中铁的质量分数______ (写出计算过程)。
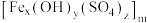 简称PFS,是一种高效絮凝剂,广泛用于水的净化,其中铁元素为+3价。
简称PFS,是一种高效絮凝剂,广泛用于水的净化,其中铁元素为+3价。(1)聚合硫酸铁PFS化学式中x、y、z之间的等量关系式是
(2)用聚合硫酸铁PFS进行模拟净化高岭土废水。该高岭土废水净化效果(即浊度去除率)受絮凝剂的投加量及
 的影响如图1、图2所示:
的影响如图1、图2所示:
可知聚合硫酸铁PFS最佳投加量是
 ,最佳
,最佳 是
是(3)为测定某聚合硫酸铁样品中铁的质量分数,进行如下实验:
a.准确称取
 该聚合硫酸铁样品溶于适量的硫酸,配成
该聚合硫酸铁样品溶于适量的硫酸,配成 溶液A。
溶液A。b.准确量取
 溶液A,加入足量铜粉,将
溶液A,加入足量铜粉,将 还原为
还原为 ,充分反应后过滤、洗涤,将滤液和洗涤的滤出液合并配成溶液B。
,充分反应后过滤、洗涤,将滤液和洗涤的滤出液合并配成溶液B。c.用
 的酸性
的酸性 溶液滴加到溶液B中至恰好反应完全,消耗
溶液滴加到溶液B中至恰好反应完全,消耗 溶液
溶液 。
。反应原理:
 (未配平),请先配平步骤c中的离子方程式
(未配平),请先配平步骤c中的离子方程式
您最近一年使用:0次
10 . 回答下列问题:
I.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式_______ 。
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为_______ 。
(4)通过以上实验确定原溶液中一定含有的阳离子是_______ ,不能确定的阳离子是_______ 。
(5)原溶液可能大量存在的阴离子是下列的_______。
II.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(6)同温同压下,M、N气体的密度之比为_______ 。
(7)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为_______ 。
I.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为
(4)通过以上实验确定原溶液中一定含有的阳离子是
(5)原溶液可能大量存在的阴离子是下列的_______。
| A.Cl- | B.NO | C.CO | D.OH- |
II.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(6)同温同压下,M、N气体的密度之比为
(7)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为
您最近一年使用:0次



