10-11高一上·浙江嘉兴·阶段练习
1 . 根据下列反应:(1) ;(2)
;(2) ,判断离子的还原性由强到弱的顺序是
,判断离子的还原性由强到弱的顺序是
 ;(2)
;(2) ,判断离子的还原性由强到弱的顺序是
,判断离子的还原性由强到弱的顺序是A. | B.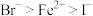 | C.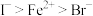 | D.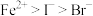 |
您最近一年使用:0次
2023-02-16更新
|
1075次组卷
|
134卷引用:【全国百强校】山东省济南外国语学校2017-2018学年高二6月份学业水平会考模拟化学试题
【全国百强校】山东省济南外国语学校2017-2018学年高二6月份学业水平会考模拟化学试题(已下线)2010年浙江省嘉兴一中高一上学期10月月考化学试题(已下线)2011届福建省周宁十中高三上学期第二次月考化学卷(已下线)2010年河南省郑州外国语学校高一上学期期中考试化学卷(已下线)2010年黑龙江大庆实验中学高一上学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州十四中高一上学期期末化学试卷(已下线)2011-2012学年山东省冠县一中高一上学期末模块考试化学试卷(已下线)2011-2012学年广东省汕头金山中学高一第一学期期末考试化学试卷(已下线)2011-2012学年山东省冠县武训高中高一上期末测试化学试卷(已下线)2012-2013学年甘肃省天水市一中高一第一学段期中考试化学试卷(已下线)2012-2013学年浙江省苍南县求知中学高二上学期期中考试文科化学试卷(已下线)2012-2013学年山东省鱼台一中高一上学期期末模拟化学试卷(已下线)2012-2013学年广东省汕头四中高一上学期期末考试化学试卷(已下线)2013-2014学年贵州省册亨县民族中学高一上学期期末考试化学试卷(已下线)2014-2015学年吉林省长春十一中高一上考试化学试卷(已下线)2015届甘肃省天水市第一中学高一上学期期中考试化学试卷(已下线)2014-2015学年湖南省怀化三中高一上学期期中化学试卷2014—2015陕西岐山县高一上学期期末质量检测化学试卷2015-2016学年湖北省宜昌市葛洲坝中学高一上学期期中测试化学试卷2015-2016学年吉林省实验中学高一上期末(理)化学试卷2015-2016学年内蒙古包头市包钢四中高一上学期期末化学试卷2016-2017学年甘肃省天水一中高一上开学考试化学试卷2016-2017学年河北省承德一中高一上学期月考二化学试卷 2016-2017学年湖北省宜昌市葛洲坝中学高一上期中化学卷2016-2017学年河北省石家庄市第一中学高一上学期期末考试化学试卷2017-2018学年高一人教版必修一:11 氧化剂和还原剂课时训练化学试题宁夏银川市兴庆区2018届高三上学期第二次月考化学试题浙江省温州中学2017-2018学年高一上学期期中考试化学试题重庆市南川三校联盟2017-2018学年高一上学期期中考试化学试题陕西省渭南市尚德中学2017-2018学年高一上学期第二次月考化学试题甘肃省靖远一中2017-2018学年高一上学期期中考试化学试题安徽省濉溪县临涣中学2017-2018学年高一上学期第二次月考化学试题【全国区级联考】山东省聊城市东昌府区2018-2019学年高一上学期第一次月考化学试题云南省沾益县第四中学2017-2018学年高一上学期期末考试化学试题【全国校级联考】新疆维吾尔自治区昌吉市教育共同体2019届高三上学期9月月考化学试题甘肃省高台县第一中学2018-2019学年高一上学期期中考试化学试题广东省广州市中山大学附属中学2018-2019学年高一第一学期期中考试化学试题【校级联考】广西壮族自治区南宁市马山县金伦中学“4+ N”高中联合体2018-2019学年高一上学期期中考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一上学期第二次月考化学试题【全国百强校】云南省玉溪市第一中学2018-2019学年高一上学期期中考试化学试题山东省微山县第二中学2018-2019学年高一上学期第三学段教学质量监测化学试题【市级联考】浙江省台州市2018-2019学年高一下学期期中考试化学试题步步为赢 初高中衔接教材化学暑假作业:第14课时 氧化还原反应的表示和规律山东省济宁市北大培文学校2018-2019学年高一上学期期中考试化学试题人教版新教材化学同步1.3.2 氧化剂和还原剂练习(1)2019-2020学年高一上学期期中考试模拟化学试题(B)云南省保山市昌宁县一中2019-2020学年高一10月月考化学试题云南省文山壮族苗族自治州马关县第一中学校2019-2020学年高一上学期10月月考化学试题宁夏银川一中2019-2020学年高一上学期期中考试化学试题黑龙江省海林市朝鲜族中学2019-2020学年高一上学期期中考试化学试题辽宁省朝阳市凌源三中2019-2020学年高一上学期第二次月考化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期第二次月考化学试题宁夏回族自治区顶级名校2019-2020学年高一上学期12月考试化学试题黑龙江省齐齐哈尔市龙江二中2019-2020学年高一上学期12月月考化学试题四川省达州市宣汉中学2019—2020学年高一上学期月考化学试题新疆维吾尔自治区乌鲁木齐市第130中学2018-2019学年高一上学期期中考试化学试题黑龙江省伊春市第二中学2019-2020学年高一上学期期末考试化学(理)试题黑龙江省农垦建三江管理局第一中学2019-2020学年高一上学期期末考试化学试题福建省师范大学附属中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第二章《化学物质及其变化》测试卷4辽宁省丹东市2019-2020学年高一上学期期末质量监测化学试题贵州省贞丰县第二中学2019-2020学年高一上学期期末考试化学试题甘肃省张掖市高台县第一中学2019-2020学年高一上学期化学期中考试化学试题上海市松江二中2014-2015学年高一上学期期末考试化学试题吉林省长春市九台区第四中学2019-2020高一上学期期末测试化学试题广东省茂名地区2017-2018学年高一上学期期中考试化学试题上海市南洋模范中学2019-2020学年高一上学期期末考试化学试题广东省湛江市第二十一中学2019-2020学年高一上学期期中考试化学试题(已下线)衔接点07 氧化剂和还原剂-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)1.3.2 氧化剂和还原剂 练习(2)——《高中新教材同步备课》(人教版 必修第一册)辽宁省铁岭市调兵山市第二高级中学2019—2020学年高一下学期线上教学测试化学试题福建省泰宁第一中学2018-2019学年高一上学期第二阶段考试化学试题辽宁省凌源市第三高级中学2019-2020学年高二下学期第四次月考化学试题(已下线)海南省儋州一中2018-2019学年高一上学期期中考试化学试卷(已下线)【浙江新东方】双师 (1)安徽省定远县育才学校2020-2021学年高一上学期11月质量检测化学试题(已下线)【浙江新东方】在线化学 (2).内蒙古包头钢铁公司第四中学2020-2021学年高一上学期期中考试化学试题辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP400】【化学】河南省新乡市长垣市第十中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】64.贵州省毕节市实验高级中学2020-2021学年高一上学期期中考试化学试题江苏省沭阳县修远中学2021届高三第四次质量检测化学(艺术班)试题湖南省娄底市春元中学2020-2021学年高一上学期期中考试化学试题专题3 第一单元 第3课时 氧化还原反应-高中化学苏教2019版必修第一册宁夏平罗中学2020-2021学年高一上学期期末考试化学试题辽宁省大连市金普新区2020-2021学年高一下学期开学检测化学试题(已下线)【浙江新东方】高中化学20210304-017黑龙江省鸡东二中2020-2021学年高一上学期期末考试化学试题安徽省芜湖市第一中学2019-2020学年高一上学期12月月考化学试题(已下线)衔接点07 氧化剂和还原剂-2021年初升高化学无忧衔接(已下线)专题1.3.3 氧化剂、还原剂(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)云南省曲靖市罗平县第二中学2020-2021学年高一下学期6月月考文科化学试题河南宋基信阳实验中学2021-2022学年高三9月开学摸底考试化学试题 (已下线)专题卷二 氧化还原反应(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)海南省东方市琼西中学2021-2022学年高三上学期第一次月考化学试题甘肃省庆阳市第六中学2021-2022学年高一上学期第一次月考化学试题河南省新乡县龙泉高级中学2021-2022学年高一上学期9月月考化学试题黑龙江省哈尔滨市第三中学校2021-2022学年上学期高一学年第一次验收考试化学试题宁夏吴忠中学2021-2022学年高一上学期期中考试化学试题四川省达州市第一中学校2021-2022学年高一上学期期中考试化学试题黑龙江省绥化市第一中学2020-2021学年高一上学期期末考试化学试题(已下线)衔接点12 氧化剂和还原剂-2022年初升高化学无忧衔接?吉林省乾安县第四中学2021-2022学年高一上学期期中考试化学试题浙江省嘉善中学2022-2023学年高一上学期10月份检测化学试题上海市敬业中学2022-2023学年高二上学期10月月考(等级考)化学试题天津市第九十五中学益中学校2022-2023学年高一上学期期中考试化学试题河北省文安县第一中学2022-2023学年高一上学期10月份考试化学试题辽宁省重点高中沈阳市郊联体2022-2023学年高一上学期期中考试化学试题甘肃省武威市古浪县第二中学2021-2022学年高一上学期期中化学试题天津市八校联考2022-2023学年高一上学期期中考试化学试题河北省武强中学2022-2023学年高一上学期期中考试化学试题福建省莆田第一中学2022-2023学年高一上学期12月月考化学试题广东省潮州市潮安区宝山中学2022-2023学年高一上学期期中考试化学试题辽宁省沈阳市辽中区第二高级中学2022-2023学年高一上学期期中考试化学试题陕西省咸阳市泾阳县泾干中学2021-2022学年高一上学期期末考试化学试题湖南省岳阳市平江县第三中学2021-2022学年高一上学期期中考试化学试题湖北省武汉海淀外国语实验学校2022-2023学年高一上学期10月月考化学试题新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2022-2023学年高一上学期期末测试化学试题湖南省郴州市2022-2023学年高一上学期期末测试化学试题湖南省张家界市民族中学2022-2023学年高一上学期期中考试化学试题(已下线)考点巩固卷02 化学物质及其变化(3大考点44题)?-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)作业(十五) 氧化剂和还原剂陕西省延安市宜川中学2020-2021学年高一上学期期末考试化学试题云南省保山市高(完)中C、D类学校2022-2023学年高一上学期10月联考化学试题福建省厦门第一中学2023-2024学年高二上学期开学考试化学试题新疆乌鲁木齐市高级中学2023-2024学年高一上学期第一次月考化学试题(已下线)专题七 氧化还原反应浙江省台州八校联盟2023-2024学年高一上学期期中联考化学试题广东省珠海市第二中学2023-2024学年高一上学期10月月考化学试题福建省福州教育学院第二附属中学2023-2024学年高一上学期12月月考化学试卷新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高三上学期第一次月考 化学试题
解题方法
2 . “曾青得铁则化为铜”涉及反应的离子方程式为: ,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
 ,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是A.该反应中 被氧化 被氧化 |
| B.该反应属于有离子参加的置换反应 |
| C.该反应说明Fe的金属活动性比Cu的弱 |
| D.该反应说明金属单质都能与盐发生反应 |
您最近一年使用:0次
3 . 根据反应①Fe+Cu2+=Fe2++Cu; ②2Fe3++Cu=Cu2++2Fe2+;③2Fe2++Cl2=2Fe3++2Cl-; ④HClO+H++Cl-=Cl2+H2O。可以判断出各微粒的氧化性由强到弱的顺序正确的是
| A.HClO>Cl2>Fe3+>Cu2+>Fe2+ | B.Cl2>HClO>Fe3+>Cu2+>Fe2+ |
| C.Cl2>Fe3+>HClO>Cu2+>Fe2+ | D.HClO>Cl2>Cu2+>Fe3+>Fe2+ |
您最近一年使用:0次
2021-09-12更新
|
1290次组卷
|
28卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(二)
2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(二)【校级联考】天津市宝坻区普通高中2018-2019学年高一上学期三校联考化学试题天津市静海区大邱庄中学等四校2019-2020学年高一10月联考化学试题2020届高三化学大二轮增分强化练——氧化还原反应湖北省恩施州清江外国语学校2019-2020学年高二上学期期末考试化学试题天津市第九十五中学2019-2020学年高一下学期3月线上测试化学试题(已下线)【浙江新东方】75.四川省眉山市东坡区多悦高级中学校2020-2021学年高一12月月考化学试题宁夏青铜峡市高级中学2020-2021学年高一上学期期末考试化学试题河北省石家庄市第一中学2020~2021学年高一上学期期中试题化学试题新疆阿勒泰地区2018-2019学年高一上学期期末考试化学试题河北省石家庄市第四中学2020-2021学年高一上学期期中考试化学试题云南省梁河县第一中学2021-2022学年高一上学期第一次月考化学试题天津市武清区杨村第一中学2021-2022学年高一上学期第一次阶段性检测化学试题河北省石家庄市第一中学2021-2022学年高一上学期期中考试化学试卷吉林省梅河口市第五中学2021-2022学年高一上学期期中考试化学试题云南省玉溪师范学院附属中学2021-2022学年高一下学期开学测试化学试题山西省稷山中学2021-2022学年高一上学期第二次月考化学试题黑龙江省密山市第四中学2021-2022学年高一上学期期末考试化学试题江西省金溪县第一中学2022-2023学年高一上学期第一次月考化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期10月联考(人教版)化学试题湖北省荆州市沙市第七中学2021-2022学年高一上学期9月调研考试化学试题山东省枣庄市第三中学2022-2023学年高一上学期12月期中考试化学试题云南省昭通市市直中学2023-2024学年高一上学期联考第一次月考化学试题(已下线)专题七 氧化还原反应天津市宝坻区第一中学2023-2024学年高一上学期10月月考化学试题河南省原阳县第一高级中学2023-2024学年高一上学期10月月考化学试题广东省茂名市高州中学2023-2024学年高一下学期期中考试化学(合格考)试题
名校
解题方法
4 . 下列不能 达到“实验目的”的“实验操作及现象”是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 证明浓硫酸有吸水性 | 向蔗糖中滴加浓硫酸,蔗糖变黑 |
| B | 证明SO2具有漂白性 | 向品红溶液中通入SO2,溶液褪色 |
| C | 证明氧化性:Br2>I2 | 向KI和淀粉的混合溶液中滴加溴水,溶液变蓝 |
| D | 检验NH4Cl溶液中的NH | 向NH4Cl溶液中加入浓NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-17更新
|
305次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
5 . 在45~ 50°C时,臭氧(O3)可以将碘氧化为碘酸碘[I(IO3)3]。反应的化学方程式如下:9O3+2I2=I(IO3)3+ 9O2。下列说法正确的是
| A.O3既不是氧化剂也不是还原剂 |
| B.I(IO3)3中碘元素的化合价均为+5 |
| C.氧化性:I(IO3)3>I2 |
| D.氧化性:I2> I(IO3)3 |
您最近一年使用:0次
解题方法
6 . 下列有关实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 两支试管各盛4 mL 0.1 mol/L酸性高锰酸钾溶液,分别加入2 mL 0.1 mol/L的 草酸溶液和2 mL 0.2 mol/L草酸溶液 | 加入0.2 mol/L草酸溶液的试管中,高锰酸钾溶液完全褪色时间更短 | 反应物浓度越大,反应速率越快 |
| B | 室温下,向 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝色 |  的氧化性比 的氧化性比 的强 的强 |
| C | 将淀粉和稀硫酸混合加热一段时间后,再加入新制的 悬浊液,加热 悬浊液,加热 | 产生砖红色沉淀 | 淀粉在稀硫酸、加热条件下水 解为葡萄糖 |
| D | 取一支试管装入2 mL 2 mol/L NaOH溶液,先滴加1 mL 1 mol/L  溶液,再滴加几滴1 mol/L 溶液,再滴加几滴1 mol/L 溶液 溶液 | 先生成白色沉淀,后沉淀变为蓝色 | 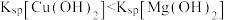 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-11更新
|
348次组卷
|
2卷引用:河南省濮阳市2021-2022学年高二下学期学业质量监测考试化学试题
7 . 元素在周期表中的位置,反映了元素的原子结构和性质。某学习小组以氯、溴、碘三种元素为例。通过实验探究同主族元素非金属性的递变规律,设计如下方案并进行实验。
已知:本实验条件下,溴水呈黄色,碘水呈棕黄色。
回答下列问题:
【实验I】取两支大小相同的试管,分别进行如图所示实验。

(1)A试管中溶液变为黄色,反应的离子方程式是________ ,由此证明氧化性:Cl2________ Br2(填“>”或“<”)。
(2)B试管中观察到的现象是________ ,由此证明氧化性:Cl2>I2。
【实验II】取少量A试管中的黄色溶液于另一支试管中,先加入足量KBr固体,充分振荡,再加入少量KI溶液,最后滴入几滴淀粉溶液,溶液变为蓝色。
(3)“先加入足量KBr固体”的目的:除去溶液中可能含有的________ 。
(4)上述实验证明:氯、溴、碘三种元素的非金属性由强到弱的顺序是________ 。
已知:本实验条件下,溴水呈黄色,碘水呈棕黄色。
回答下列问题:
【实验I】取两支大小相同的试管,分别进行如图所示实验。

(1)A试管中溶液变为黄色,反应的离子方程式是
(2)B试管中观察到的现象是
【实验II】取少量A试管中的黄色溶液于另一支试管中,先加入足量KBr固体,充分振荡,再加入少量KI溶液,最后滴入几滴淀粉溶液,溶液变为蓝色。
(3)“先加入足量KBr固体”的目的:除去溶液中可能含有的
(4)上述实验证明:氯、溴、碘三种元素的非金属性由强到弱的顺序是
您最近一年使用:0次
8 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
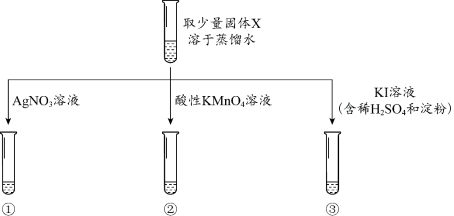
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
283次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
解题方法
9 . 下列物质中可以使湿润的淀粉-KI试纸变蓝的是
| A.HCl | B.Br2 | C.O2 | D.Fe2+ |
您最近一年使用:0次
名校
解题方法
10 . 反应 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是| A.Al的还原性比Mo强 | B.Mo为还原产物 |
| C.Al得到电子 | D. 发生还原反应 发生还原反应 |
您最近一年使用:0次
2022-12-27更新
|
479次组卷
|
5卷引用:江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题
江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题江苏省涟水县第一中学2022-2023学年高二上学期学业水平合格性考试化学试题(已下线)专题七 氧化还原反应(已下线)合格考汇编3氧化还原反应广东省湛江市第二十一中学2023-2024学年高一下学期第一次月考化学(学考)试题



