名校
解题方法
1 . 往 和
和 的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是
的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是
 和
和 的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是
的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是| A.滤渣中一定有Fe粉 | B.滤渣中一定有Cu粉 |
C.滤液中一定有 | D.滤液中一定有 、 、 |
您最近一年使用:0次
2 . 高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为:2Fe(OH)3 + 3ClO- + 4OH- = 2 + 3Cl- + 2H2O。下列有关说法不正确的是
+ 3Cl- + 2H2O。下列有关说法不正确的是
A.由上述反应可知,C1O- 的氧化性强于FeO |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
解题方法
3 . 下列离子方程式正确的是
| A.FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| B.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
C.铜与浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
D.碳酸氢铵与足量的NaOH溶液反应:HCO +OH-=CO2↑+H2O +OH-=CO2↑+H2O |
您最近一年使用:0次
4 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水的处理。工业上制备高铁酸钠(Na2FeO4)的一种方法的化学原理可用离子方程式表示为:ClO-+Fe3++OH-= +Cl-+H2O(未配平)。下列说法中不正确的是
+Cl-+H2O(未配平)。下列说法中不正确的是
 +Cl-+H2O(未配平)。下列说法中不正确的是
+Cl-+H2O(未配平)。下列说法中不正确的是A. 是氧化产物 是氧化产物 |
| B.Na2FeO4中铁元素的化合价为+6价 |
| C.每生成1molNa2FeO4,反应转移6mol电子 |
D.ClO-的氧化性强于 |
您最近一年使用:0次
名校
5 . 我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。下列说法错误的是
| A.氧化剂是KNO3和S |
| B.木炭被氧化 |
| C.每生成1mol的CO2转移8NA个电子 |
| D.KNO3的氧化性强于CO2 |
您最近一年使用:0次
2024-03-12更新
|
87次组卷
|
2卷引用:贵州省瓮安中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
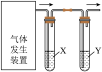
6 . 实验室用如图装置完成下表所列的四个实验,不能达到实验目的的是
| 实验装置 | 选项 | 实验目的 | 试剂X | 试剂Y |
| A | 验证电石与饱和食盐水反应生成的乙炔的性质 | CuSO4溶液 | KMnO4溶液 |
| B | 检验CH3CH2Br消去反应后的气体有机产物 | 水 | KMnO4溶液 | |
| C | 检验CH3CH2OH消去反应后的气体有机产物 | NaOH溶液 | 溴水 | |
| D | 验证氧化性Cl2>Br2>I2 | NaBr溶液 | 淀粉-KI溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-19更新
|
342次组卷
|
2卷引用:河南省济源一中2022-2023学年高二下学期5月月考化学试题
名校
7 . 下列实验操作、现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 向足量NaBr溶液中通入少量氯气,再加入淀粉KI溶液 | 溶液先变橙色,后变为蓝色 | 氧化性:Cl2>Br2>I2 |
| B | 取适量NaHCO3固体于试管中,滴入少量水并用温度计检测 | 试管内温度上升,NaHCO3结块变为晶体 | NaHCO3溶于水放热 |
| C | 向AlCl3溶液中逐滴加入稀氨水至过量 | 产生白色沉淀,并逐渐增多,后慢慢溶解 | 碱性:NH3∙H2O>Al(OH)3 |
| D | 取适量浓硝酸于试管中,将灼热的木炭插入试管 | 产生红棕色气体 | 浓硝酸与炭反应产生NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-13更新
|
235次组卷
|
3卷引用:山东省淄博市沂源县第一中学2022-2023学年高一下学期第二次月考化学试题
名校
8 . 2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑧中,金属性最强的是___________ (填元素符号)。
(2)元素⑦的原子结构示意图是___________ 。
(3)比较元素②、③的最高价氧化物对应水化物的酸性:___________ (填化学式)。说明你判断的理由:___________ 。
(4)主族元素砷(As)的部分信息如图所示。

下列说法正确的是___________ (填序号)。
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)②⑥两种元素以原子个数比1:1形成的一种化合物,是一种重要的高温耐磨材料。该物质中,②元素显___________ (填“正”或“负”)化合价,从原子结构角度解释原因是___________ 。
(6)与⑧同主族的元素溴和碘可以发生下列置换反应:Br2+2I-=2Br-+I2,I2+2BrO =2IO
=2IO +Br2,这两个置换反应矛盾吗?简述理由
+Br2,这两个置换反应矛盾吗?简述理由___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ||||||||
(1)元素①~⑧中,金属性最强的是
(2)元素⑦的原子结构示意图是
(3)比较元素②、③的最高价氧化物对应水化物的酸性:
(4)主族元素砷(As)的部分信息如图所示。

下列说法正确的是
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)②⑥两种元素以原子个数比1:1形成的一种化合物,是一种重要的高温耐磨材料。该物质中,②元素显
(6)与⑧同主族的元素溴和碘可以发生下列置换反应:Br2+2I-=2Br-+I2,I2+2BrO
 =2IO
=2IO +Br2,这两个置换反应矛盾吗?简述理由
+Br2,这两个置换反应矛盾吗?简述理由
您最近一年使用:0次
名校
9 . 废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH 完全转化为N2,该反应可表示为2NH
完全转化为N2,该反应可表示为2NH +3ClO-=N2+3Cl-+2H++3H2O。下列说法中,不正确的是
+3ClO-=N2+3Cl-+2H++3H2O。下列说法中,不正确的是
 完全转化为N2,该反应可表示为2NH
完全转化为N2,该反应可表示为2NH +3ClO-=N2+3Cl-+2H++3H2O。下列说法中,不正确的是
+3ClO-=N2+3Cl-+2H++3H2O。下列说法中,不正确的是| A.反应中氮元素被氧化,氯元素被还原 |
B.还原性NH >Cl- >Cl- |
| C.反应中每生成1molN2,转移6mol电子 |
| D.经此法处理过的废水可以直接排放 |
您最近一年使用:0次
名校
解题方法
10 . 浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是


| A.对比①和②可以说明还原性:Br->Cl- |
| B.②中试管口白雾是盐酸小液滴,说明酸性:H2SO4>HCl |
| C.③中浓H2SO4被还原成SO2 |
| D.对比①和③可以说明还原性:SO2>Br2 |
您最近一年使用:0次