名校
解题方法
1 . 下列离子方程式书写正确的是
A.碳酸氢铵稀溶液中加入足量烧碱溶液:HCO +NH +NH +2OH-=CO +2OH-=CO +NH3•H2O+H2O +NH3•H2O+H2O |
| B.向FeI2溶液中通入等物质的量的Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+2Cl- |
| C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
D.明矾溶液中滴入Ba(OH)2溶液使SO 恰好完全沉淀:2Ba2++3OH-+Al3++2SO 恰好完全沉淀:2Ba2++3OH-+Al3++2SO =2BaSO4↓+Al(OH)3↓ =2BaSO4↓+Al(OH)3↓ |
您最近一年使用:0次
名校
解题方法
2 . 下列反应的离子方程式正确的是
A.水杨酸与过量碳酸钠溶液反应:2 + +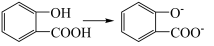 +2 +2 |
B.向碘化亚铁溶液中滴加少量稀硝酸: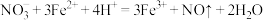 |
C.Mg(HCO3)2溶液中加足量的烧碱溶液: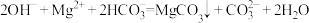 |
D.二元弱酸亚磷酸(H3PO3)溶液中滴加少量的NaOH溶液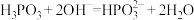 |
您最近一年使用:0次
2023-08-12更新
|
507次组卷
|
4卷引用:浙江省金丽衢十二校2022-2023学年高三第一次联考化学试题
3 . 下列根据实验操作、现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有少量酸性KMnO4溶液的试管中滴加足量的双氧水 | 溶液的紫红色逐渐褪去且有气泡产生 | 氧化性:KMnO4>H2O2 |
| B | 将Cl2通过装有湿润有色布条的集气瓶 | 有色布条褪色 | 说明Cl2具有漂白性 |
| C | 常温下,向两支装有等物质的量AgCl、AgI的试管中分别滴加足量等体积等浓度的氨水 | AgCl溶解而AgI不溶解 | 常温下,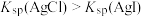 |
| D | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列离子方程式正确的是
A.Na2S2O3溶液中滴加稀硝酸:S2O +2H+ = S↓+SO2↑+H2O +2H+ = S↓+SO2↑+H2O |
B.苯酚钠溶液中通入少量 CO2:2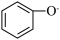 + CO2+ H2O→2 + CO2+ H2O→2 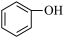 + CO + CO |
C.小苏打溶液与明矾溶液混合:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
| D.向含 4 mol FeI2的溶液中通入5mol的Cl2:4Fe2++6I-+5Cl2=4Fe3++3I2+10Cl- |
您最近一年使用:0次
解题方法
5 . 下列离子方程式正确的是
A.用醋酸除去水垢: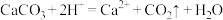 |
B.向 溶液中加过量的 溶液中加过量的 溶液: 溶液: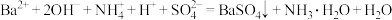 |
C.向饱和 溶液中通入过量 溶液中通入过量 : :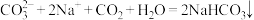 |
D.1mol  通入含1mol 通入含1mol  的溶液中: 的溶液中: |
您最近一年使用:0次
解题方法
6 . 二氟化氧( )可用作极强的氧化剂和氟化剂。已知:①
)可用作极强的氧化剂和氟化剂。已知:① (NaOH溶液的浓度为2%),②
(NaOH溶液的浓度为2%),② 。下列说法错误的是
。下列说法错误的是
 )可用作极强的氧化剂和氟化剂。已知:①
)可用作极强的氧化剂和氟化剂。已知:① (NaOH溶液的浓度为2%),②
(NaOH溶液的浓度为2%),② 。下列说法错误的是
。下列说法错误的是A. 分子的空间结构呈V形 分子的空间结构呈V形 |
B.反应①中,每生成 ,转移电子4mol ,转移电子4mol |
C.反应②中, 和 和 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
D.氧化性的强弱比较: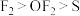 |
您最近一年使用:0次
2023-06-27更新
|
473次组卷
|
3卷引用:河北省部分高中2022-2023学年高三下学期第三次模拟考试化学试题
解题方法
7 . 某实验小组学生为探究氧化性: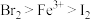 ,设计下列实验方案。
,设计下列实验方案。
【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
回答下列问题:
(1)利用 和氯水,设计实验证明氧化性:
和氯水,设计实验证明氧化性: ,实验如图所示,实验过程中,能证明氧化性:
,实验如图所示,实验过程中,能证明氧化性: 的现象是
的现象是_____ ,有关反应的离子方程式为_____ 。

(2)利用 的
的 溶液和
溶液和 的
的 溶液,不用任何试剂证明氧化性:
溶液,不用任何试剂证明氧化性: ,
, 溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
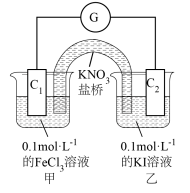
①通过外电路中电流方向:_____ (用 和
和 表示),可证明氧化性:
表示),可证明氧化性: 。
。
②也可通过甲池中颜色变化证明,甲池中颜色变化为_____ 。
(3)有同学认为还可以通过电解反应来证明氧化性: ,为此设计了如下实验:利用惰性电极电解
,为此设计了如下实验:利用惰性电极电解 的
的 溶液,探究外界条件对电极反应产物的影响,实验数据如下表所示:
溶液,探究外界条件对电极反应产物的影响,实验数据如下表所示:
①实验1中,阳极反应式是_____ ,阴极反应式为_____ 。
②实验1、3调节溶液的 宜选用
宜选用_____ (填“硝酸”或“硫酸”)。
③由实验1、2的现象可得出的结论为_____ ;由实验1、3可得出的结论为_____ 。
 ,设计下列实验方案。
,设计下列实验方案。【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
| 氧化还原电对(氧化型/还原型) | 电极反应式(氧化型 还原型) 还原型) | 电极电势 |
 / / | 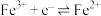 | 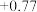 |
 / / |  | 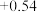 |
 / / |  | 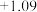 |
(1)利用
 和氯水,设计实验证明氧化性:
和氯水,设计实验证明氧化性: ,实验如图所示,实验过程中,能证明氧化性:
,实验如图所示,实验过程中,能证明氧化性: 的现象是
的现象是
(2)利用
 的
的 溶液和
溶液和 的
的 溶液,不用任何试剂证明氧化性:
溶液,不用任何试剂证明氧化性: ,
, 溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
①通过外电路中电流方向:
 和
和 表示),可证明氧化性:
表示),可证明氧化性: 。
。②也可通过甲池中颜色变化证明,甲池中颜色变化为
(3)有同学认为还可以通过电解反应来证明氧化性:
 ,为此设计了如下实验:利用惰性电极电解
,为此设计了如下实验:利用惰性电极电解 的
的 溶液,探究外界条件对电极反应产物的影响,实验数据如下表所示:
溶液,探究外界条件对电极反应产物的影响,实验数据如下表所示:| 实验 | 电压 |  | 阳极现象 | 阴极现象 |
| 实验1 | 1.5 | 5.5 | 滴加淀粉溶液显蓝色,滴加 溶液不显红色 溶液不显红色 | 无气泡,银白色金属析出 |
| 实验2 | 3.0 | 5.5 | 滴加淀粉溶液显蓝色,滴加 溶液显浅红色 溶液显浅红色 | 无气泡,银白色金属析出 |
| 实验3 | 1.5 |  | 滴加淀粉溶液显蓝色,滴加 溶液不显红色 溶液不显红色 | 较多气泡,极少量金属析出 |
②实验1、3调节溶液的
 宜选用
宜选用③由实验1、2的现象可得出的结论为
您最近一年使用:0次
名校
8 . 下列实验的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案设计 | 实验现象和结论 |
| A | 检验未知溶液中是否含有铵盐 | 取一定量未知溶液于试管中,滴入NaOH溶液并加热,试管口放置湿润的红色石蕊试纸 | 试纸变蓝,说明溶液中一定含有铵盐 |
| B | 检验某固体试样中是否存在三价铁 | 取少量固体试样完全溶于盐酸,再滴加KSCN溶液 | 没有出现血红色,说明该固体试样中不存在三价铁 |
| C | 比较Ksp(CaSO4)与Ksp(CaCO3)的大小 | 向饱和CaSO4溶液中滴加相同浓度的Na2CO3溶液 | 产生白色沉淀,说明Ksp(CaSO4)>Ksp(CaCO3) |
| D | 探究Ag+与Fe3+氧化性的强弱 | 向Fe(NO3)2和KSCN 的混合溶液中滴加酸化的AgNO3溶液 | 溶液变红,说明氧化性: Ag+>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用铂丝蘸取某溶液进行焰色反应 | 火焰呈黄色 | 溶液为钠盐溶液 |
B | 取少量溶液于试管中,先加入BaCl2溶液,再滴加稀盐酸, | 产生的白色沉淀不溶解 | 溶液中含 |
C | 将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡静置 | 溶液分层,下层呈紫色 | 还原性: Cl-<I- |
D | 取少量溶液于试管中,滴加几滴新制氯水,振荡,加入KSCN溶液 | 溶液变红色 | 溶液中含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-18更新
|
576次组卷
|
2卷引用:四川省绵阳南山中学2023届高三下学期高考仿真考试理综化学试题
解题方法
10 . 实验小组制备高铁酸钾( K2FeO4 )并进行相关探究。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是_____________________________________ 。
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、______ 。
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是_________ (写一条)。
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
①实验i中产生的“黄绿色气体”中,除含有Cl2,还可能含有____________________ ( 填化学式)。
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:__________________ 。
③能证明K2FeO4氧化了Cl-的实验是____ (填“ i”“ii” “iii”或“iv”)。
④资料表明,酸性溶液中的氧化性 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________ 。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
实验方案与现象 | |
i | 取适量C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2 |
ii | 取少量a,滴加淀粉KI溶液,无明显现象 |
iii | |
iv | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液 b,取少量b,滴加盐酸,有Cl2产生 |
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:
③能证明K2FeO4氧化了Cl-的实验是
④资料表明,酸性溶液中的氧化性
 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次



