名校
解题方法
1 . 重铬酸钾( )在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为
)在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为 ,还含杂质
,还含杂质 )为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
)为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
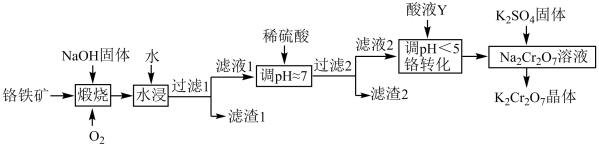
回答下列问题:
(1)基态Cr原子的未成对电子数为_______ 。二氧化硅比二氧化碳熔点高得多的最主要原因是_______ 。
(2)煅烧铬铁矿后生成 和
和 等,已知
等,已知 遇水强烈水解,生成红褐色沉淀,
遇水强烈水解,生成红褐色沉淀, 水解的离子方程式为
水解的离子方程式为_______ ;滤液1中的阴离子主要有 、
、_______ 。
(3)流程中若省去 这一操作,产品中可能含有的杂质是
这一操作,产品中可能含有的杂质是_______ 。
(4)结合离子方程式,从化学平衡移动的角度分析加入酸液Y的作用:_______ 。
(5)由于 是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含
是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含 酸性废水需要进行处理,可用焦亚硫酸钠(
酸性废水需要进行处理,可用焦亚硫酸钠( )将
)将 转化为毒性较低的
转化为毒性较低的 ,室温下再调节溶液的pH,生成
,室温下再调节溶液的pH,生成 沉淀,分离出污泥,保证废水中
沉淀,分离出污泥,保证废水中 的质量浓度小于
的质量浓度小于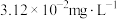 。已知室温下,
。已知室温下,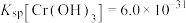 。
。
① 参加反应的离子方程式为
参加反应的离子方程式为_______ 。
②溶液的pH至少要大于_______ 。
 )在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为
)在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为 ,还含杂质
,还含杂质 )为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
)为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
回答下列问题:
(1)基态Cr原子的未成对电子数为
(2)煅烧铬铁矿后生成
 和
和 等,已知
等,已知 遇水强烈水解,生成红褐色沉淀,
遇水强烈水解,生成红褐色沉淀, 水解的离子方程式为
水解的离子方程式为 、
、(3)流程中若省去
 这一操作,产品中可能含有的杂质是
这一操作,产品中可能含有的杂质是(4)结合离子方程式,从化学平衡移动的角度分析加入酸液Y的作用:
(5)由于
 是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含
是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含 酸性废水需要进行处理,可用焦亚硫酸钠(
酸性废水需要进行处理,可用焦亚硫酸钠( )将
)将 转化为毒性较低的
转化为毒性较低的 ,室温下再调节溶液的pH,生成
,室温下再调节溶液的pH,生成 沉淀,分离出污泥,保证废水中
沉淀,分离出污泥,保证废水中 的质量浓度小于
的质量浓度小于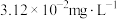 。已知室温下,
。已知室温下,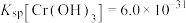 。
。①
 参加反应的离子方程式为
参加反应的离子方程式为②溶液的pH至少要大于
您最近一年使用:0次
2023-02-17更新
|
354次组卷
|
4卷引用:湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题
湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题湖南省名校联盟2022-2023学年高三下学期2月联考化学试题(已下线)云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题
名校
2 . 碳、硅、锗、锡、铅属于同一主族元素,其单质及化合物具有重要的用途。
(1)铅蓄电池是最早使用的充电电池,其构造示意图如图所示,放电时的离子反应方程式为PbO2+Pb+4H++2 =2PbSO4+2H2O。该电池的负极为
=2PbSO4+2H2O。该电池的负极为_______ ,电池放电时正极质量将_______ 。(填“增大”、“减小”或“不变”)

(2)PbO2可发生如图所示的转化:

①写出“还原”反应的离子方程式:__________ ;
②写出“复分解”反应的化学方程式:___________ 。
(3)1400℃~1450℃时,石英、焦炭和氮气可反应生成耐高温、硬度大的化合物X,该反应的化学方程式为3SiO2+6C+2N2 X+6CO。
X+6CO。
①X的化学式为_______ 。
②下列措施不 能提高该反应速率的是_______ (填字母)。
a.将石英和焦炭充分混合 b.增大N2的浓度 c.将粉末状石英换成块状石英
(4)甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。在2L容器中充入1molCO2和3moH2的混合气体,反应10min后,气体的总物质的量变为原来的75%。则0~10min内,H2的平均反应速率为_______ 。
(1)铅蓄电池是最早使用的充电电池,其构造示意图如图所示,放电时的离子反应方程式为PbO2+Pb+4H++2
 =2PbSO4+2H2O。该电池的负极为
=2PbSO4+2H2O。该电池的负极为
(2)PbO2可发生如图所示的转化:

①写出“还原”反应的离子方程式:
②写出“复分解”反应的化学方程式:
(3)1400℃~1450℃时,石英、焦炭和氮气可反应生成耐高温、硬度大的化合物X,该反应的化学方程式为3SiO2+6C+2N2
 X+6CO。
X+6CO。①X的化学式为
②下列措施
a.将石英和焦炭充分混合 b.增大N2的浓度 c.将粉末状石英换成块状石英
(4)甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。在2L容器中充入1molCO2和3moH2的混合气体,反应10min后,气体的总物质的量变为原来的75%。则0~10min内,H2的平均反应速率为
您最近一年使用:0次
2021-05-03更新
|
286次组卷
|
2卷引用:湖南省岳阳临湘市2020-2021学年高一下学期期末考试化学试题



