名校
解题方法
1 . 下列过程中的化学反应,相应的离子方程式正确的是
A.澄清石灰水中滴加少量 溶液: 溶液: |
B.用银氨溶液检验乙醛中的醛基: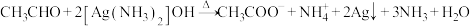 |
C.铅酸蓄电池充、放电原理: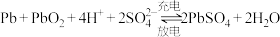 |
D.过量铁粉加入稀硝酸中: |
您最近一年使用:0次
2024-03-03更新
|
145次组卷
|
2卷引用:山东省菏泽市东明县第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
2 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
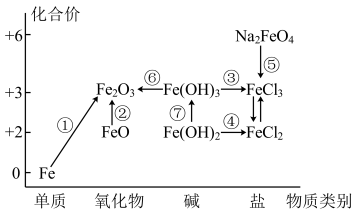
请回答以下问题:
(1)Na2FeO4中Fe的化合价为_______ 。
(2)Fe2O3是否为碱性氧化物_______ (填是或否),理由:_______ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______ 。
(4)已知Na2FeO4在强碱溶液中稳定存在,pH越小稳定性越差;则制备Na2FeO4时需要在_______ (填“酸性”“碱性”或“中性”)环境中进行;Na2FeO4也可以作为净水剂,能与水反应生成具有吸附性的Fe(OH)3胶体,写出其中离子方程式:_______ 。其中检验溶液中Fe3+的试剂是_______ 。

请回答以下问题:
(1)Na2FeO4中Fe的化合价为
(2)Fe2O3是否为碱性氧化物
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)已知Na2FeO4在强碱溶液中稳定存在,pH越小稳定性越差;则制备Na2FeO4时需要在
您最近一年使用:0次
3 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质间的转化及其定量关系。图中字母代表常见的含氯元素的物质,b、e均为钠盐。下列说法正确的是


| A.a、d、f都属于一元强酸 |
| B.c、d均具有强氧化性和漂白性 |
C.的转化中,每消耗1mol c转移 个电子 个电子 |
D.b、e在一定条件下反应生成c时,物质的量之比 |
您最近一年使用:0次
4 . 硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图所示:

步骤①的目的是去除废铁屑表面的油污。回答下列问题:
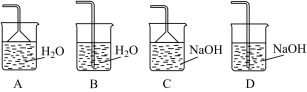
(1)步骤②需要加热的目的是_______ ,温度保持80~95 ℃,采用的合适加热方式是_______ 。铁屑中含有少量硫化物,反应产生的硫化氢气体需要净化处理,合适的装置为_______ (填标号)。
(2)步骤③中选用足量的H2O2,理由是_______ 。
(3)步骤⑤的具体实验操作有_______ ,经干燥得到硫酸铁铵晶体样品。将硫酸铁铵晶体样品加热到150 ℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_______ 。

步骤①的目的是去除废铁屑表面的油污。回答下列问题:
(1)步骤②需要加热的目的是

(2)步骤③中选用足量的H2O2,理由是
(3)步骤⑤的具体实验操作有
您最近一年使用:0次
名校
解题方法
5 . (1) S2O 可以与Fe2+反应制备Fe2O3纳米颗粒。
可以与Fe2+反应制备Fe2O3纳米颗粒。
①若S2O 与Fe2+的物质的量之比为1:2,配平该反应的离子方程式:
与Fe2+的物质的量之比为1:2,配平该反应的离子方程式:
___ Fe2++___ S2O +
+___ H2O2+___ OH- = ___ Fe2O3+___ S2O +
+___ H2O
②下列关于该反应的说法中正确的是______ (填序号)。
A 该反应中S2O 表现了氧化性
表现了氧化性
B 已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C 该反应中H2O2作氧化剂
(2)人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
_____ Cu2S+____ Fe3++____ H2O 
____ Cu2++____ Fe2++___ ( ) +____ SO
(3)书写下列反应的热化学方程式: 1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量;_________ 。
 可以与Fe2+反应制备Fe2O3纳米颗粒。
可以与Fe2+反应制备Fe2O3纳米颗粒。①若S2O
 与Fe2+的物质的量之比为1:2,配平该反应的离子方程式:
与Fe2+的物质的量之比为1:2,配平该反应的离子方程式: +
+ +
+②下列关于该反应的说法中正确的是
A 该反应中S2O
 表现了氧化性
表现了氧化性B 已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C 该反应中H2O2作氧化剂
(2)人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:


(3)书写下列反应的热化学方程式: 1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量;
您最近一年使用:0次
6 . 已知某一反应体系有反应物和生成物共三种物质:FeCl3、FeCl2、Fe。完成下列问题:
(1)该反应中的还原产物的化学式是________ ,氧化产物的化学式是________ 。
(2)该反应的离子方程式为____________________________________________ 。
(3)标出该反应中电子转移的方向和数目________________________________ 。
(4)如反应转移了0.3 mol电子,则________ (填“溶解”或“生成”)的铁的质量为________ 。
(1)该反应中的还原产物的化学式是
(2)该反应的离子方程式为
(3)标出该反应中电子转移的方向和数目
(4)如反应转移了0.3 mol电子,则
您最近一年使用:0次
2016-12-09更新
|
349次组卷
|
4卷引用:2015-2016学年山东省淄博市高青一中高一下收心考试化学试卷
2015-2016学年山东省淄博市高青一中高一下收心考试化学试卷(已下线)【走进新高考】(人教版必修一)第二章 化学物质及其变化 单元练习01江西省南昌市进贤一中2020-2021学年高一上学期第二次月考化学试题四川省雅安市汉源县2023-2024学年高一上学期第一次联测化学试题



