名校
1 . 回答下列问题:
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生___________ 反应,说明亚硝酸钠具有___________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有___________ 性。
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是___________ ,还原剂是___________ ,反应中被氧化的氮原子与未被氧化的氮原子物质的量之比为___________ 。
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为___________ 。
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为
您最近一年使用:0次
2 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_______ (填“SiO2”或“Si”);
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为_______ mol •L-1• min-1。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO 2CO2 +
2CO2 + _______ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO
 2CO2 +
2CO2 +
您最近一年使用:0次
3 . 镁及其化合物在现代工业、国防建设中有着广泛的应用。回答下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的___________ ,还生成少量的___________ (填化学式)。
(2)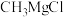 是一种重要的有机合成剂,其中镁的化合价为
是一种重要的有机合成剂,其中镁的化合价为___________ ,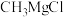 水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:
水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:___________ 。
(3)现有一块 合金,将其置于烧杯中。若加入
合金,将其置于烧杯中。若加入 溶液,恰好完全反应生成
溶液,恰好完全反应生成 。若加入
。若加入 少量盐酸,则生成
少量盐酸,则生成 。计算
。计算
___________  。
。
(4) 是常用的阻燃材料。以白云石(
是常用的阻燃材料。以白云石( ,不考虑杂质)为原料制备
,不考虑杂质)为原料制备 和
和 工艺流程如下:
工艺流程如下:

①相同条件下,溶解度:
___________ (填“>”或“<”) 。
。
②“煅烧”时称取 白云石,高温加热到质量不再变化,收集到的
白云石,高温加热到质量不再变化,收集到的 为
为 (标准状况下),若工艺中不考虑
(标准状况下),若工艺中不考虑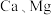 损失,则
损失,则 和
和 的质量分别为
的质量分别为___________ 、___________ 。
(1)单质镁在空气中燃烧的主要产物是白色的
(2)
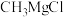 是一种重要的有机合成剂,其中镁的化合价为
是一种重要的有机合成剂,其中镁的化合价为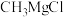 水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:
水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:(3)现有一块
 合金,将其置于烧杯中。若加入
合金,将其置于烧杯中。若加入 溶液,恰好完全反应生成
溶液,恰好完全反应生成 。若加入
。若加入 少量盐酸,则生成
少量盐酸,则生成 。计算
。计算
 。
。(4)
 是常用的阻燃材料。以白云石(
是常用的阻燃材料。以白云石( ,不考虑杂质)为原料制备
,不考虑杂质)为原料制备 和
和 工艺流程如下:
工艺流程如下:
①相同条件下,溶解度:

 。
。②“煅烧”时称取
 白云石,高温加热到质量不再变化,收集到的
白云石,高温加热到质量不再变化,收集到的 为
为 (标准状况下),若工艺中不考虑
(标准状况下),若工艺中不考虑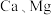 损失,则
损失,则 和
和 的质量分别为
的质量分别为
您最近一年使用:0次
2022-10-06更新
|
89次组卷
|
2卷引用:湖南省邵阳市部分校2022-2023学年高三上学期第一次联考化学试题
名校
4 . 碳、硅、锗、锡、铅属于同一主族元素,其单质及化合物具有重要的用途。
(1)铅蓄电池是最早使用的充电电池,其构造示意图如图所示,放电时的离子反应方程式为PbO2+Pb+4H++2 =2PbSO4+2H2O。该电池的负极为
=2PbSO4+2H2O。该电池的负极为_______ ,电池放电时正极质量将_______ 。(填“增大”、“减小”或“不变”)

(2)PbO2可发生如图所示的转化:

①写出“还原”反应的离子方程式:__________ ;
②写出“复分解”反应的化学方程式:___________ 。
(3)1400℃~1450℃时,石英、焦炭和氮气可反应生成耐高温、硬度大的化合物X,该反应的化学方程式为3SiO2+6C+2N2 X+6CO。
X+6CO。
①X的化学式为_______ 。
②下列措施不 能提高该反应速率的是_______ (填字母)。
a.将石英和焦炭充分混合 b.增大N2的浓度 c.将粉末状石英换成块状石英
(4)甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。在2L容器中充入1molCO2和3moH2的混合气体,反应10min后,气体的总物质的量变为原来的75%。则0~10min内,H2的平均反应速率为_______ 。
(1)铅蓄电池是最早使用的充电电池,其构造示意图如图所示,放电时的离子反应方程式为PbO2+Pb+4H++2
 =2PbSO4+2H2O。该电池的负极为
=2PbSO4+2H2O。该电池的负极为
(2)PbO2可发生如图所示的转化:

①写出“还原”反应的离子方程式:
②写出“复分解”反应的化学方程式:
(3)1400℃~1450℃时,石英、焦炭和氮气可反应生成耐高温、硬度大的化合物X,该反应的化学方程式为3SiO2+6C+2N2
 X+6CO。
X+6CO。①X的化学式为
②下列措施
a.将石英和焦炭充分混合 b.增大N2的浓度 c.将粉末状石英换成块状石英
(4)甲醇是常见的燃料电池原料,CO2催化氢化可合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。在2L容器中充入1molCO2和3moH2的混合气体,反应10min后,气体的总物质的量变为原来的75%。则0~10min内,H2的平均反应速率为
您最近一年使用:0次
2021-05-03更新
|
286次组卷
|
2卷引用:湖南省岳阳临湘市2020-2021学年高一下学期期末考试化学试题



