1 . 下图中有5种物质 、
、 、
、 、
、 、
、 ,图中相交部分“A、B、C、D”代表两种物质相互反应的产物。
,图中相交部分“A、B、C、D”代表两种物质相互反应的产物。
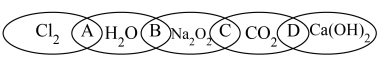
回答下列问题:
(1)5种物质中属于酸性氧化物的是___________ (填化学式,下同),属于电解质的是___________ 。
(2)产物中含有难溶电解质的是___________ (填“A”、“B”、“C”或“D”)。
(3)过去工业曾采用 与
与 溶液反应制备NaOH,写出相应的离子方程式
溶液反应制备NaOH,写出相应的离子方程式___________ ;现代工业利用电解饱和食盐水制备NaOH,同时生成两种单质 和X,写出相应的化学方程式
和X,写出相应的化学方程式___________ 。
(4)阴阳离子数目比:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
 、
、 、
、 、
、 、
、 ,图中相交部分“A、B、C、D”代表两种物质相互反应的产物。
,图中相交部分“A、B、C、D”代表两种物质相互反应的产物。
回答下列问题:
(1)5种物质中属于酸性氧化物的是
(2)产物中含有难溶电解质的是
(3)过去工业曾采用
 与
与 溶液反应制备NaOH,写出相应的离子方程式
溶液反应制备NaOH,写出相应的离子方程式 和X,写出相应的化学方程式
和X,写出相应的化学方程式(4)阴阳离子数目比:

 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
您最近一年使用:0次
2 . K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
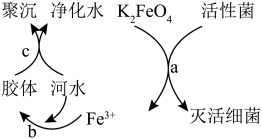
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近一年使用:0次
解题方法
3 . 根据所学知识回答下列问题:
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为__________ 。
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:__________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:
方案一:碱性条件下用 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为__________ 。
方案二:在碱性条件下,用铝粉处理,已知反应时Al与 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是__________ ,还原产物是__________ ,请写出反应的离子方程式:__________ 。
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:方案一:碱性条件下用
 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为方案二:在碱性条件下,用铝粉处理,已知反应时Al与
 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是
您最近一年使用:0次
解题方法
4 . 物质分类与转化是学习化学的基石,如图为氯及其化合物的“价-类”二维图,请正确回答下列问题:
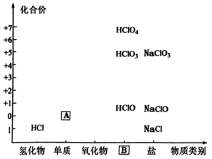
(1)填写二维图缺失的内容:化学式A__________ ;类别B__________ 。
(2)A可与热的 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式__________ 。
(3)关于盐酸与 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于__________ 反应类型(填四大基本反应类型);乙同学认为发生氧化还原反应,因为他曾经看到一篇报道称:某家庭主妇在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式__________ ,该反应从化合价角度体现了盐酸具有__________ 性。

(1)填写二维图缺失的内容:化学式A
(2)A可与热的
 浓溶液反应生成
浓溶液反应生成 和
和 ,写出反应的化学方程式
,写出反应的化学方程式(3)关于盐酸与
 反应,同学们有不同意见,甲同学认为发生反应:
反应,同学们有不同意见,甲同学认为发生反应: ,该反应属于
,该反应属于 )而发生氯气中毒事件。请写出反应方程式
)而发生氯气中毒事件。请写出反应方程式
您最近一年使用:0次
5 . 钠是一种非常活泼、具有广泛应用的金属。
(1)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(2)汽车安全气囊的气体发生剂 :可由金属钠生产。某汽车安全气囊内含
:可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时,引发 分解
分解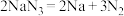 ,从而为气囊充气。用单线桥表示该反应电子转移的方向数目
,从而为气囊充气。用单线桥表示该反应电子转移的方向数目___________ 。
②产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是:
,化学方程式是:___________ 。
③ 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为:
起冷却作用时发生反应的化学方程式为:___________ 。
(3)工业通过电解NaCl生产金属钠: ,过程如图:
,过程如图:
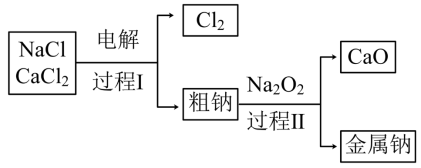
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把培点降至约580℃。
从而把培点降至约580℃。
①NaCl固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质Ca,过程Ⅱ在加热条件下除去Ca的化学方程式是:___________ 。
③过程Ⅰ中, 能发生像NaCl那样的电解反应而被消耗。但在过程1中
能发生像NaCl那样的电解反应而被消耗。但在过程1中 却不断地被重新生成,原因是:
却不断地被重新生成,原因是:___________ 。
(1)金属钠非常活泼,通常保存在
(2)汽车安全气囊的气体发生剂
 :可由金属钠生产。某汽车安全气囊内含
:可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,引发
 分解
分解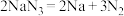 ,从而为气囊充气。用单线桥表示该反应电子转移的方向数目
,从而为气囊充气。用单线桥表示该反应电子转移的方向数目②产生的Na立即与
 发生置换反应生成
发生置换反应生成 ,化学方程式是:
,化学方程式是:③
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为:
起冷却作用时发生反应的化学方程式为:(3)工业通过电解NaCl生产金属钠:
 ,过程如图:
,过程如图:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把培点降至约580℃。
从而把培点降至约580℃。①NaCl固体加热至熔融状态,目的是
②粗钠中含有少量杂质Ca,过程Ⅱ在加热条件下除去Ca的化学方程式是:
③过程Ⅰ中,
 能发生像NaCl那样的电解反应而被消耗。但在过程1中
能发生像NaCl那样的电解反应而被消耗。但在过程1中 却不断地被重新生成,原因是:
却不断地被重新生成,原因是:
您最近一年使用:0次
名校
6 .  分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
(1)汽车燃料中一般不含氮元素,尾气中所含的 是如何产生的?请用化学方程式解释相关原因
是如何产生的?请用化学方程式解释相关原因___________ 。
(2)在含有 的酶的活化中心,亚硝酸根离子(
的酶的活化中心,亚硝酸根离子( )可转化为
)可转化为 ,写出
,写出 和
和 在酸性溶液中转化为
在酸性溶液中转化为 的离子方程式
的离子方程式___________ 。
(3)一定条件下 可转化为
可转化为 和另一种红棕色气体,方程式为
和另一种红棕色气体,方程式为___________ 。
(4)镁铁混合物 ,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下
,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下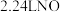 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是___________ 。
 分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
分子曾因污染空气而臭名昭著,但随着“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:(1)汽车燃料中一般不含氮元素,尾气中所含的
 是如何产生的?请用化学方程式解释相关原因
是如何产生的?请用化学方程式解释相关原因(2)在含有
 的酶的活化中心,亚硝酸根离子(
的酶的活化中心,亚硝酸根离子( )可转化为
)可转化为 ,写出
,写出 和
和 在酸性溶液中转化为
在酸性溶液中转化为 的离子方程式
的离子方程式(3)一定条件下
 可转化为
可转化为 和另一种红棕色气体,方程式为
和另一种红棕色气体,方程式为(4)镁铁混合物
 ,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下
,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下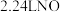 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
您最近一年使用:0次
7 . NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:___________NaNO2+___________HI=___________NO↑+___________I2+___________NaI+___________H2O。
(1)配平上述化学方程式_________ 。
(2)若有1mol的还原剂被氧化,则反应中转移电子的数目是___________ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋。进行试验,下列选项合适的是:___________(填字母)。
(4)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl能使NaNO2转化为不引起二次污染的N2,反应的离子方程式为:___________ 。
(5)①配平以下化学方程式:___________ 。
___________Al+___________NaNO3+___________NaOH=___________NaAlO2+___________N2↑+___________。
②若反应过程中转移5mole-,则生成标准状况下N2的体积为___________ L。
(1)配平上述化学方程式
(2)若有1mol的还原剂被氧化,则反应中转移电子的数目是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋。进行试验,下列选项合适的是:___________(填字母)。
| A.③⑤ | B.①②④ | C.①②⑤ | D.①③⑤ |
(5)①配平以下化学方程式:
___________Al+___________NaNO3+___________NaOH=___________NaAlO2+___________N2↑+___________。
②若反应过程中转移5mole-,则生成标准状况下N2的体积为
您最近一年使用:0次
名校
8 . 按要求完成下列填空:
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是___________ ;然后又褪色,起作用的微粒是___________ 。
(3)实验证明铜、不能在低温下与 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)过量铁粉与稀硝酸反应方程式为: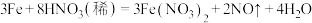 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为___________ 。当产生 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子___________  ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为___________  。
。
(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是
(3)实验证明铜、不能在低温下与
 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为(4)过量铁粉与稀硝酸反应方程式为:
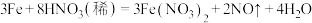 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子 ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为 。
。(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)
您最近一年使用:0次
名校
解题方法
9 . 某班同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在 溶液中需加入少量铁屑,结合化学方程式说明其目的是
溶液中需加入少量铁屑,结合化学方程式说明其目的是________ 。
(2)甲组同学取 溶液,加入几滴
溶液,加入几滴 ,再加入1滴KSCN溶液,溶液变红,说明
,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与
溶液与 反应的离子方程式为:
反应的离子方程式为:________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 溶液中先加入0.5mL煤油,再于液面下依次加入几滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴 和1滴KSCN溶液,溶液变红,煤油的作用是
和1滴KSCN溶液,溶液变红,煤油的作用是_______ 。
(4)丙组同学向 溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:
溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:_______ 。
(5)丁组同学模拟电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:_________ 。
(6)戊组同学模拟工业上用 氧化酸性
氧化酸性 废液制备
废液制备 。
。
①若酸性 废液中:
废液中: ,
,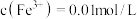 ,
,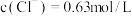 ,则该溶液的
,则该溶液的
_______ 。
②完成 氧化酸性
氧化酸性 的离子方程式:
的离子方程式:______ 。__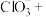 __
__ ____=___
____=___ ___
___ ____
____
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在
 溶液中需加入少量铁屑,结合化学方程式说明其目的是
溶液中需加入少量铁屑,结合化学方程式说明其目的是(2)甲组同学取
 溶液,加入几滴
溶液,加入几滴 ,再加入1滴KSCN溶液,溶液变红,说明
,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与
溶液与 反应的离子方程式为:
反应的离子方程式为:(3)乙组同学认为甲组的实验不够严谨,该组同学在
 溶液中先加入0.5mL煤油,再于液面下依次加入几滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴 和1滴KSCN溶液,溶液变红,煤油的作用是
和1滴KSCN溶液,溶液变红,煤油的作用是(4)丙组同学向
 溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:
溶液滴加氢氧化钠溶液并在空气中放置一段时间,沉淀转化的化学方程式为:(5)丁组同学模拟电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(6)戊组同学模拟工业上用
 氧化酸性
氧化酸性 废液制备
废液制备 。
。①若酸性
 废液中:
废液中: ,
,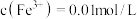 ,
,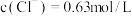 ,则该溶液的
,则该溶液的
②完成
 氧化酸性
氧化酸性 的离子方程式:
的离子方程式: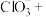 __
__ ____=___
____=___ ___
___ ____
____
您最近一年使用:0次
解题方法
10 . 某化学学习小组同学用如下实验探究 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是___________ 。
(2)乙组同学取 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:___________ 。
(3)丙组同学认为乙组的实验不够严谨,该组同学在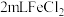 溶液中先加入
溶液中先加入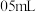 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是___________ 。
(4)丁组同学探究证实了 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式___________ 。
(5)戊组同学模拟工业上用 氧化酸性
氧化酸性  废液制备
废液制备  。
。
①若酸性 废液中:
废液中: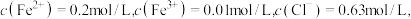 则该溶液的
则该溶液的
___________ 。
②完成 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
___________ +___________
+___________ ___________=___________
___________=___________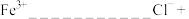 ___________。
___________。
 的性质。请回答下列问题:
的性质。请回答下列问题:(1)甲组分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在  溶液中加入少量铁屑,其目的是
溶液中加入少量铁屑,其目的是(2)乙组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴  溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将  氧化。
氧化。  溶液与氯水反应的离子方程式为:
溶液与氯水反应的离子方程式为:(3)丙组同学认为乙组的实验不够严谨,该组同学在
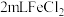 溶液中先加入
溶液中先加入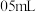 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴  溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(4)丁组同学探究证实了
 沉淀易被
沉淀易被  氧化,写出该反应的化学方程式
氧化,写出该反应的化学方程式(5)戊组同学模拟工业上用
 氧化酸性
氧化酸性  废液制备
废液制备  。
。①若酸性
 废液中:
废液中: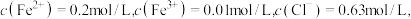 则该溶液的
则该溶液的
②完成
 氧化酸性
氧化酸性  的离子方程式 (“□ ”中填离子或分子的化学式):
的离子方程式 (“□ ”中填离子或分子的化学式):___________
 +___________
+___________ ___________=___________
___________=___________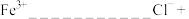 ___________。
___________。
您最近一年使用:0次



