1 . 已知R为短周期主族元素,一种白色钠盐M的组成用通式 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:
(1)若在M溶液中滴加 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为__________ ,M的俗名是__________ 。
(2)若在M溶液中滴加 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为______________ 。
(3)若将M溶液加入酸性 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是__________ ,则M溶液和酸性 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为________ ,其中还原剂是__________ 。
(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为________ ,铜粉溶解的离子方程式为____________ ,工业上,氨催化氧化可制备X,其反应的化学方程式为__________ 。
 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:(1)若在M溶液中滴加
 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为(2)若在M溶液中滴加
 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为(3)若将M溶液加入酸性
 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为
您最近半年使用:0次
解题方法
2 . 丙烯是重要的有机化合物,具有广泛应用。
Ⅰ.工业上以苯和丙烯为原料合成聚碳酸酯的生产原理如下。
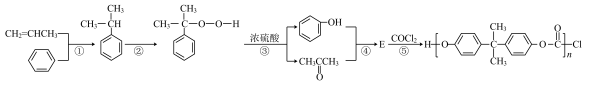
(1)丙酮与水互溶的原因是______ 。
(2)反应②的原子利用率为100%,加入的氧化剂是______ (填分子式)。
(3)蒸馏分离丙酮、苯酚前,需要除去剩余硫酸,最适宜选择______ (选填序号)。
A.NaOH B. C.
C.
(4)E的分子式为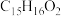 ,则其结构简式为
,则其结构简式为______ 。
Ⅱ.开发新型高效、无毒的催化剂,以丙烯为还原剂脱硝除去NO。
(5)对Mn基催化剂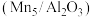 分别添加Ce、Co助剂进行催化剂性能测试后,得到NO的转化率、
分别添加Ce、Co助剂进行催化剂性能测试后,得到NO的转化率、 的选择性随温度变化曲线分别如图-1、图-2所示。
的选择性随温度变化曲线分别如图-1、图-2所示。
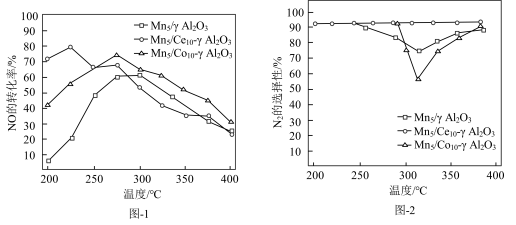
添加助剂______ (选填“Ce”、“Co”)改善催化剂的催化活性效果更加显著。
(6)研究表明催化剂添加助剂后催化活性提高的原因是形成活性 参与反应,图-3为丙烯脱硝机理。
参与反应,图-3为丙烯脱硝机理。
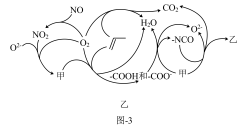
①图中,甲为______ ,乙为______ 。(用化学式表示)
②若参加反应的丙烯与NO物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为______ 。
Ⅰ.工业上以苯和丙烯为原料合成聚碳酸酯的生产原理如下。

(1)丙酮与水互溶的原因是
(2)反应②的原子利用率为100%,加入的氧化剂是
(3)蒸馏分离丙酮、苯酚前,需要除去剩余硫酸,最适宜选择
A.NaOH B.
 C.
C.
(4)E的分子式为
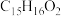 ,则其结构简式为
,则其结构简式为Ⅱ.开发新型高效、无毒的催化剂,以丙烯为还原剂脱硝除去NO。
(5)对Mn基催化剂
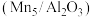 分别添加Ce、Co助剂进行催化剂性能测试后,得到NO的转化率、
分别添加Ce、Co助剂进行催化剂性能测试后,得到NO的转化率、 的选择性随温度变化曲线分别如图-1、图-2所示。
的选择性随温度变化曲线分别如图-1、图-2所示。
添加助剂
(6)研究表明催化剂添加助剂后催化活性提高的原因是形成活性
 参与反应,图-3为丙烯脱硝机理。
参与反应,图-3为丙烯脱硝机理。
①图中,甲为
②若参加反应的丙烯与NO物质的量之比为
 ,则反应的化学方程式为
,则反应的化学方程式为
您最近半年使用:0次
3 . 化合物X由三种元素组成,某学习小组做了一系列实验,流程如下图。(所有数据均为标准状况下数据)
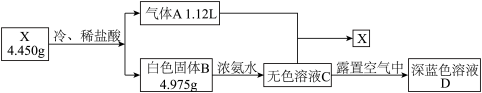
已知:气体A是一种常见的烃。B为二元化合物。
完成下列问题:
(1)写出X的化学式___________ ;A的结构简式___________
(2)C→D的离子反应方程式___________
(3)将A通入C中也能生成X,写出离子反应方程式___________
(4)设计实验验证A中含有的两种元素。___________

已知:气体A是一种常见的烃。B为二元化合物。
完成下列问题:
(1)写出X的化学式
(2)C→D的离子反应方程式
(3)将A通入C中也能生成X,写出离子反应方程式
(4)设计实验验证A中含有的两种元素。
您最近半年使用:0次
名校
解题方法
4 . 有机物A产量可衡量一个国家的石化水平,聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:

(1)A的结构简式为:_______ ;
(2)已知: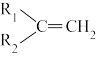
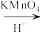
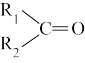 +CO2,则A与酸性高锰酸钾反应的离子方程式为
+CO2,则A与酸性高锰酸钾反应的离子方程式为_______ 。
(3)氯乙烯所含官能团为_______ 。
(4)与1,2-二氯乙烷互为同系物,比其相对分子质量多14的同分异构体有_______ 种;其中核磁共振氢谱有1种峰的分子的结构简式为_______ 。(写一种即可)
(5)反应③的化学方程式为_______ ,反应类型为_______ 。
(6)乙烯的一种同系物的键线式为 ,请用系统命名法为其命名
,请用系统命名法为其命名_______ 。

(1)A的结构简式为:
(2)已知:
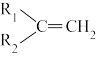
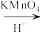
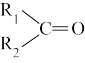 +CO2,则A与酸性高锰酸钾反应的离子方程式为
+CO2,则A与酸性高锰酸钾反应的离子方程式为(3)氯乙烯所含官能团为
(4)与1,2-二氯乙烷互为同系物,比其相对分子质量多14的同分异构体有
(5)反应③的化学方程式为
(6)乙烯的一种同系物的键线式为
 ,请用系统命名法为其命名
,请用系统命名法为其命名
您最近半年使用:0次
5 . (1)按要求写出下列反应的离子方程式:
①少量二氧化碳通入澄清石灰水_____________________________________________ 。
②硫酸氢钠与过量氢氧化钡溶液混合______________________________________ 。
③熔融状态下NaHSO4电离方程式__________________________ 。
(2)①用双线桥表示下列氧化还原反应电子转移:__________________________ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②配平下面方程式:_________ 。
KMnO4+ H2O2+ H2SO4 — K2SO4 + MnSO4 + O2↑+ H2O
①少量二氧化碳通入澄清石灰水
②硫酸氢钠与过量氢氧化钡溶液混合
③熔融状态下NaHSO4电离方程式
(2)①用双线桥表示下列氧化还原反应电子转移:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②配平下面方程式:
KMnO4+ H2O2+ H2SO4 — K2SO4 + MnSO4 + O2↑+ H2O
您最近半年使用:0次



