名校
解题方法
1 . 如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ ,体现了c的_____ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是_____ (填化学式)。
(3)将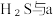 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为_____ 。
(4)配平下列反应:_____ 。
_____
(5)为防止多余的a气体污染环境,应将尾气通入_____ 溶液中;
(6)将足量的 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填字母)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀

(7)将 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为_____ 。 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:_____ 。
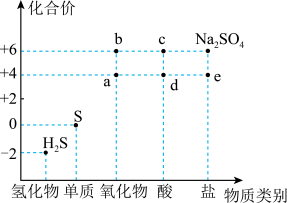
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是
(3)将
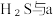 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应:
_____

(5)为防止多余的a气体污染环境,应将尾气通入
(6)将足量的
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(7)将
 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为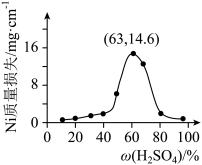
 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近半年使用:0次
解题方法
2 . 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用生成1mol氧气所转移的电子数为___________ 。
(3)次氯酸钠氧化法___________ 。
②副产品的成分为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法
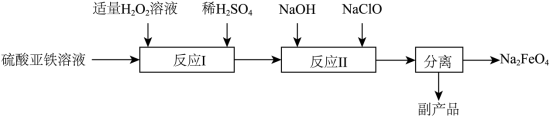
②副产品的成分为
您最近半年使用:0次
解题方法
3 . 叠氮化钠(NaN3)可用于汽车安全气囊的产气药。一种由氨基化钠(NaNH2)制备NaN3的工艺流程如图。
①钠元素位于周期表第_____ 周期_____ 族。
②NaNH2中氮元素的化合价为_____ 。
③用单线桥 标出该反应电子转移的方向和数目_____ 。
(2)NaOH的电子式为_____ ,流程中“反应”的化学方程式为_____ 。
(3)NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积为_____ L。
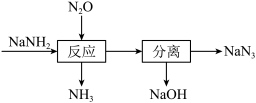
①钠元素位于周期表第
②NaNH2中氮元素的化合价为
③用
(2)NaOH的电子式为
(3)NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积为
您最近半年使用:0次
名校
4 . 氮及其化合物与生产生活及环境息息相关。请回答下列问题:
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:___________ 。
(2)硝酸与金属反应会产生氮氧化物。下列环境问题与氮的氧化物排放无关的是___________ 。
A酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式___________ ,氧化产物与还原产物的物质的量之比为___________ 。
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸(HSbF6),称为超强酸。氟锑酸可由SbF5与HF混合得到。制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是___________ (用化学方程式回答)
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:
(2)硝酸与金属反应会产生氮氧化物。下列环境问题与氮的氧化物排放无关的是
A酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸(HSbF6),称为超强酸。氟锑酸可由SbF5与HF混合得到。制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是
您最近半年使用:0次
名校
5 . N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与NO在加热和催化剂作用下生成N2O的化学方程式为___________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2 +H2O
+H2O
2NO2+2OH-= +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是___________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与NO在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为:
NO+NO2+2OH-=2
 +H2O
+H2O2NO2+2OH-=
 +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。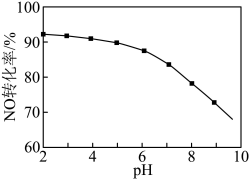
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近半年使用:0次
6 . Ⅰ.某无色透明溶液中可能大量存在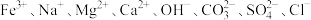 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。
(1)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
Ⅱ.次磷酸 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。
(2)写出白磷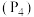 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:_______ ,反应中每消耗 ,转移的电子数为
,转移的电子数为_______ 。
(3)写出 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)工业上利用 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为_______ 。
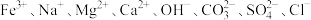 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。(1)根据上述实验现象可知,原溶液中一定存在的离子是
Ⅱ.次磷酸
 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。(2)写出白磷
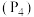 与
与 溶液反应的化学方程式:
溶液反应的化学方程式: ,转移的电子数为
,转移的电子数为(3)写出
 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(4)工业上利用
 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为
您最近半年使用:0次
名校
7 . 配平方程式并标出电子转移方向及数目___________ 。
___________ ___________
___________ ___________
___________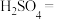 ___________
___________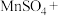 ___________
___________ ___________
___________ ___________
___________
___________
 ___________
___________ ___________
___________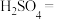 ___________
___________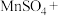 ___________
___________ ___________
___________ ___________
___________
您最近半年使用:0次
名校
8 . 近年来,利用SRB(硫酸盐还原菌)治理废水中的有机物、 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。
(1)图1表示 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:____________ 。 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。______ 。
②负极附近的 的变化:
的变化:______ (“减小”或“增大”)。
(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。
第一步________
______ ______
______ _______+______↓+______
_______+______↓+______
第二步:
 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。(1)图1表示
 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化: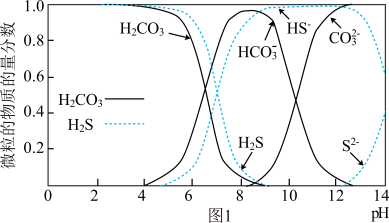
 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
②负极附近的
 的变化:
的变化:(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将
 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。第一步
______
 ______
______ _______+______↓+______
_______+______↓+______
第二步:

您最近半年使用:0次
解题方法
9 . 甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、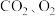 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。
(1) 属于
属于___________ (填“电解质”、“非电解质”)。
(2)从物质分类标准看,“铜绿”属于___________(填字母)。
(3)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式___________ 。
(4)古代人们高温灼烧孔雀石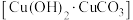 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为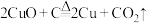 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应: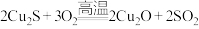 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是___________  ,第二个反应中氧化剂有
,第二个反应中氧化剂有___________ 。如把红色的 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目___________ 。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为___________ 。
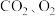 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。(1)
 属于
属于(2)从物质分类标准看,“铜绿”属于___________(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼烧孔雀石
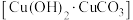 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为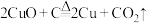 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。| A.化合反应 | B.置换反应 | C.氧化还原反应 | D.非氧化还原反应 |
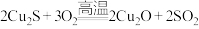 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是 ,第二个反应中氧化剂有
,第二个反应中氧化剂有 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近半年使用:0次
解题方法
10 . 试用化合价升降法配平下列化学方程式。
(1)___________Cu+___________HNO3(浓)=___________Cu(NO3)2+___________NO2↑+___________H2O,___________ ;
(2)___________NO2+___________H2O=___________HNO3+___________NO↑,___________ 。
(1)___________Cu+___________HNO3(浓)=___________Cu(NO3)2+___________NO2↑+___________H2O,
(2)___________NO2+___________H2O=___________HNO3+___________NO↑,
您最近半年使用:0次



