名校
1 . 为消除燃煤烟气中含有的 、
、 ,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
(1)向燃煤中加入适量石灰石,高温时将 气体转化为
气体转化为 的总反应化学方程式是
的总反应化学方程式是___________ 。
(2)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NO进行无害化处理。 还原NO的化学方程式是
还原NO的化学方程式是___________ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的 、NO转化为
、NO转化为 、
、 。
。
①在碱性条件下,NaClO溶液吸收烟气中 的离子方程式是
的离子方程式是___________ 。
②一定时间内,温度对硫、硝脱除率的影响曲线如图, 的脱除率高于NO,可能的原因是
的脱除率高于NO,可能的原因是___________ 。(1种即可)。 和NO的体积比为4:1,50℃时的脱除率见图,则此吸收液中烟气转化生成的
和NO的体积比为4:1,50℃时的脱除率见图,则此吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为___________ 。
 、
、 ,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
,研究者提出了若干烟气“脱硫”、“脱硝”的方法。(1)向燃煤中加入适量石灰石,高温时将
 气体转化为
气体转化为 的总反应化学方程式是
的总反应化学方程式是(2)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NO进行无害化处理。
 还原NO的化学方程式是
还原NO的化学方程式是(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的
 、NO转化为
、NO转化为 、
、 。
。①在碱性条件下,NaClO溶液吸收烟气中
 的离子方程式是
的离子方程式是②一定时间内,温度对硫、硝脱除率的影响曲线如图,
 的脱除率高于NO,可能的原因是
的脱除率高于NO,可能的原因是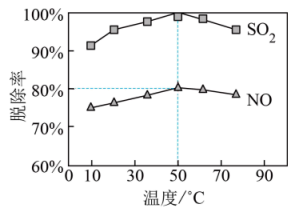
 和NO的体积比为4:1,50℃时的脱除率见图,则此吸收液中烟气转化生成的
和NO的体积比为4:1,50℃时的脱除率见图,则此吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
名校
2 . 铬及其化合物在催化、金属防腐等方面具有重要应用。催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。
(1)完成化学方程式:_____ 。
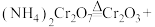 _____+_____。
_____+_____。
(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为_____ (列式表示)。_____ (用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_____ 。
(1)完成化学方程式:
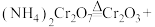 _____+_____。
_____+_____。(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图,
 过程的焓变为
过程的焓变为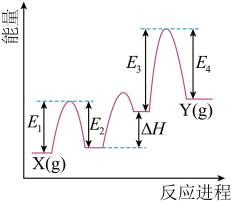
您最近半年使用:0次
名校
解题方法
3 . 硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒( ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。
(1) 的原子结构示意图为
的原子结构示意图为______________ ,其在周期表中的位置为______________ 。
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是______________ (填标号)。
A.还原性: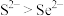
B.浓硒酸可能具有强氧化性、吸水性
C.稳定性:
D.氧化性: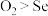
② 通入
通入 的水溶液中会生成不溶于水的
的水溶液中会生成不溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为______________ ; 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为______________ 。
(3)某混合物中硒主要以 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
ⅰ.将该混合物与浓硫酸混合焙烧,产生 、
、 的烟气
的烟气
ⅱ.用水吸收ⅰ中烟气,可得 固体
固体
已知: 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。
①可用足量 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为__________ 。
② 中
中 的化合价为
的化合价为_________ 价;焙烧时, 与浓
与浓 反应的化学方程式为
反应的化学方程式为_________________ ,理论上该反应每转移1 电子,得到的
电子,得到的 的质量为
的质量为_________ g。
 ),有抗癌、抗衰老等重要功能。请回答下列问题。
),有抗癌、抗衰老等重要功能。请回答下列问题。(1)
 的原子结构示意图为
的原子结构示意图为(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是
A.还原性:
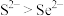
B.浓硒酸可能具有强氧化性、吸水性
C.稳定性:

D.氧化性:
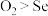
②
 通入
通入 的水溶液中会生成不溶于水的
的水溶液中会生成不溶于水的 ,该反应的化学方程式为
,该反应的化学方程式为 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为(3)某混合物中硒主要以
 和
和 的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:ⅰ.将该混合物与浓硫酸混合焙烧,产生
 、
、 的烟气
的烟气ⅱ.用水吸收ⅰ中烟气,可得
 固体
固体已知:
 的熔点为315℃,沸点为684.9℃。
的熔点为315℃,沸点为684.9℃。①可用足量
 溶液吸收烟气中的
溶液吸收烟气中的 ,二者反应生成一种盐,该盐的化学式为
,二者反应生成一种盐,该盐的化学式为②
 中
中 的化合价为
的化合价为 与浓
与浓 反应的化学方程式为
反应的化学方程式为 电子,得到的
电子,得到的 的质量为
的质量为
您最近半年使用:0次
2024-04-21更新
|
210次组卷
|
3卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
名校
4 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)湿法制备高铁酸钾的反应体系有六种微粒: 。
。
①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是______ 。
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为______ mol。
③高铁酸钾作为一种理想的水处理剂,其处理水的原理______
(2)铁明矾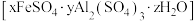 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
①称取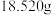 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。
②量取 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
体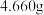 。
。
③再量取 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。
(已知 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)
①在25.00mL试样中,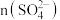
______ mol,
______ mol。
②铁明矾的化学式为______ (写出详细的解题步骤)
(1)湿法制备高铁酸钾的反应体系有六种微粒:
 。
。①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为
③高铁酸钾作为一种理想的水处理剂,其处理水的原理
(2)铁明矾
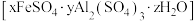 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。①称取
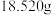 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。②量取
 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体
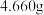 。
。③再量取
 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。(已知
 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)①在25.00mL试样中,
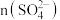

②铁明矾的化学式为
您最近半年使用:0次
名校
解题方法
5 . 氮的氧化物是大气污染物之一,用活性炭还原氮氧化物,可防止空气污染。向2L真空密闭容器中加入固体活性炭(无杂质,足量)和NO,在三种不同条件下发生反应: ,NO物质的量变化如下表所示。
,NO物质的量变化如下表所示。
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟和CO的主要原因是___________ 。
(2)与实验1相比,实验2使用了效率更高的___________ 。
(3)若实验1与实验3控制的条件仅仅是温度不同,则
___________ 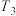 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)配平:亚硫酸钠和碘酸钾在酸性溶液中发生的化学方程式:_______ 。
___________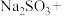 ___________
___________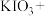 ___________
___________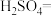 ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)该反应的过程和机理较复杂,一般认为发生以下①~④反应:
① (反应速率慢)
(反应速率慢)
② (反应速率快)
(反应速率快)
③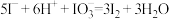 (反应速率快)
(反应速率快)
④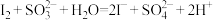 (反应速率快)
(反应速率快)
根据上述步骤推测该反应总的反应速率由___________ 反应决定(填写上述四步反应的序号)。若预先加入淀粉溶液,由上述四步反应可以看出必须在___________ 离子消耗完全时,会有淀粉变蓝的现象产生。
 ,NO物质的量变化如下表所示。
,NO物质的量变化如下表所示。| 时间(min) NO物质的量(mol) 实验序号/温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 |
实验1/ ℃ ℃ | 2.00 | 1.60 | 1.30 | 1.10 | 1.00 | 1.00 |
实验2/ ℃ ℃ | 2.00 | 1.40 | 1.00 | 1.00 | 1.00 | 1.00 |
实验3/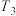 ℃ ℃ | 2.00 | 1.58 | 1.26 | 1.04 | 1.04 | 1.04 |
(2)与实验1相比,实验2使用了效率更高的
(3)若实验1与实验3控制的条件仅仅是温度不同,则

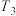 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)配平:亚硫酸钠和碘酸钾在酸性溶液中发生的化学方程式:
___________
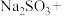 ___________
___________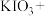 ___________
___________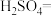 ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)该反应的过程和机理较复杂,一般认为发生以下①~④反应:
①
 (反应速率慢)
(反应速率慢)②
 (反应速率快)
(反应速率快)③
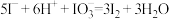 (反应速率快)
(反应速率快)④
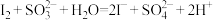 (反应速率快)
(反应速率快)根据上述步骤推测该反应总的反应速率由
您最近半年使用:0次
名校
解题方法
6 . 细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为___________ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ 。

a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
您最近半年使用:0次
2024高三下·全国·专题练习
7 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示: 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
若铬钒渣中铬的含氧酸盐为 ,则“煅烧”过程中
,则“煅烧”过程中 发生反应的化学方程式为
发生反应的化学方程式为___________ 。若在实验室中进行煅烧铬钒渣,___________ (填“能”或“不能”)用陶瓷坩埚,理由是___________ 。

 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。若铬钒渣中铬的含氧酸盐为
 ,则“煅烧”过程中
,则“煅烧”过程中 发生反应的化学方程式为
发生反应的化学方程式为
您最近半年使用:0次
名校
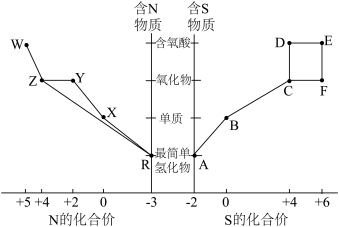
8 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题: 反应的化学方程式
反应的化学方程式______
(2)下列有关图中所示含N、S物质的叙述,正确的是______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠( ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应
(3)写出B与氢氧化钠溶液反应的离子反应方程式______
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是______ 。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: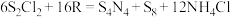 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有______ ,该反应每生成 转移电子
转移电子______ mol。
 反应的化学方程式
反应的化学方程式(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(
 ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应(3)写出B与氢氧化钠溶液反应的离子反应方程式
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: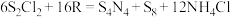 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如下图所示:
的一种制备方法如下图所示: 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 的一种制备方法如下图所示:
的一种制备方法如下图所示:
 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为
您最近半年使用:0次
2024高三下·全国·专题练习
10 . 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要化学成分为( ,还含有一定量的FeO和
,还含有一定量的FeO和 )生产BeO的一种工艺流程如下。
)生产BeO的一种工艺流程如下。 可用作聚合反应的催化剂。BeO、
可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备
与足量C在600~800℃制备 的化学方程式为
的化学方程式为_______ 。
 ,还含有一定量的FeO和
,还含有一定量的FeO和 )生产BeO的一种工艺流程如下。
)生产BeO的一种工艺流程如下。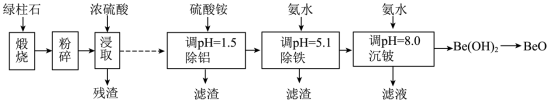
 可用作聚合反应的催化剂。BeO、
可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备
与足量C在600~800℃制备 的化学方程式为
的化学方程式为
您最近半年使用:0次



