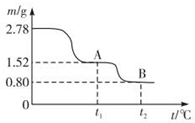
1 . 在中国古代,炼丹家以绿矾(FeSO4•7H2O为原料,放在炼丹炉中煅烧可制得绿矾油.绿矾油是一种无色粘稠液体,可用于除掉兵器上的铁锈.如图是2.78g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线.将加热产生的所有气体通入足量的BaCl2溶液.得自色沉淀1.16g.
(1)绿矾油主要成份的化学式为_________ .t1~t2.发生反应的化学方程式为_________________ .
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为_________ .
(3)以下是FeSO4•7H2O的实验室制备流理图.
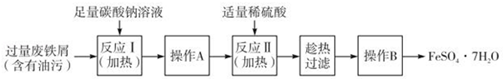
根据题意完成下列填空:
①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及____________ .
②操作A的名称为_____________ .
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为_______________ ,计算上述样品中FeSO4•7H2O的质量分数为_________ (保留两位有效数字).
(1)绿矾油主要成份的化学式为
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为
(3)以下是FeSO4•7H2O的实验室制备流理图.

根据题意完成下列填空:

①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及
②操作A的名称为
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为
您最近半年使用:0次
2 . 高铁酸钾(K2FeO4)是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。(已知:Fe3++3H2O⇌Fe(OH)3+3H+)
(1)高铁酸钾可用于杀菌消毒,是因为它具有强___________ 性。
(2)高铁酸钾被用于消毒后,产物与水形成一种分散系,其中的分散质能使得水中的悬浮杂质聚沉,方便除去,这是因为________ 。这种分散系区分于其他分散系的最本质区别是_________ 。
(3)在使用高铁酸钾时,常通过测定其纯度来判断是否变质。K2FeO4在硫酸溶液中发生如下反应:______ +______H+=_____O2↑+______Fe3++_______。
+______H+=_____O2↑+______Fe3++_______。
①完成上述离子方程式:___________ 。
②现取10.00g样品,加入稀硫酸完全反应后,共收集到0.8064L气体(已换算成标准状况)。则样品中高铁酸钾的质量分数约为___________ 。(计算结果保留到0.1%)
湿法制备高铁酸钾的流程如下图。
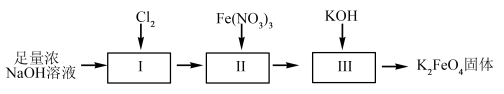
(4)过程II为碱性条件下制备高铁酸钠。写出过程II中反应的离子方程式,并标出电子转移方向和数目。___________ ,反应每生成1molCl-转移的电子数目为___________ 。
(5)湿法制备时,不同的温度下,不同质量浓度的Fe3+对K2FeO4生成率有不同影响,由下图可知工业生产中最佳条件(温度和Fe3+的质量浓度)为___________。

(1)高铁酸钾可用于杀菌消毒,是因为它具有强
(2)高铁酸钾被用于消毒后,产物与水形成一种分散系,其中的分散质能使得水中的悬浮杂质聚沉,方便除去,这是因为
(3)在使用高铁酸钾时,常通过测定其纯度来判断是否变质。K2FeO4在硫酸溶液中发生如下反应:______
 +______H+=_____O2↑+______Fe3++_______。
+______H+=_____O2↑+______Fe3++_______。①完成上述离子方程式:
②现取10.00g样品,加入稀硫酸完全反应后,共收集到0.8064L气体(已换算成标准状况)。则样品中高铁酸钾的质量分数约为
湿法制备高铁酸钾的流程如下图。

(4)过程II为碱性条件下制备高铁酸钠。写出过程II中反应的离子方程式,并标出电子转移方向和数目。
(5)湿法制备时,不同的温度下,不同质量浓度的Fe3+对K2FeO4生成率有不同影响,由下图可知工业生产中最佳条件(温度和Fe3+的质量浓度)为___________。

| A.24℃,75g∙L-1 | B.26℃,75g∙L-1 | C.28℃,75g∙L-1 | D.22℃,80g∙L-1 |
您最近半年使用:0次
解题方法
3 . 漂白粉的主要成分是次氯酸钙和氯化钙。请回答下列问题:
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):____________________________ 。
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为_____________ (假设漂白粉中的其它成份不与硝酸反应)。
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为
您最近半年使用:0次
解题方法
4 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,f、g均为含钠元素的正盐,请回答:
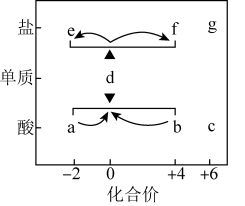
(1)当a与b混合时,可观察到的现象是___________ ;
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为___________ ;
(3)某同学利用下列装置测定空气中 的含量。
的含量。
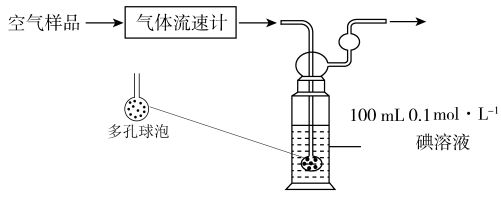
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是___________ ,该装置中 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为:___________ 。若空气流速为 ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是___________  。(用含V的最简表达式表示)
。(用含V的最简表达式表示)

(1)当a与b混合时,可观察到的现象是
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为
(3)某同学利用下列装置测定空气中
 的含量。
的含量。
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是
 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为: ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是 。(用含V的最简表达式表示)
。(用含V的最简表达式表示)
您最近半年使用:0次
2023-04-21更新
|
175次组卷
|
2卷引用:浙江省杭州市六县九校联考2022-2023学年高一下学期4月期中考试化学试题
解题方法
5 .  俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
(1)取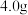 摩尔盐样品溶于适量水配成
摩尔盐样品溶于适量水配成
 溶液,该溶液中离子浓度由大到小的顺序为
溶液,该溶液中离子浓度由大到小的顺序为_______ 。检验该样品是否氧化变质的试剂是_______ 。
(2)经检验样品未变质。取
 溶液(
溶液( )于试管中,滴入上述所配
)于试管中,滴入上述所配 溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为_______ ,产生的红褐色分散系为_______ ,请结合上述过程解释产生该分散系的原因_______ 。
 俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:(1)取
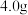 摩尔盐样品溶于适量水配成
摩尔盐样品溶于适量水配成
 溶液,该溶液中离子浓度由大到小的顺序为
溶液,该溶液中离子浓度由大到小的顺序为(2)经检验样品未变质。取

 溶液(
溶液( )于试管中,滴入上述所配
)于试管中,滴入上述所配 溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
您最近半年使用:0次
解题方法
6 . 过量排放含氮化合物对大气和水体造成环境污染,研究氮及其化合物的性质及转化,对降低含氮物质的污染有着重大的意义。
(1)水体中过量氨氮(以 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
I.
II.
III.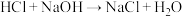
①写出用次氯酸钠去除氨氮的总反应的化学方程式:_____ 。
②从该反应历程并结合 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是_____ 。
(2)用零价铁( )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,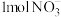 转化成
转化成 时转移
时转移____  电子。
电子。
(3)实验室模拟测定大气中 的含量,将含有
的含量,将含有 的气体样品
的气体样品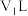 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。
①加入 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是_______ 。
②气体样品中 折合成
折合成 的含量为
的含量为_______  (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果_______ (填“偏高”“偏低”或“无影响”)。
(1)水体中过量氨氮(以
 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:I.

II.

III.
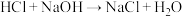
①写出用次氯酸钠去除氨氮的总反应的化学方程式:
②从该反应历程并结合
 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是(2)用零价铁(
 )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,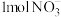 转化成
转化成 时转移
时转移 电子。
电子。(3)实验室模拟测定大气中
 的含量,将含有
的含量,将含有 的气体样品
的气体样品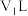 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。①加入
 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是②气体样品中
 折合成
折合成 的含量为
的含量为 (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果
您最近半年使用:0次
名校
7 . 氧化还原反应分析
(1)全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下:
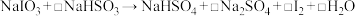 (未配平)
(未配平)
完成下列填空:
①配平上述化学方程式,并用单线桥注明电子转移的方向和数目___________ 。
②该反应实质是两步反应:① ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②___________ ;若要使碘酸钠的利用率最高,碘酸钠在第一步和第二步反应中的用量之比是___________ 。
③已知亚硫酸放置在空气中,容易变质为硫酸钠。检验亚硫酸钠固体是否氧化变质的方法是___________ 。
(2)硫酸是重要的化工原料,我国制备硫酸的原料通常用过硫化亚铁,第一步反应为:
①并用双线桥注明电子转移的方向和数目___________ 。
②该反应的氧化产物为___________ 氧化产物和还原产物的质量之比为___________ 。
(1)全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下:
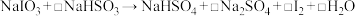 (未配平)
(未配平)完成下列填空:
①配平上述化学方程式,并用单线桥注明电子转移的方向和数目
②该反应实质是两步反应:①
 ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②③已知亚硫酸放置在空气中,容易变质为硫酸钠。检验亚硫酸钠固体是否氧化变质的方法是
(2)硫酸是重要的化工原料,我国制备硫酸的原料通常用过硫化亚铁,第一步反应为:

①并用双线桥注明电子转移的方向和数目
②该反应的氧化产物为
您最近半年使用:0次
名校
解题方法
8 . 高锰酸钾是一种强氧化剂,具有很好的消炎、杀菌、抑菌的作用,因此临床上可以用于急性皮炎、湿疹、皮肤感染等疾病的治疗。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的___________ 性。
②高锰酸钾水溶液易变质的原因是___________ 。
③高锰酸钾外用片不可与碘化物接触或并用的原因是___________ 。
(2)将 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为___________ ;当生成0.1mol还原产物时转移电子的数目为___________ 。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
| 【注意事项】 1.本品仅供外用,切忌口服。 2.本品水溶液易变质,故使用前用温水配制,并立即使用。 【药品相互作用】 不可与碘化物、有机物接触或并用,尤其是晶体。 |
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的
②高锰酸钾水溶液易变质的原因是
③高锰酸钾外用片不可与碘化物接触或并用的原因是
(2)将
 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为
您最近半年使用:0次
9 . 氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______(选填编号)。
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关系”可用下图表示。
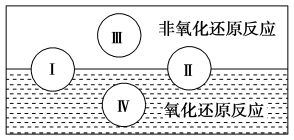
试写出有水参加且符合反应类型IV的一个化学方程式:_______ 。
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2。
①配平下列化学方程式并单线桥标明电子转移的方向和数目: _______ NaIO3+_______NaHSO3→_______
___
②该反应中,若生成1个还原产物则转移电子数目为___ 个。
(4)已知: 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
____ I-(填“>”或“<”)。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______(选填编号)。
| A.高炉炼铁 | B.食物腐败变质 | C.高温煅烧石灰石 | D.燃放烟花爆竹 |

试写出有水参加且符合反应类型IV的一个化学方程式:
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2。
①配平下列化学方程式并单线桥标明电子转移的方向和数目: _______ NaIO3+_______NaHSO3→_______

②该反应中,若生成1个还原产物则转移电子数目为
(4)已知:
 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
您最近半年使用:0次
10 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。图1是自然界中硫元素的存在示意图,图2是硫及其化合物的“价—类”二维图。
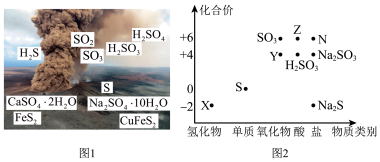
回答下列问题:
(1)图1中的 属于
属于_______ (填“纯净物”或“混合物”)。
(2)请写出图2中X和Y反应的化学方程式:_______ 。该反应中氧化产物和还原产物的质量之比为_______ 。
(3) 溶液很容易变质,请设计实验证明其已变质:
溶液很容易变质,请设计实验证明其已变质:_______ 。
(4)若N是 ,某同学设计了甲和乙两种方法制备:
,某同学设计了甲和乙两种方法制备:
甲: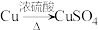
乙:
①写出甲方法反应的化学方程式:_______ 。
②甲和乙方法更合理的是_______ (填“甲”或“乙”),理由是_______ 。
(5)为测定硫酸工厂周围空气中 的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的
的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的 溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
①写出 与碘水反应的离子方程式:
与碘水反应的离子方程式:_______ 。
②空气中 的体积分数是
的体积分数是_______ (用含V、m的代数式表示)。

回答下列问题:
(1)图1中的
 属于
属于(2)请写出图2中X和Y反应的化学方程式:
(3)
 溶液很容易变质,请设计实验证明其已变质:
溶液很容易变质,请设计实验证明其已变质:(4)若N是
 ,某同学设计了甲和乙两种方法制备:
,某同学设计了甲和乙两种方法制备:甲:
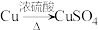
乙:

①写出甲方法反应的化学方程式:
②甲和乙方法更合理的是
(5)为测定硫酸工厂周围空气中
 的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的
的含量,进行如下实验:取VL(标准状况)空气,缓慢通入碘水,充分反应后,向溶液中加入过量的 溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。
溶液,经过滤、洗涤、干燥,称重得白色沉淀mg。①写出
 与碘水反应的离子方程式:
与碘水反应的离子方程式:②空气中
 的体积分数是
的体积分数是
您最近半年使用:0次



