解题方法
1 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,f、g均为含钠元素的正盐,请回答:
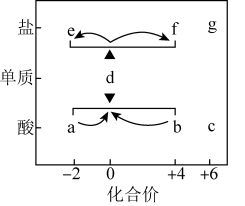
(1)当a与b混合时,可观察到的现象是___________ ;
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为___________ ;
(3)某同学利用下列装置测定空气中 的含量。
的含量。
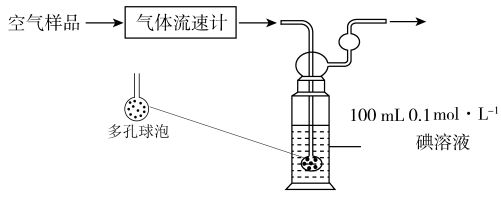
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是___________ ,该装置中 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为:___________ 。若空气流速为 ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是___________  。(用含V的最简表达式表示)
。(用含V的最简表达式表示)

(1)当a与b混合时,可观察到的现象是
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为
(3)某同学利用下列装置测定空气中
 的含量。
的含量。
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是
 与碘
与碘 溶液发生反应的化学方程式为:
溶液发生反应的化学方程式为: ,当
,当 与碘
与碘 溶液恰好完全反应时,耗时10min,则该空气样品中
溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是 。(用含V的最简表达式表示)
。(用含V的最简表达式表示)
您最近一年使用:0次
2023-04-21更新
|
177次组卷
|
2卷引用:湖北省恩施州恩高芳华高级中学2022-2023学年高二上学期期末考试化学试卷
解题方法
2 .  俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
(1)取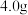 摩尔盐样品溶于适量水配成
摩尔盐样品溶于适量水配成
 溶液,该溶液中离子浓度由大到小的顺序为
溶液,该溶液中离子浓度由大到小的顺序为_______ 。检验该样品是否氧化变质的试剂是_______ 。
(2)经检验样品未变质。取
 溶液(
溶液( )于试管中,滴入上述所配
)于试管中,滴入上述所配 溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为_______ ,产生的红褐色分散系为_______ ,请结合上述过程解释产生该分散系的原因_______ 。
 俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:
俗称摩尔盐,在净水和定量分析中具有重要用途。某小组探究摩尔盐性质进行如下实验:(1)取
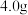 摩尔盐样品溶于适量水配成
摩尔盐样品溶于适量水配成
 溶液,该溶液中离子浓度由大到小的顺序为
溶液,该溶液中离子浓度由大到小的顺序为(2)经检验样品未变质。取

 溶液(
溶液( )于试管中,滴入上述所配
)于试管中,滴入上述所配 溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
溶液5滴,溶液立即变为棕黄色并产生大量气泡并放热,静置一会儿,颜色变为红褐色,用激光笔照射,出现丁达尔效应。溶液变为棕黄色的相应离子方程式为
您最近一年使用:0次
解题方法
3 . 过量排放含氮化合物对大气和水体造成环境污染,研究氮及其化合物的性质及转化,对降低含氮物质的污染有着重大的意义。
(1)水体中过量氨氮(以 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
I.
II.
III.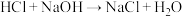
①写出用次氯酸钠去除氨氮的总反应的化学方程式:_____ 。
②从该反应历程并结合 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是_____ 。
(2)用零价铁( )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,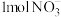 转化成
转化成 时转移
时转移____  电子。
电子。
(3)实验室模拟测定大气中 的含量,将含有
的含量,将含有 的气体样品
的气体样品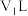 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。
①加入 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是_______ 。
②气体样品中 折合成
折合成 的含量为
的含量为_______  (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果_______ (填“偏高”“偏低”或“无影响”)。
(1)水体中过量氨氮(以
 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:I.

II.

III.
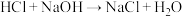
①写出用次氯酸钠去除氨氮的总反应的化学方程式:
②从该反应历程并结合
 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是(2)用零价铁(
 )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,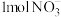 转化成
转化成 时转移
时转移 电子。
电子。(3)实验室模拟测定大气中
 的含量,将含有
的含量,将含有 的气体样品
的气体样品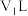 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。①加入
 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是②气体样品中
 折合成
折合成 的含量为
的含量为 (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
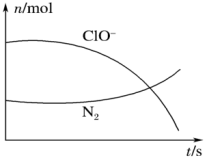
(1)某反应体系中有H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式_______ ,消耗1 mol还原剂,转移电子数为_______ 。
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是_______ ,相关反应的离子方程式是_______ 。
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为_______ ,生成的还原产物的质量为_______ g。
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式_____ 。
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
(1)某反应体系中有H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO
 + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
您最近一年使用:0次
名校
5 . 氯化铬( )是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡(
)是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡( )可制备少量氯化铬:
)可制备少量氯化铬:

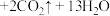 。回答下列问题:
。回答下列问题:
(1)上述反应中,还原剂是_________ ,还原产物与氧化产物的物质的量之比是________ 。
(2)该制备操作方法中,需加稍过量的乙醇,目的是________ 。
(3)制备的氯化铬粗样品利用下列滴定方法测定其纯度(杂质不参加反应):

已知:I.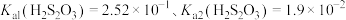 。
。
Ⅱ.上述过程发生反应: 、
、 。
。
① 标准液应盛放在
标准液应盛放在_______ 中进行滴定。
②滴定终点时,溶液由蓝色变为无色,则滴定时加入的指示剂名称是_______ 。
③滴定时,平行测定3次,平均消耗 标准液的体积为
标准液的体积为 ,则该氯化铬粗样品中
,则该氯化铬粗样品中 的纯度是
的纯度是______ (保留四位有效数字)。
 )是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡(
)是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡( )可制备少量氯化铬:
)可制备少量氯化铬:

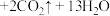 。回答下列问题:
。回答下列问题:(1)上述反应中,还原剂是
(2)该制备操作方法中,需加稍过量的乙醇,目的是
(3)制备的氯化铬粗样品利用下列滴定方法测定其纯度(杂质不参加反应):

已知:I.
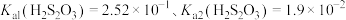 。
。Ⅱ.上述过程发生反应:
 、
、 。
。①
 标准液应盛放在
标准液应盛放在②滴定终点时,溶液由蓝色变为无色,则滴定时加入的指示剂名称是
③滴定时,平行测定3次,平均消耗
 标准液的体积为
标准液的体积为 ,则该氯化铬粗样品中
,则该氯化铬粗样品中 的纯度是
的纯度是
您最近一年使用:0次
6 . “环境就是民生,青山就是美丽、蓝天也是幸福”。回答下列问题:
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是___________ 。
②某团队设计处理流程如下:
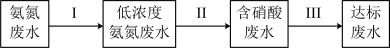
过程Ⅱ为硝化过程,在微生物的作用下实现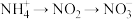 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为___________ ;
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现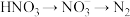 的转化,反应的化学方程式为
的转化,反应的化学方程式为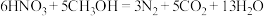 ,氧化产物是
,氧化产物是___________ ,当有1mol硝酸完全转化时,转移的电子数目为___________ 。
(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________ 。也可用NaClO2在酸性条件下氧化处理SO2,反应的离子方程式是___________ 。
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
引起雨水pH变化的主要原因是___________ (用化学方程式表示)。
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为___________ 。
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是②某团队设计处理流程如下:

过程Ⅱ为硝化过程,在微生物的作用下实现
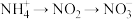 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现
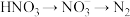 的转化,反应的化学方程式为
的转化,反应的化学方程式为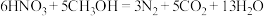 ,氧化产物是
,氧化产物是(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
| 时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为
您最近一年使用:0次
名校
7 . “7•20特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和 等都是有效的消杀试剂。
等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理______ ,标况下56L氯气完全被吸收,需要______ L 1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为______ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知: 溶液呈碱性;
溶液呈碱性; ;
;
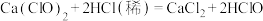
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,乙同学不同意这一观点,你认为的结论是______ 。
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是______ (从①②③中选填)。
(4)目前普遍使用 代替
代替 及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。
及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。 还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式______ 。
 等都是有效的消杀试剂。
等都是有效的消杀试剂。(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:
 溶液呈碱性;
溶液呈碱性; ;
;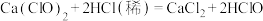
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,乙同学不同意这一观点,你认为的结论是
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用
 代替
代替 及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。
及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。 还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
136次组卷
|
2卷引用:吉林省长春市第五中学2022-2023学年高一上学期期末考试化学试题
名校
8 . Ⅰ.实验室可由软锰矿(主要成分为 )制备
)制备 ,方法如下:软锰矿和过量的固体KOH和
,方法如下:软锰矿和过量的固体KOH和 在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,
在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后, 转变为
转变为 和
和 ;滤去
;滤去 沉淀,浓缩溶液,结晶得到深紫色的针状
沉淀,浓缩溶液,结晶得到深紫色的针状 。试回答:
。试回答:
(1)软锰矿制备 的化学方程式是
的化学方程式是_______ ;
(2) 制备
制备 的离子方程式是
的离子方程式是_______ ;
(3) 能与热的经硫酸酸化的
能与热的经硫酸酸化的 反应,生成
反应,生成 和
和 等产物,该反应的化学方程式是
等产物,该反应的化学方程式是_______ 。
Ⅱ.是一种重要的无机功能材料,粗的提纯是工业生产的重要环节。某研究性学习小组设计了将粗(含有较多的MnO和 )样品转化为纯实验,其流程如下:
)样品转化为纯实验,其流程如下:

(4)第①步加稀 时,粗
时,粗 样品中的
样品中的_______ (写化学式)转化为可溶性物质。
(5)完成第②步反应的离子方程式并配平:_______
 _______+
_______+ _______=
_______=

 _______。(“1”也要填写在
_______。(“1”也要填写在 内)
内)
 )制备
)制备 ,方法如下:软锰矿和过量的固体KOH和
,方法如下:软锰矿和过量的固体KOH和 在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,
在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后, 转变为
转变为 和
和 ;滤去
;滤去 沉淀,浓缩溶液,结晶得到深紫色的针状
沉淀,浓缩溶液,结晶得到深紫色的针状 。试回答:
。试回答:(1)软锰矿制备
 的化学方程式是
的化学方程式是(2)
 制备
制备 的离子方程式是
的离子方程式是(3)
 能与热的经硫酸酸化的
能与热的经硫酸酸化的 反应,生成
反应,生成 和
和 等产物,该反应的化学方程式是
等产物,该反应的化学方程式是Ⅱ.是一种重要的无机功能材料,粗的提纯是工业生产的重要环节。某研究性学习小组设计了将粗(含有较多的MnO和
 )样品转化为纯实验,其流程如下:
)样品转化为纯实验,其流程如下:
(4)第①步加稀
 时,粗
时,粗 样品中的
样品中的(5)完成第②步反应的离子方程式并配平:
 _______+
_______+ _______=
_______=

 _______。(“1”也要填写在
_______。(“1”也要填写在 内)
内)
您最近一年使用:0次
9 . 二氧化氯( )在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
)在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
(1)制备二氧化氯:
方法1:60℃时,用潮湿的 与草酸(
与草酸( )反应制取
)反应制取 。
。
方法2:亚氯酸钠( )和稀盐酸反应,反应原理为
)和稀盐酸反应,反应原理为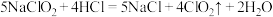 。
。
①方法1中制得的 中混有的气态杂质主要为
中混有的气态杂质主要为_____ (写分子式)。
②方法2中氧化产物和还原产物物质的量之比为______ 。
(2)利用 进行自来水消毒时,需要监测水中
进行自来水消毒时,需要监测水中 的含量,其步骤为:
的含量,其步骤为:
步骤1:量取自来水10.0mL,准确配制100mL检测液,量取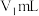 检测液于碘量瓶(
检测液于碘量瓶( )中。
)中。
步骤2:调节试样呈弱酸性,加入足量的KI,立即盖紧碘量瓶的塞子并在塞子周围加入少量水,将碘量瓶置于黑暗处静置片刻。
步骤3:加入几滴淀粉溶液于碘量瓶中,用 的
的 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液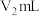 (发生的化学反应方程式:
(发生的化学反应方程式: )。
)。
①制100mL检测液,除了量筒外,还需要_____ (填字母)。
A.普通漏斗B.胶头滴管C.100mL容量瓶D.分液漏斗
②使用碘量瓶代替锥形瓶的目的是_______ (写出一点即可)。
③步骤2中发生反应的离子方程式为_______ 。
④该自来水样品中 的质量浓度为
的质量浓度为_____  (质量浓度
(质量浓度 )。
)。
 )在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
)在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:(1)制备二氧化氯:
方法1:60℃时,用潮湿的
 与草酸(
与草酸( )反应制取
)反应制取 。
。方法2:亚氯酸钠(
 )和稀盐酸反应,反应原理为
)和稀盐酸反应,反应原理为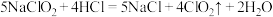 。
。①方法1中制得的
 中混有的气态杂质主要为
中混有的气态杂质主要为②方法2中氧化产物和还原产物物质的量之比为
(2)利用
 进行自来水消毒时,需要监测水中
进行自来水消毒时,需要监测水中 的含量,其步骤为:
的含量,其步骤为:步骤1:量取自来水10.0mL,准确配制100mL检测液,量取
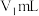 检测液于碘量瓶(
检测液于碘量瓶( )中。
)中。步骤2:调节试样呈弱酸性,加入足量的KI,立即盖紧碘量瓶的塞子并在塞子周围加入少量水,将碘量瓶置于黑暗处静置片刻。
步骤3:加入几滴淀粉溶液于碘量瓶中,用
 的
的 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液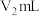 (发生的化学反应方程式:
(发生的化学反应方程式: )。
)。①制100mL检测液,除了量筒外,还需要
A.普通漏斗B.胶头滴管C.100mL容量瓶D.分液漏斗
②使用碘量瓶代替锥形瓶的目的是
③步骤2中发生反应的离子方程式为
④该自来水样品中
 的质量浓度为
的质量浓度为 (质量浓度
(质量浓度 )。
)。
您最近一年使用:0次
名校
10 . 酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_______ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_______ (用文字表达),又变为棕黄色的离子方程式是_______ 。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,配平下面方程式_______ 。
_______ +_______
+_______ +_______H+=_______Mn2++_______
+_______H+=_______Mn2++_______ +_______H2O
+_______H2O
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,配平下面方程式
_______
 +_______
+_______ +_______H+=_______Mn2++_______
+_______H+=_______Mn2++_______ +_______H2O
+_______H2O
您最近一年使用:0次



