名校
解题方法
1 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体(H2C2O4·2H2O),并验证其具有的某些性质。回答下列问题:
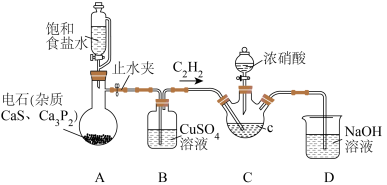
(1)仪器C的名称是_________ 。有人经分析后认为,用质量分数为70%的酒精溶液代替饱和食盐水(20℃时NaCl溶解度为36g)可获得更为平稳的气流,他得出这种结论的依据是_______ 。
(2)装置B的作用是_______________ ,若实验中使用上述酒精溶液代替食盐水,并且利用酸性KMnO4溶液检验有乙炔生成,则气体通过B后应先通入到盛有__________ 的洗气瓶,最后通入到酸性KMnO4溶液中。
(3)草酸在装置C中生成,反应的化学方程式为__________ ,装置D的作用是___________ 。
(4)待反应结束后,从C中分离出草酸晶体,然后用0.1000mol/L的酸性KMnO4溶液进行滴定以测定其纯度。
①称量3.500g草酸晶体配制100mL溶液,下 列配制操作中错误的是________ (填标号)。
a.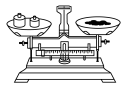 b.
b.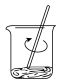 c.
c.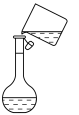 d.
d. 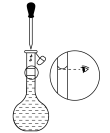
②三次平行滴定实验中消耗KMnO4溶液的体积如下表所示,其中第一次实验滴定后的液面位置如图所示。
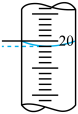
则V=_____ mL,样品中草酸晶体的质量分数为___________ 。

(1)仪器C的名称是
(2)装置B的作用是
(3)草酸在装置C中生成,反应的化学方程式为
(4)待反应结束后,从C中分离出草酸晶体,然后用0.1000mol/L的酸性KMnO4溶液进行滴定以测定其纯度。
①称量3.500g草酸晶体配制100mL溶液,下 列配制操作中错误的是
a.
 b.
b. c.
c. d.
d. 
②三次平行滴定实验中消耗KMnO4溶液的体积如下表所示,其中第一次实验滴定后的液面位置如图所示。

| 滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积/mL | ||
| 第一次 | 20.00 | 0.20 | V1 | |
| 第二次 | 20.00 | 2.56 | 23.40 | |
| 第三次 | 20.00 | 0.22 | 20.32 | |
您最近一年使用:0次
名校
2 . 亚硝酸钠( )是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于
)是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
(1) 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性 测定
测定 样品纯度,反应原理如下:
样品纯度,反应原理如下:________
__________ __________
__________ __________=__________
__________=__________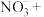 __________
__________ __________
__________ ,请将离子方程式抄写在答题卡上并完成配平。
,请将离子方程式抄写在答题卡上并完成配平。
(2)从物质分类角度来看, 是
是__________ (填字母代号)。
a.酸 b.正盐 c.酸式盐
d.碱 e.电解质 f.非电解质
(3)下列关于中毒与解毒原理中说法正确的是__________(填序号)。
(4)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列__________(填序号)反应中
表现出的性质与下列__________(填序号)反应中 表现出的性质相同。
表现出的性质相同。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式:______________________________ 。
 )是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于
)是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:(1)
 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性 测定
测定 样品纯度,反应原理如下:
样品纯度,反应原理如下:__________
 __________
__________ __________=__________
__________=__________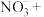 __________
__________ __________
__________ ,请将离子方程式抄写在答题卡上并完成配平。
,请将离子方程式抄写在答题卡上并完成配平。(2)从物质分类角度来看,
 是
是a.酸 b.正盐 c.酸式盐
d.碱 e.电解质 f.非电解质
(3)下列关于中毒与解毒原理中说法正确的是__________(填序号)。
| A.解毒剂美蓝应该具有氧化性 | B.中毒时亚硝酸盐发生氧化反应 |
| C.解毒时高铁血红蛋白被还原 | D.中毒过程中血红蛋白显氧化性 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列__________(填序号)反应中
表现出的性质与下列__________(填序号)反应中 表现出的性质相同。
表现出的性质相同。A. |
B. |
C.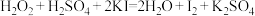 |
D. |
您最近一年使用:0次
解题方法
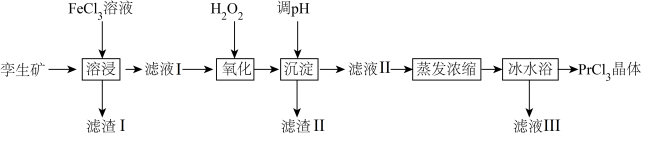
3 . 无水氯化镨(PrCl3)是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含 、
、 、
、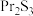 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(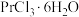 )。
)。
已知:①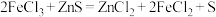 ;
;
②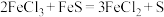 ;
;
③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
④沉淀时加入氨水逐步调节溶液的pH至6.5。此时滤渣中Ⅱ不含Pr的化合物。
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有___________ (填一种即可)。
(2)滤渣Ⅰ的主要成分为 和
和 ;
;
①写出 的一种用途:
的一种用途:___________ 。
②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:___________ 。
(3)加入 的目的是
的目的是___________ ,其发生反应的离子方程式为___________ 。
(4)滤渣Ⅱ的主要成分为___________ (填化学式)。
(5)利用表中的数据求出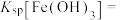
___________ 。
(6)利用电解法可以生产金属镨。先将氯化镨与工业纯KCl配成二元电解质体系( ),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
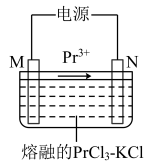
①M电极与电源的___________ (㙋“正极”或“负极”)相连。
②电池工作时,每转移 个电子,此时产生的气体的体积为
个电子,此时产生的气体的体积为___________ L(已换算成标准状况下)。
 、
、 、
、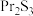 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(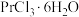 )。
)。
已知:①
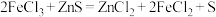 ;
;②
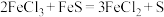 ;
;③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
| 金属离子 |  |  |  |
开始沉淀时的 | 5.4 | 2.2 | 7.5 |
沉淀完全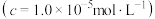 时的 时的 | 6.4 | 3.2 | 9.0 |
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有
(2)滤渣Ⅰ的主要成分为
 和
和 ;
;①写出
 的一种用途:
的一种用途:②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:
(3)加入
 的目的是
的目的是(4)滤渣Ⅱ的主要成分为
(5)利用表中的数据求出
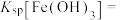
(6)利用电解法可以生产金属镨。先将氯化镨与工业纯KCl配成二元电解质体系(
 ),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
),然后置于槽内熔化,通入直流电进行电解(如图所示,两电极均为惰性电极)。
①M电极与电源的
②电池工作时,每转移
 个电子,此时产生的气体的体积为
个电子,此时产生的气体的体积为
您最近一年使用:0次



