1 . 钯(Pd)是重要的金属元素,在有机合成工业上用途广泛。自然界中,钯含量少,常伴生在其他矿藏中,如硫化镍铜矿、镍黄铁矿等。以硫化镍铜矿(含有CuS、NiS、 以及少量的Pd)为原料制备
以及少量的Pd)为原料制备 和Pd的工艺流程如下:
和Pd的工艺流程如下:

已知“酸浸”后的固体剩余物为 、PdO(不与碱反应)。回答下列问题:
、PdO(不与碱反应)。回答下列问题:
(1)“灼烧”时产生的污染性气体是_______ (填化学式)。
(2)写出“除硅”反应的离子方程式:_______ 。
(3)“系列操作”包括_______ 、过滤、洗涤、干燥。
(4)“还原”时反应还生成无污染的气体,化学方程式为_______ 。
(5)王水是按照体积比3∶1将浓盐酸和浓硝酸混合而得到的强氧化性溶液,“王水溶解”时需要加热,该过程除了生成NO外,还有 生成。写出Pd和王水反应的化学方程式:
生成。写出Pd和王水反应的化学方程式:_______ 。
(6)“氢气还原”时,参加反应的氧化剂与还原剂的物质的量之比为_______ 。
 以及少量的Pd)为原料制备
以及少量的Pd)为原料制备 和Pd的工艺流程如下:
和Pd的工艺流程如下:
已知“酸浸”后的固体剩余物为
 、PdO(不与碱反应)。回答下列问题:
、PdO(不与碱反应)。回答下列问题:(1)“灼烧”时产生的污染性气体是
(2)写出“除硅”反应的离子方程式:
(3)“系列操作”包括
(4)“还原”时反应还生成无污染的气体,化学方程式为
(5)王水是按照体积比3∶1将浓盐酸和浓硝酸混合而得到的强氧化性溶液,“王水溶解”时需要加热,该过程除了生成NO外,还有
 生成。写出Pd和王水反应的化学方程式:
生成。写出Pd和王水反应的化学方程式:(6)“氢气还原”时,参加反应的氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
解题方法
2 . 碘化钾( )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:
步骤Ⅰ:取含碘废液,调节溶液 为
为 ,加入一定量
,加入一定量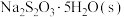 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;
步骤Ⅱ:在 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约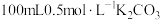 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;
步骤Ⅲ:用氢碘酸调滤液A的 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中的控温方法为___________ , 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为___________ 。
(2)步骤Ⅱ中铁粉转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)步骤Ⅲ中,仪器的名称是___________ ,现象是___________ 。
(4)产品中KI含量的测定
称取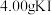 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入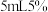 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。
①用 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是___________ ,在滴定时 溶液应盛放在
溶液应盛放在___________ (“酸式”或“碱式”)滴定管。
②样品中 的质量分数为
的质量分数为___________ 。
 )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:步骤Ⅰ:取含碘废液,调节溶液
 为
为 ,加入一定量
,加入一定量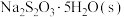 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;步骤Ⅱ:在
 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约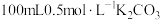 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;步骤Ⅲ:用氢碘酸调滤液A的
 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中的控温方法为
 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为(2)步骤Ⅱ中铁粉转化为
 ,该反应的化学方程式为
,该反应的化学方程式为(3)步骤Ⅲ中,仪器的名称是
(4)产品中KI含量的测定
称取
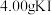 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入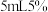 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。①用
 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是 溶液应盛放在
溶液应盛放在②样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2024-01-02更新
|
209次组卷
|
2卷引用:贵州省贵阳市2023-2024学年高三上学期11月质量检测化学试题
名校
解题方法
3 . 铍及其化合物用途广泛,以绿柱石(主要组成是3BeO·Al2O3·6SiO2, 还含少量铁元素)和方解石(主要成分是CaCO3)为原料生产铍的工艺流程如图所示:

已知:①铝铵矾[NH4Al(SO4 )2·12H2O]在不同温度下的溶解度如下表:
②Be(OH)2性质和Al(OH)3相似,是两性氢氧化物。
回答下列问题:
(1)绿柱石中Be的化合价为___________ 。“熔炼”中生成气体的电子式为 ___________ 。
(2)滤渣1中除SiO2及难溶性硅酸盐外,还含有___________ (填化学式); “转化”后,要得到铝铵矾晶体,在中学实验室中可采取的操作是___________ 、___________ 、过滤、 洗涤、干燥。
(3)加H2O2时,溶液中发生反应的离子方程式是___________ 。
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是___________ ,所得母液中的主要溶质可返回到___________ 工序循环利用。
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全___________ 。(已知:该条件下,Ksp[Be(OH)2]=1.6×10-22; 离子浓度≤1×10-5mol·L-1时,可认为离子沉淀完全。)

已知:①铝铵矾[NH4Al(SO4 )2·12H2O]在不同温度下的溶解度如下表:
| 温度/°C | 0 | 10 | 20 | 30 | 40 | 60 |
| 溶解度/g | 2.10 | 5.00 | 7.74 | 10.9 | 14.9 | 26.7 |
回答下列问题:
(1)绿柱石中Be的化合价为
(2)滤渣1中除SiO2及难溶性硅酸盐外,还含有
(3)加H2O2时,溶液中发生反应的离子方程式是
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全
您最近一年使用:0次
2023-05-20更新
|
268次组卷
|
2卷引用:贵州省贵阳市2023届高三下学期适应性考试(二)理综化学试题
名校
4 . 铜是人类最早使用的金属,在生产生活中有着重要的应用。一种以黄铜矿(主要成分为 ,含少量Fe的氧化物、
,含少量Fe的氧化物、 、Au等)为原料制备纳米Cu的工艺流程如图。
、Au等)为原料制备纳米Cu的工艺流程如图。

回答下列问题:
(1)溶浸前,要将黄铜矿粉碎过筛,目的是____________ 。
(2)溶浸后,滤渣的主要成分为______ (填化学式)。
(3)写出加入双氧水氧化时反应的离子方程式__________________ 。
(4)氨化时要确保溶液的pH不小于______ (当离子的浓度 mol⋅L
mol⋅L 时视为完全沉淀,已知常温下
时视为完全沉淀,已知常温下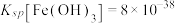 ,
, )。
)。
(5)保持其他条件相同,分别测得纳米Cu的产率随 和pH变化的曲线如图。
和pH变化的曲线如图。

生产时pH过大,纳米Cu的产率反而下降的原因可能是______ 。
(6)纳米氧化亚铜( )是一种用途广泛的光电材料,已知高温下
)是一种用途广泛的光电材料,已知高温下 比CuO稳定,解释高温下
比CuO稳定,解释高温下 比CuO更稳定的原因:
比CuO更稳定的原因:______ 。
(7) 的晶胞结构如图所示,该结构中O原子的配位数是
的晶胞结构如图所示,该结构中O原子的配位数是______ ;晶胞结构为正方体,边长为a pm,则晶体的密度为______ g·cm (用含
(用含 、a的代数式表示)。
、a的代数式表示)。

 ,含少量Fe的氧化物、
,含少量Fe的氧化物、 、Au等)为原料制备纳米Cu的工艺流程如图。
、Au等)为原料制备纳米Cu的工艺流程如图。
回答下列问题:
(1)溶浸前,要将黄铜矿粉碎过筛,目的是
(2)溶浸后,滤渣的主要成分为
(3)写出加入双氧水氧化时反应的离子方程式
(4)氨化时要确保溶液的pH不小于
 mol⋅L
mol⋅L 时视为完全沉淀,已知常温下
时视为完全沉淀,已知常温下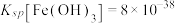 ,
, )。
)。(5)保持其他条件相同,分别测得纳米Cu的产率随
 和pH变化的曲线如图。
和pH变化的曲线如图。
生产时pH过大,纳米Cu的产率反而下降的原因可能是
(6)纳米氧化亚铜(
 )是一种用途广泛的光电材料,已知高温下
)是一种用途广泛的光电材料,已知高温下 比CuO稳定,解释高温下
比CuO稳定,解释高温下 比CuO更稳定的原因:
比CuO更稳定的原因:(7)
 的晶胞结构如图所示,该结构中O原子的配位数是
的晶胞结构如图所示,该结构中O原子的配位数是 (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
解题方法
5 . 不同价态的铜化合物用途广泛,性质多变,如 在很多有机反应中常被用作催化剂,该物质为白色固体,具有易被氧化,微溶于水,不溶于乙醇等性质,可用如图所示的装置制备。
在很多有机反应中常被用作催化剂,该物质为白色固体,具有易被氧化,微溶于水,不溶于乙醇等性质,可用如图所示的装置制备。
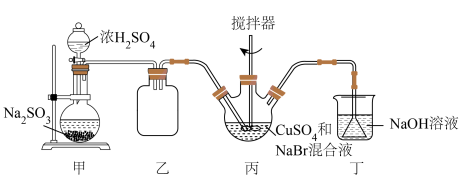
回答下列问题:
(1)制备 的反应在装置乙中进行,向其中加入一定量
的反应在装置乙中进行,向其中加入一定量 和过量
和过量 配制成的
配制成的 溶液,然后通入足量的
溶液,然后通入足量的 (部分夹持及加热装置已略去)。
(部分夹持及加热装置已略去)。
①装置乙用到的容器名称为_____ 。
②请指出上图所示的实验装置中的明显错误:_____ 。
③该反应需保持反应液温度为 ,写出装置乙中发生反应的离子方程式:
,写出装置乙中发生反应的离子方程式:_____ ,能说明装置乙中反应已经完全的实验现象是_____ 。
(2)装置乙中反应完成后,过滤出溴化亚铜沉淀进行洗涤,先用亚硫酸溶液而不直接用蒸馏水洗涤的原因是_____ ,再用乙醇洗涤的目的是_____ (任答两点)。
(3)某研究性学习小组探究不同价态铜的稳定性,进行如下实验:
①向 中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,更稳定的是
中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,更稳定的是_____ 价铜(填“ ”或“
”或“ ”)。
”)。
②将 粉末加热至
粉末加热至 以上完全分解成
以上完全分解成 粉末,该反应的化学方程式为
粉末,该反应的化学方程式为_____ ,该反应说明:在高温条件下,更稳定的是_____ 价铜(填“ ”或“
”或“ ”)。
”)。
 在很多有机反应中常被用作催化剂,该物质为白色固体,具有易被氧化,微溶于水,不溶于乙醇等性质,可用如图所示的装置制备。
在很多有机反应中常被用作催化剂,该物质为白色固体,具有易被氧化,微溶于水,不溶于乙醇等性质,可用如图所示的装置制备。
回答下列问题:
(1)制备
 的反应在装置乙中进行,向其中加入一定量
的反应在装置乙中进行,向其中加入一定量 和过量
和过量 配制成的
配制成的 溶液,然后通入足量的
溶液,然后通入足量的 (部分夹持及加热装置已略去)。
(部分夹持及加热装置已略去)。①装置乙用到的容器名称为
②请指出上图所示的实验装置中的明显错误:
③该反应需保持反应液温度为
 ,写出装置乙中发生反应的离子方程式:
,写出装置乙中发生反应的离子方程式:(2)装置乙中反应完成后,过滤出溴化亚铜沉淀进行洗涤,先用亚硫酸溶液而不直接用蒸馏水洗涤的原因是
(3)某研究性学习小组探究不同价态铜的稳定性,进行如下实验:
①向
 中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,更稳定的是
中加适量稀硫酸,得到蓝色溶液和一种红色固体,由此可知,在酸性溶液中,更稳定的是 ”或“
”或“ ”)。
”)。②将
 粉末加热至
粉末加热至 以上完全分解成
以上完全分解成 粉末,该反应的化学方程式为
粉末,该反应的化学方程式为 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
6 . 镍及其化合物用途广泛。某矿渣的土要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,如图是从该矿渣中回收NiSO4的工艺路线:
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中
生成NiSO4、Fe2(SO4)3。锡(Sn)位子第五周期第IVA族.
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是________________ 。
(2)"浸泡“过程中Fe2(SO4)3生成FeO(OH)的离子方程式为__________ ,“浸渣”的成分除Fe2O3、FeO(OH)外还含有____________ (填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将 Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的_____ 倍;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式________________ 。
⑷“浸出液”中c(Ca2+) =1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=______ mol·L-1。[已知Ksp(CaF2) > 4.0×10-11]

(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是__________ 。
(6)已知正十二烷可用作该工艺的萃取剂。用电化学制备正十二烷的方法为:向烧杯中加入50mL甲醇,不断搅拌加入少量金属钠,再加入11mL正庚酸搅拌均匀,装好铂电极,接通电源反应,当电流明显减小时切断电源,然后提纯正十二烷。已知电解总反应为:
2C6H13COONa + 2CH3OH C12H26+ 2CO2↑+H2↑+2CH3ONa
C12H26+ 2CO2↑+H2↑+2CH3ONa
下列说法正确的是(_____ )
A.图中电源的A极为直流电源的负极
B.加入金属钠可以将酸转化为钠盐,提高离子浓度,增强导电性
C.阳极电极反应为:2C6H13COO--2e-=C12H26+2CO2↑
D.反应一段时间后将电源正负极反接,会产生杂质影响正十二烷的制备

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中
生成NiSO4、Fe2(SO4)3。锡(Sn)位子第五周期第IVA族.
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是
(2)"浸泡“过程中Fe2(SO4)3生成FeO(OH)的离子方程式为
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将 Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的
⑷“浸出液”中c(Ca2+) =1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=

(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是
(6)已知正十二烷可用作该工艺的萃取剂。用电化学制备正十二烷的方法为:向烧杯中加入50mL甲醇,不断搅拌加入少量金属钠,再加入11mL正庚酸搅拌均匀,装好铂电极,接通电源反应,当电流明显减小时切断电源,然后提纯正十二烷。已知电解总反应为:
2C6H13COONa + 2CH3OH
 C12H26+ 2CO2↑+H2↑+2CH3ONa
C12H26+ 2CO2↑+H2↑+2CH3ONa
下列说法正确的是(
A.图中电源的A极为直流电源的负极
B.加入金属钠可以将酸转化为钠盐,提高离子浓度,增强导电性
C.阳极电极反应为:2C6H13COO--2e-=C12H26+2CO2↑
D.反应一段时间后将电源正负极反接,会产生杂质影响正十二烷的制备
您最近一年使用:0次
2017-05-11更新
|
649次组卷
|
2卷引用:贵州省遵义市第二教育集团2023-2024学年高一上学期期末化学模拟试卷



