21-22高一·全国·假期作业
解题方法
1 . 重铬酸钾(K2Cr2O7)是重要的化合物,常用于制铬矾、火柴、铬颜料等。一些含铬化合物的转化关系如下图所示:
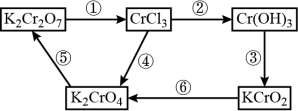
下列有关说法不正确的是

下列有关说法不正确的是
| A.K2Cr2O7中Cr的化合价为+6 |
| B.②③⑤均属于非氧化还原反应 |
| C.完成①④⑥的转化均需加入氧化剂 |
| D.①中生成1molCrCl3,转移3mol电子 |
您最近一年使用:0次
2 . 若以I2(l)为溶剂,下列四个反应中何者为歧化、反歧化、溶剂合、复分解:
(1)KI+IBr=KBr+I2_______
(2)NaCN+I2=NaI+ICN_______
(3)KI+I2=KI3_______
(4)PbC12+2KI=PbI2+2KCl_______
(1)KI+IBr=KBr+I2
(2)NaCN+I2=NaI+ICN
(3)KI+I2=KI3
(4)PbC12+2KI=PbI2+2KCl
您最近一年使用:0次
解题方法
3 . 工业上产生的硫化氢要经过处理变成硫单质后方能排放,以防止大气污染。富玛克斯法治理硫化氢的方法和步骤如下:
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式_______ 。
(2)请对富玛克斯法的优点做一简要评价_______ 。
①用2%~3%的Na2CO3溶液作吸收剂生成2种酸式盐;
②再加入一种RNO(液)(R表示芳香烃基)与生成的一种酸式盐的水溶液反应生成硫、碱和RNHOH;
③第②步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④RNHOH与空气中的氧发生反应又得到RNO。
(1)写出上述四步反应的化学方程式
(2)请对富玛克斯法的优点做一简要评价
您最近一年使用:0次
4 . 下列关于氧化还原反应的说法错误的是
①NaH+H2O=NaOH+H2↑的反应中NaH是还原剂,H2O是氧化剂
②反应3NO2+H2O=2HNO3+NO中氧化剂、还原剂的物质的量比为2:1
③3Cu+8H++2 =3Cu2++2NO↑+4H2O的反应中硝酸只起还原作用
=3Cu2++2NO↑+4H2O的反应中硝酸只起还原作用
④2Al+2NaOH+2H2O=2NaAlO2+3H2↑的反应中Al是还原剂,H2是还原产物
⑤5NH4NO3=4N2↑+2HNO3+9H2O的反应中,氧化产物和还原产物物质的量比为3:5
①NaH+H2O=NaOH+H2↑的反应中NaH是还原剂,H2O是氧化剂
②反应3NO2+H2O=2HNO3+NO中氧化剂、还原剂的物质的量比为2:1
③3Cu+8H++2
 =3Cu2++2NO↑+4H2O的反应中硝酸只起还原作用
=3Cu2++2NO↑+4H2O的反应中硝酸只起还原作用④2Al+2NaOH+2H2O=2NaAlO2+3H2↑的反应中Al是还原剂,H2是还原产物
⑤5NH4NO3=4N2↑+2HNO3+9H2O的反应中,氧化产物和还原产物物质的量比为3:5
| A.①②③④⑤ | B.②④⑤ | C.①②③⑤ | D.②③⑤ |
您最近一年使用:0次
5 . 某同学利用6种试剂中的4种进行实验[(a)0.1mol·L-1KI-淀粉溶液、(b)0.1mol·L-1KClO3溶液、(c)0.1mol·L-1KClO4溶液、(d)新制氯水、(e)稀硫酸、(f)1mol·L-1NaOH溶液]:向一支试管中按照一定顺序分别加入这些物质,且每种物质最多只加入一次,观察到的现象是:①无色→②无色→③蓝色→④无色→⑤蓝色。对该过程的下列分析中,正确的是
| A.试剂的加入顺序是:a→c→e→f→d |
B.②→③反应的离子方程式为:C1O +8I-+8H+=Cl-+4I2+4H2O +8I-+8H+=Cl-+4I2+4H2O |
| C.③蓝色→④无色,是因为加入NaOH溶液后,单质碘发生歧化反应 |
| D.④无色→⑤蓝色,一定是因为加入氯水后,将溶液中的I-氧化为单质碘 |
您最近一年使用:0次
解题方法
6 . 由于6s2惰性电子对效应,金Au、汞Hg、铊TI、铅Pb、铋Bi的最稳定氧化态分别为-1,0,+1,+2,+3.下 列说法正确的是
| A.根据这个规律,人们制出负一价的金的化合物CsAu |
B.与汞同族锌镉为较活泼金属而汞为不活泼金属,且对于+1氧化态,Hg倾向于形成Hg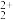 |
| C.二氧化铅氧化性很强,可和浓盐酸反应制取氯气PbO2 + 4HCl(浓) = PbCl2+ Cl2↑+ 2H2O |
D.铋酸钠与硫酸锰反应的离子方程式5NaBiO3+ 2Mn2++ 14H+ = 5Bi3++ 2MnO + 5Na++ 7H2O + 5Na++ 7H2O |
您最近一年使用:0次
7 . 硼氢化钠(NaBH4)是常用的还原剂之一,与水反应可放出氢气,可用如下所示转化合成。已知硼氢化钠中B为+3价。下列有关说法错误的是
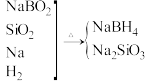
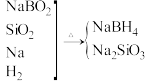
| A.该合成反应在隔绝空气的条件下进行 |
| B.该合成反应中Na和H2作还原剂 |
| C.NaBH4与水反应时,每生成1molH2转移1mole- |
D.该反应的化学方程式为NaBO2+2SiO2+4Na+2H2 2Na2SiO3+NaBH4 2Na2SiO3+NaBH4 |
您最近一年使用:0次
解题方法
8 . (1)下列物质中①NaCl晶体 ②二氧化碳 ③稀硫酸 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦熔融NaHCO3,属于电解质的是(填序号)___________ 。
(2)0.5molH2O的质量为___________ g,含有质子数为___________ 。
(3)20g A和14. 6g B恰好完全反应生成12.4gC和0.2mol D,则D的摩尔质量为___________ 。
(4)某地酸雨经检验,除含氢离子外,还有如下离子:c(Na+)=1.4×10-3 mol·L-1 ,c(Cl-) =3.5×10-3 mol·L-1 ,c(NH ) =2.3×10-3 mol·L-1 , c(SO
) =2.3×10-3 mol·L-1 , c(SO ) =1.5×10-3 mol·L-1.,则该溶液中氢离子的浓度为
) =1.5×10-3 mol·L-1.,则该溶液中氢离子的浓度为___________ mol·L-1。
(5)已知Cu与稀硝酸的反应为:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2H2O。
①用双线桥标出电子转移的方向与数目___________ 。
②氧化剂与还原剂的物质的量之比为:___________ 。
③当反应中有lmol NO2生成,转移的电子有___________ mol。
(2)0.5molH2O的质量为
(3)20g A和14. 6g B恰好完全反应生成12.4gC和0.2mol D,则D的摩尔质量为
(4)某地酸雨经检验,除含氢离子外,还有如下离子:c(Na+)=1.4×10-3 mol·L-1 ,c(Cl-) =3.5×10-3 mol·L-1 ,c(NH
 ) =2.3×10-3 mol·L-1 , c(SO
) =2.3×10-3 mol·L-1 , c(SO ) =1.5×10-3 mol·L-1.,则该溶液中氢离子的浓度为
) =1.5×10-3 mol·L-1.,则该溶液中氢离子的浓度为(5)已知Cu与稀硝酸的反应为:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2H2O。
①用双线桥标出电子转移的方向与数目
②氧化剂与还原剂的物质的量之比为:
③当反应中有lmol NO2生成,转移的电子有
您最近一年使用:0次



