1 . 在实验室进行少量铁粉和硫粉混合加热的实验,将其产物又进行了系列实验,流程如下。下列说法正确的是
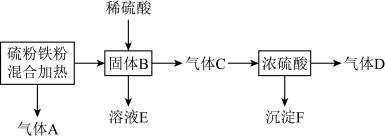

A.气体A和D含有 ,且均为氧化产物 ,且均为氧化产物 |
| B.上述过程中,硫元素共参加了2个氧化还原反应 |
| C.气体A、C混合也能生成固体F |
D.气体C与浓硫酸反应的化学方程式为: |
您最近一年使用:0次
2023-02-12更新
|
1314次组卷
|
4卷引用:江西省南昌市进贤县第一中学2022-2023学年高一下学期第一次月考化学试题
2 . 部分含氯物质的分类与相应氯元素的化合价关系如图所示,下列说法错误的是
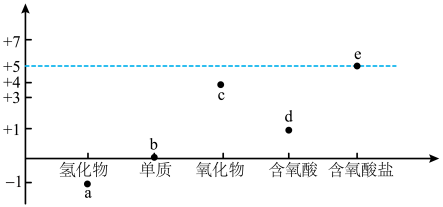

| A.a与d,a与e在酸性情况下反应,均可以得到b |
| B.c为一种新型自来水消毒剂,可用于代替b,能有效降低水中余氯的含量 |
| C.b的水溶液久置后会因为b的挥发导致溶液pH升高 |
| D.消毒液可用于环境消毒,主要是因为产生d |
您最近一年使用:0次
名校
解题方法
3 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
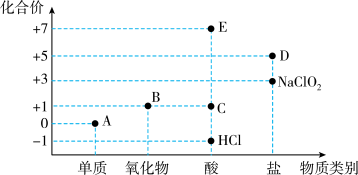
回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有_______ ;A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为_______ 。
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______ 。
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为______ 。
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的_______ 倍(还原产物都是Cl-,消毒效率以单位物质的量的物质得到的电子数表示)。
②ClO2在杀菌消毒过程中会产生亚氯酸盐( ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是_________ (填标号)。
A.FeSO4 B.O3 C.KMnO4 D.Na2SO3

回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的
②ClO2在杀菌消毒过程中会产生亚氯酸盐(
 ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是A.FeSO4 B.O3 C.KMnO4 D.Na2SO3
您最近一年使用:0次
2023-06-08更新
|
236次组卷
|
5卷引用:江西省丰城中学2023-2024学年高三上学期开学考试化学试题
4 . A、B、C、D几种纯净物至少含一种共同的元素,它们之间有如下转化关系(部分条件和产物省略)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为___________ 。C→D的离子方程式为___________ 。
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为___________ ,X的电离方程式为___________ 。
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为___________ 。
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
①能证明C中阳离子具有还原性的实验是___________ (填代号)。
②丙实验中溶液由无色变红色的原因是___________ (用离子方程式表示)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
| 实验 | 操作 | 现象 |
| 甲 | 加入镁粉 | 溶液颜色逐渐变为无色 |
| 乙 | 依次滴加KSCN溶液、新制氯水 | 开始不变色,后变红色 |
| 丙 | 先滴加KSCN溶液,后滴加酸化的双氧水 | 开始不变色,后变红色 |
②丙实验中溶液由无色变红色的原因是
您最近一年使用:0次
名校
解题方法
5 . A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、E五种物质里含有相同的一种金属元素,并且A、B、C、D都可与物质M反应生成E,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B的澄清溶液检验CO2。
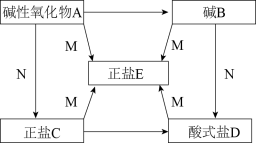
回答下列问题:
(1)写出物质的化学式:A__________ 、B__________ 、C__________ 、E__________ 。
(2)M属于__________ (填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(3)写出正盐C转化为酸式盐D的化学方程式:____________________ 。
(4)写出碱B转化为酸式盐D的化学方程式:____________________ 。

回答下列问题:
(1)写出物质的化学式:A
(2)M属于
(3)写出正盐C转化为酸式盐D的化学方程式:
(4)写出碱B转化为酸式盐D的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 现有原子序数依次增大的短周期主族元素W、P、Q,气体X、Y、Z分别为W、P、Q的单质,X、Y、Z之间能发生如图转换关系。已知化合物乙的水溶液常用于蚀刻玻璃,化合物乙与化合物甲反应可生成白烟。下列说法正确的是
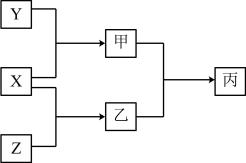

| A.W元素的氧化物中只存在极性共价键 |
| B.P元素的氧化物都是酸性氧化物 |
| C.化合物甲能使湿润的紫色石蕊试纸变红 |
| D.化合物甲和乙分子中所含电子总数相同 |
您最近一年使用:0次
名校
解题方法
7 . 物质类别和元素价态,是学习元素及其化合物性质的重要认识视角。部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断不合理的是

A.工业上通过a→c→d→e来制备 |
| B.a→b的过程是氮的固定 |
C.浓的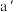 溶液和浓的 溶液和浓的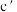 溶液反应可以得到 溶液反应可以得到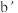 |
D.加热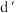 的固态钾盐可以产生 的固态钾盐可以产生 |
您最近一年使用:0次
2023-01-16更新
|
832次组卷
|
4卷引用:江西省湖口中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
8 . 某金属单质在一定条件下有如下转化关系。Y是氧化物,能被强磁铁吸附,溶液P呈浅绿色。

请回答下列问题:
(1)W是___________ (填化学式),Y的俗名是___________ 。
(2)写出X在高温下与水蒸气反应的化学方程式:___________ 。
(3)检验Q中显黄色的阳离子实验方法是___________ 。
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:___________ 。
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有___________ (填两条)。
(6)在溶液Q中加入单质M粉末从反应的离子方程式为___________ 。

请回答下列问题:
(1)W是
(2)写出X在高温下与水蒸气反应的化学方程式:
(3)检验Q中显黄色的阳离子实验方法是
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有
(6)在溶液Q中加入单质M粉末从反应的离子方程式为
您最近一年使用:0次
2022-12-10更新
|
236次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
名校
解题方法
9 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为_______ ;丁属于_______ (“酸性”或“碱性”)氧化物。
(2)根据氯元素的化合价判断,乙物质的性质_______ (填标号)。
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为: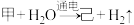 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是_______ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_______ 。庚与洁厕灵(主要成分盐酸)同时使用会产生有毒的氯气,写出反应的离子方程式:_______ 。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为_______ 。
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式_______ 。

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质的性质
a.只有氧化性
b.既有氧化性又有还原性
c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:
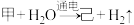 (未配平),配平后参与反应的甲与H2O的微粒个数之比是
(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024个氧气分子,转移e-的物质的量为
(6)工业上可以用草酸(H2C2O4,二元弱酸)还原辛的方法生产丙,草酸被氧化为CO2,请写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.根据下图转化关系及现象回答问题:
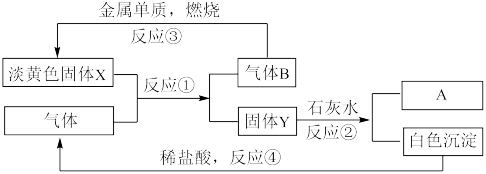
(1)物质A是_______ (填写化学式)
(2)反应①的化学方程式为_______ 。
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是_______ 。(填序号)
①NaCl溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液
Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。
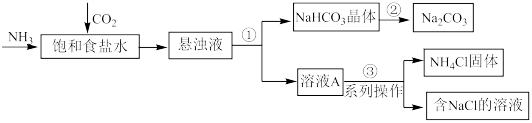
(4)步骤①②③中涉及“过滤”操作的是_______ (填序号)。
(5)向饱和食盐水中通入 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是_______ 。
(6)从步骤①中分离出的 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是_______ (写出杂质的化学式),欲得到纯净的 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,_______ 。

(1)物质A是
(2)反应①的化学方程式为
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是
①NaCl溶液 ②
 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。

(4)步骤①②③中涉及“过滤”操作的是
(5)向饱和食盐水中通入
 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是(6)从步骤①中分离出的
 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
您最近一年使用:0次
2022-11-16更新
|
554次组卷
|
5卷引用:江西省丰城中学2022-2023学年高一上学期第三次段考化学试卷



