1 . 海洋蕴藏着中极为丰富的化学资源,如海水中就有80多种元素,所含的盐大部分是氯化钠。十九世纪末工业上开始通过电解饱和食盐水的方法制备氯气、氨气和烧碱,并以它们为原料生产一系列含氯、含钠产品(氯碱工业),请回答下列问题:
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
(2)电解饱和食盐水时,与电源正极相连的电极叫阳极,阳极产物是氯气,可以用______ 检验,现象为______ ,写出检验氯气的离子方程式_____________________
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
(4)新制氧水呈浅黄绿色,是因为氯水中存在______(单选)
(5)有两组学生根据不同的反应原理在实验室制取氯气。

①请按要求填表。
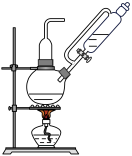
②有同学建议第一组使用图所示装置作为氯气的发生装置,请谈谈你的看法______ 。
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。
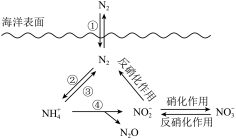
(6)海洋中的氮循环属于固氮作用的一步是______ (填图中的数字序号)。
(7)下列关于海洋氮循环的说法正确的是______(双选)。
(8)有氧时,在硝化细菌作用下, 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。_______ 。

(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是______ ,在最佳反应温度时, 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是____ 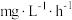 。
。
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
| A.侯德榜 | B.吴蕴初 | C.荣毅仁 | D.戴安邦 |
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
A. | B. | C. | D. |
A. | B. | C. | D. |

①请按要求填表。
实验组 | 实验原理 | 发生装置(填编号) |
第一组 |  | |
第二组 | 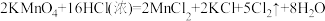 |

氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。

(6)海洋中的氮循环属于固氮作用的一步是
(7)下列关于海洋氮循环的说法正确的是______(双选)。
| A.海洋中存在游离态的氮 |
| B.海洋中的氮循环起始于氮的氧化 |
C.向海洋排放含 的废水会影响海洋中 的废水会影响海洋中 的含量 的含量 |
| D.海洋中的反硝化作用一定有氧气的参与 |
 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对
 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是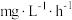 。
。温度/ | 样本氨氮含量/ | 处理 | 处理 |
氨氮含量/ | 氨氮含量/ | ||
20 | 1008 | 838 | 788 |
25 | 1008 | 757 | 468 |
30 | 1008 | 798 | 600 |
40 | 1008 | 977 | 910 |
您最近一年使用:0次
2 . 1774年,舍勒在研究软锰矿(主要成分MnO2)时,将它与浓盐酸混合加热,产生了一种黄绿色气体。舍勒的方法沿用至今,实验室用如下装置制取氯气并进行氯气性质探究。
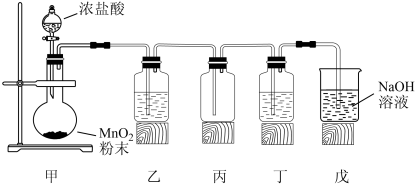
完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是_______ 。盛放浓盐酸的仪器名称为_______ 。
(2)乙为除杂装置,盛有_______ (填写下列字母编号),目的是为了_______ 。
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是_______ 。
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
(5)戊装置的作用是_______ ,该处的化学反应方程式为_______ 。
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是_______ g(保留一位小数)。

完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是
(2)乙为除杂装置,盛有
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
| 实验现象 | 原因 |
| 最初溶液从紫色逐渐变为 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | |
| 然后溶液从无色逐渐变为 | / |
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是
您最近一年使用:0次
2022-01-16更新
|
343次组卷
|
2卷引用:上海市静安区2022届高三一模化学试题
23-24高三上·上海浦东新·阶段练习
名校
解题方法
3 . 海水中的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(1)氯气是一种重要的化工原料,可用以下几种方法制取氯气。
a.实验室可用二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:___________ 。
b.工业上电解饱和食盐水制氯气,写出其反应的离子方程式:___________ 。
c.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(2)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________ 。
(3)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________ 。

(1)氯气是一种重要的化工原料,可用以下几种方法制取氯气。
a.实验室可用二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:
b.工业上电解饱和食盐水制氯气,写出其反应的离子方程式:
c.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为
(2)将氯气分别通入含下列离子的溶液中,离子浓度减小的是
A. | B. | C. | D. |

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时间的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
您最近一年使用:0次
4 . 含氯化合物在生活生产中具有广泛作用。完成下列问题:
(1)含氯产品①中钢瓶上应贴的标签为______ 。

(2)关于保存液氯、液溴的说法正确的是______ 。
漂白粉的消毒能力以酸化时释放出来的氯气量作标准,用来衡量含氯消毒剂的消毒能力,以Cl%= ×100%(有效氯含量)表示。
×100%(有效氯含量)表示。
(3)漂白粉的有效成分为______ (填写化学式)。实验证实,某批次的漂白粉的碱性明显大于正常情况下的漂白粉。原因是可能该批次的产品中混有较多的______ (填写化学式)。
(4)现有一种漂白粉:Ca(OH)2•3CaCl(ClO)•nH2O的“有效氯”为40.4%,则式中n值应是______ 。
小宸同学在实验室制备、收集氯气,并进行氯水中相关物质的性质探究,回答下列问题。
I.制备并收集Cl2
(5)写出制备方程式______ ,MnO2发生______ 反应(填写氧化或还原)。
(6)图1装置制备氯气中含有______ 和水蒸气,收集前需要通过装有______ 的洗气瓶除杂。

(7)有同学提出用图2装置制取氯气。

①仪器X名称为______ ;
②使用仪器X制备气体,优点在于______ 。
II.氯水相关物质的性质探究
(8)关于液氯与新制氯水叙述正确的是______ 。
(9)久置的氯水和新制的氯水相比较,下列结论正确的是______ 。
III.验证氯水中HClO光照分解的产物
将图3新制氯水置于三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。


(10)若能够证明氯水中HClO在光照下发生了分解反应,则图4中纵坐标不可以表示的物理量是______ 。(注:酸性溶液中,c(H+)越大,pH越小,溶液酸性越强)
(11)氯水久置易变质,检验一瓶氯水是否已经完全变质,可选用的试剂是______ 。
(1)含氯产品①中钢瓶上应贴的标签为

A. | B. | C. | D. |
| A.液氯贮存在干燥的钢瓶中 | B.液溴保存时需加入一些苯覆盖 |
| C.常温下保存液氯应采用低压 | D.液溴应保存在棕色的广口瓶中 |
漂白粉的消毒能力以酸化时释放出来的氯气量作标准,用来衡量含氯消毒剂的消毒能力,以Cl%=
 ×100%(有效氯含量)表示。
×100%(有效氯含量)表示。(3)漂白粉的有效成分为
(4)现有一种漂白粉:Ca(OH)2•3CaCl(ClO)•nH2O的“有效氯”为40.4%,则式中n值应是
小宸同学在实验室制备、收集氯气,并进行氯水中相关物质的性质探究,回答下列问题。
I.制备并收集Cl2
(5)写出制备方程式
(6)图1装置制备氯气中含有

(7)有同学提出用图2装置制取氯气。

①仪器X名称为
②使用仪器X制备气体,优点在于
II.氯水相关物质的性质探究
(8)关于液氯与新制氯水叙述正确的是
| A.都含有氯离子 | B.都含氯分子 | C.都是电解质 | D.都能导电 |
| A.颜色相同 | B.都能使有色布条褪色 |
| C.都能使淀粉碘化钾试纸变蓝 | D.加AgNO3溶液都能生成白色沉淀 |
III.验证氯水中HClO光照分解的产物
将图3新制氯水置于三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。


(10)若能够证明氯水中HClO在光照下发生了分解反应,则图4中纵坐标不可以表示的物理量是
| A.氯水的pH | B.氢离子的浓度 | C.氯离子的浓度 | D.氧气的体积分数 |
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.紫色石蕊溶液 |
您最近一年使用:0次
名校
5 . 用氯气制成漂粉精的目的
| A.转变为较稳定,便于贮存的物质 | B.转变为能溶于水的物质 |
| C.提高氯的质量分数 | D.增强漂白能力 |
您最近一年使用:0次
解题方法
6 . 用自来水养鱼时,将水注入鱼缸前需在阳光下暴晒一段时间,这样做的目的是
| A.分解水中的次氯酸 | B.增加氧气的含量 | C.杀菌消毒 | D.使水的温度升高 |
您最近一年使用:0次
名校
7 . 生产自来水最重要的两步工序是净化和消毒,净化一般使用 ,消毒一般使用
,消毒一般使用 。
。
(1) 溶液呈酸性的原因是(用离子方程式表示)
溶液呈酸性的原因是(用离子方程式表示)____________ ; 具有净水作用,但会腐蚀钢铁设备,除
具有净水作用,但会腐蚀钢铁设备,除 作用外,另一主要原因是(用离子方程式表示):
作用外,另一主要原因是(用离子方程式表示):____________ 。
(2)氯气的水溶液称为氯水,氯水中存在多个平衡,写出其中两个含氯元素的平衡方程式:____________ 、____________ 。氯水中存在 分子、
分子、 分子和
分子和 分子,不存在
分子,不存在 分子的原因是
分子的原因是_______ ,除水分子外,新制氯水中含量最多的微粒是__________ 。
(3)次氯酸有漂白杀菌作用,其作用原理是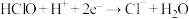 ,该变化是
,该变化是____________ 反应(选填“氧化”、“还原”、“氧化还原”);在 溶液中通入少量
溶液中通入少量 气体,只发生如下反应:
气体,只发生如下反应: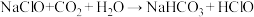 ,由此判断
,由此判断 、
、 和
和 的酸性由强到弱的顺序是
的酸性由强到弱的顺序是____________ 。
(4) 能用于自来水消毒,还能除去水中的
能用于自来水消毒,还能除去水中的 杂质,产物为
杂质,产物为 和盐酸。写出该反应的离子方程式
和盐酸。写出该反应的离子方程式__________________ 。
 ,消毒一般使用
,消毒一般使用 。
。(1)
 溶液呈酸性的原因是(用离子方程式表示)
溶液呈酸性的原因是(用离子方程式表示) 具有净水作用,但会腐蚀钢铁设备,除
具有净水作用,但会腐蚀钢铁设备,除 作用外,另一主要原因是(用离子方程式表示):
作用外,另一主要原因是(用离子方程式表示):(2)氯气的水溶液称为氯水,氯水中存在多个平衡,写出其中两个含氯元素的平衡方程式:
 分子、
分子、 分子和
分子和 分子,不存在
分子,不存在 分子的原因是
分子的原因是(3)次氯酸有漂白杀菌作用,其作用原理是
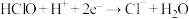 ,该变化是
,该变化是 溶液中通入少量
溶液中通入少量 气体,只发生如下反应:
气体,只发生如下反应: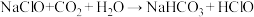 ,由此判断
,由此判断 、
、 和
和 的酸性由强到弱的顺序是
的酸性由强到弱的顺序是(4)
 能用于自来水消毒,还能除去水中的
能用于自来水消毒,还能除去水中的 杂质,产物为
杂质,产物为 和盐酸。写出该反应的离子方程式
和盐酸。写出该反应的离子方程式
您最近一年使用:0次
真题
8 . 印染工业常用亚氯酸钠(NaClO2)漂白织物。亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2—,其中HClO2是漂白剂的有效成分,ClO2是有毒气体。各组分含量随pH变化情况如图所示,由图可知,使用该漂白剂的最佳pH为


| A.3.0 | B.4.0—4.5 | C.6.5—7.0 | D.9.0 |
您最近一年使用:0次
2019-01-30更新
|
472次组卷
|
6卷引用:2008年普通高等学校招生统一考试综合试题(理科使用)化学部分(上海卷)
2008年普通高等学校招生统一考试综合试题(理科使用)化学部分(上海卷)(已下线)2011-2012学年北京市朝阳区高一下学期期末统一考试化学试卷2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷第 25 届全国高中学生化学竞赛(江苏赛区)初赛试题北京市海淀区中国地质大学附属中学2019-2020学年高一上学期9月月考化学试卷(已下线)微项目 科学使用含氯消毒剂-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
9 . CuCl广泛应用于化工和印染等行业。在实验室中模拟热分解CuCl2·xH2O制备CuCl的原理和实验装置如下:
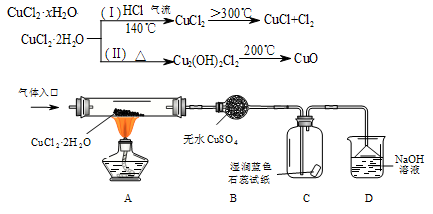
完成下列填空:
(1)在实验(Ⅰ)过程中,观察到B中固体由白色变为蓝色,C中产生的现象是__________ ,导致该现象的物质是________________________ 。
(2)装置D的作用是___________________________________ ,其中发生氧化还原反应的化学方程式是_____________________________________ 。
(3)反应结束后,CuCl产品中可能存在少量的CuCl2或CuO杂质。
①若杂质是CuCl2,则原因是_________________________________________ 。
②若杂质是CuO,则原因是__________________________________________ 。
(4)根据实验(Ⅱ),测定CuCl2·xH2O中结晶水的含量。取CuCl2·xH2O样品1.692g,经过3次灼烧、冷却、称量,得到黑色固体的质量数据如下:
则x=_____________ (保留2位小数)。

完成下列填空:
(1)在实验(Ⅰ)过程中,观察到B中固体由白色变为蓝色,C中产生的现象是
(2)装置D的作用是
(3)反应结束后,CuCl产品中可能存在少量的CuCl2或CuO杂质。
①若杂质是CuCl2,则原因是
②若杂质是CuO,则原因是
(4)根据实验(Ⅱ),测定CuCl2·xH2O中结晶水的含量。取CuCl2·xH2O样品1.692g,经过3次灼烧、冷却、称量,得到黑色固体的质量数据如下:
| 称 量 | 第1次 | 第2次 | 第3次 |
| 质量(g) | 0.820g | 0.800g | 0.800g |
则x=
您最近一年使用:0次
2018-05-02更新
|
451次组卷
|
2卷引用:【全国区级联考】上海市金山区2018届高三下学期质量监控(二模)化学试题
名校
10 . 饲养金鱼所用的自来水(经氯气消毒),需经日晒或放置一段时间后,再注入鱼缸。其主要目的是
| A.提高水温,有利于金鱼生长 |
| B.利用紫外线杀灭水中的细菌 |
| C.增加水中氧气的含量 |
| D.除去溶于水中Cl2,并促使次氯酸分解,以利于金鱼存活 |
您最近一年使用:0次
2016-12-09更新
|
258次组卷
|
9卷引用:2.1.3 次氯酸和次氯酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
(已下线)2.1.3 次氯酸和次氯酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)2015-2016学年吉林省长春第十一高中高一上期末化学试卷吉林省长春市十一高中2017-2018学年高一上学期期末考试化学试题安徽省滁州市定远县育才学校2017-2018学年高一(普通班)下学期第一次月考化学试题安徽省合肥市长丰县2020-2021学年高一上学期期末联考化学试题吉林市第五十五中学2021-2022学年高一上学期期中考试化学(理)试题吉林市第五十五中学2021-2022学年高一上学期期中考试化学(文)试题吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(文)试题山东省五地市多校2023-2024学年高一上学期10月月考化学试题






