1 . 某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。
已知:①A中反应为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。
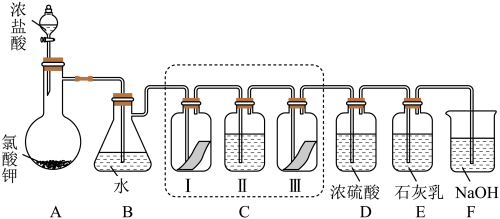
(1)写出B装置中反应的离子方程式_______ 。实验结束后,立即将B中溶液滴几滴在紫色石蕊试纸上,可观察到的现象是_______ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III 处依次放入的物质正确的是_______ (填编号)。
(3)F 装置的作用是(用离子方程式表示)_______
(4)为测定E中所得漂白粉的有效成分含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成分的质量分数为_______ (用含 a、b 的式子表示)。
已知:①A中反应为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。

(1)写出B装置中反应的离子方程式
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III 处依次放入的物质正确的是
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
(4)为测定E中所得漂白粉的有效成分含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成分的质量分数为
您最近一年使用:0次
解题方法
2 . 某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。已知:
①A 中反应为 KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为 Ca(OH)2,其他杂质不参与反应。
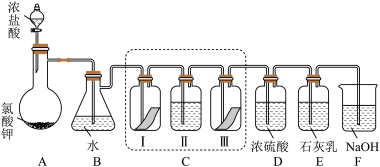
(1)写出 B 装置中反应的化学方程式_______________ 。实验结束后,立即将 B 中溶液滴几滴在紫色石蕊试纸上,可观察到的现象是______________ 。
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中 I、II、III 处依次放入的物质正确的是_________ (填编号)。
(3)待 E 中物质完全反应后,经过一系列加工处理,得到漂白粉样品,其有效成份为____________ (填化学式)。
(4)F 装置的作用是(用离子方程式表示)_____________
(5)为测定(3)中所得漂白粉的有效成份含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成份的质量分数为_________________ (用含 a、b 的式子表示)。
①A 中反应为 KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为 Ca(OH)2,其他杂质不参与反应。

(1)写出 B 装置中反应的化学方程式
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中 I、II、III 处依次放入的物质正确的是
| 编号 | I | II | III |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
(4)F 装置的作用是(用离子方程式表示)
(5)为测定(3)中所得漂白粉的有效成份含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成份的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验纯碱入中是否存在NaCl | 向待测液中加入AgNO3溶液 |
| B | 检验新制氯水的酸碱性 | 将pH试纸放在玻璃片上,用玻璃棒蘸取新制氯水点在试纸中部,再与标准比色卡对照 |
| C | 除去CO2气体中混杂的少量HCl气体 | 将混合气体依次通过盛有饱和NaHCO3溶液和浓硫酸的洗气瓶 |
| D | 测定NaHCO3和CaCO3固体混合物中的NaHCO3质量分数 | 准确称取ag样品和试管总质量。充分加热后冷却至室温,再称量总质量为bg |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-19更新
|
77次组卷
|
3卷引用:福建省师范大学附属中学2023-2024学年高一上学期期末考试化学试题
解题方法
4 . 下列关于氯及其化合物的叙述中,正确的是
| A.用自来水配制硝酸银溶液不会引起变质 |
| B.铁在少量Cl2中燃烧,生成氯化铁 |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有HClO |
| D.等物质的量的Na2O与Na2O2与等量且足量的水反应得到溶液的质量分数不同 |
您最近一年使用:0次
名校
5 . 核心知识的准确记忆、巩固是学好化学最重要、最基础的环节。按要求回答:
(1)气体摩尔体积的单位是__________ ;
(2)物质的量浓度(c)与质量分数( )的换算公式:
)的换算公式: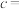
__________ ;(摩尔质量用M表示,密度 的单位为
的单位为 )
)
(3)蒸馏装置中温度计水银球的位置处于__________ ;
(4)容量瓶和分液漏斗使用前都必须进行的操作是__________ ;
(5)利用焰色反应检验物质,钾元素的焰色是__________ ;
(6) 的电离方程式为
的电离方程式为__________ ;
(7)氯气与水反应的化学方程式为__________ ;
不考虑物质挥发,新制氯水久置后导电能力变__________ (填“强或弱”)。
(8)下列溶液中 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。
(1)气体摩尔体积的单位是
(2)物质的量浓度(c)与质量分数(
 )的换算公式:
)的换算公式: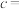
 的单位为
的单位为 )
)(3)蒸馏装置中温度计水银球的位置处于
(4)容量瓶和分液漏斗使用前都必须进行的操作是
(5)利用焰色反应检验物质,钾元素的焰色是
(6)
 的电离方程式为
的电离方程式为(7)氯气与水反应的化学方程式为
不考虑物质挥发,新制氯水久置后导电能力变
(8)下列溶液中
 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。A. 的 的 溶液 溶液 | B. 的 的 溶液 溶液 |
C.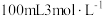 的 的 溶液 溶液 | D. 的 的 溶液 溶液 |
您最近一年使用:0次
解题方法
6 . 氯及其化合物是重要的化工原料。回答问题:
(1)在新制氯水中加入紫色石蕊试液的现象是___________ 。
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉
①制取漂白粉溶液的过程中,发生氧化还原反应的离子方程式为___________ 。
②将漂白粉加入含 的废水(密度为
的废水(密度为 )中,发生反应:
)中,发生反应: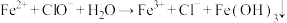 。理论上处理10吨含
。理论上处理10吨含 浓度为
浓度为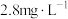 的废水(不考虑其他物质与漂白粉的反应),所需含
的废水(不考虑其他物质与漂白粉的反应),所需含 质量分数为
质量分数为 的漂白粉的质量为
的漂白粉的质量为___________ g。
(3)几种含氯离子的相对能量如下表所示:
①在上述五种离子中,最稳定的离子是___________ (填离子符号)。
②反应 的
的
___________  。
。
③写出 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:______ 。
(4)以 为原料,用
为原料,用 氧化制取
氧化制取 ,可提高效益减少污染。反应如下:
,可提高效益减少污染。反应如下:

上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可使 转化率接近
转化率接近 ,其基本原理如图所示。过程
,其基本原理如图所示。过程 的反应为
的反应为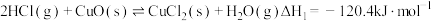 ,过程II反应的热化学方程式为
,过程II反应的热化学方程式为___________ 。

(1)在新制氯水中加入紫色石蕊试液的现象是
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石
 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉①制取漂白粉溶液的过程中,发生氧化还原反应的离子方程式为
②将漂白粉加入含
 的废水(密度为
的废水(密度为 )中,发生反应:
)中,发生反应: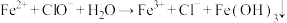 。理论上处理10吨含
。理论上处理10吨含 浓度为
浓度为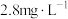 的废水(不考虑其他物质与漂白粉的反应),所需含
的废水(不考虑其他物质与漂白粉的反应),所需含 质量分数为
质量分数为 的漂白粉的质量为
的漂白粉的质量为(3)几种含氯离子的相对能量如下表所示:
| 离子 | Cl—(aq) | ClO——(aq) |  (aq) (aq) |  (aq) (aq) |  (aq) (aq) |
| 相对能量/(kJ·mol-1) | 0 | 60 | 101 | 63 | 38 |
①在上述五种离子中,最稳定的离子是
②反应
 的
的
 。
。③写出
 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:(4)以
 为原料,用
为原料,用 氧化制取
氧化制取 ,可提高效益减少污染。反应如下:
,可提高效益减少污染。反应如下:
上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可使
 转化率接近
转化率接近 ,其基本原理如图所示。过程
,其基本原理如图所示。过程 的反应为
的反应为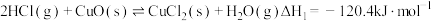 ,过程II反应的热化学方程式为
,过程II反应的热化学方程式为
您最近一年使用:0次
名校
7 . 某小组同学在实验室制备、收集氯气,并进行氯水中相关物质的性质探究,回答下列问题。
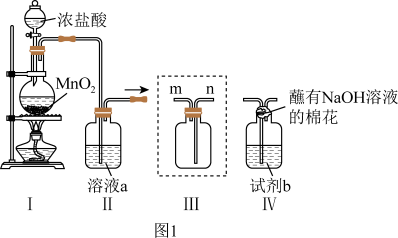
(1)制备Cl2。写出装置Ⅰ中发生的化学反应方程式_____________ 。
(2)氯水相关物质的性质探究。
①若装置Ⅳ中试剂b为H2O,制得氯水。写出Cl2与H2O反应的化学方程式为_________ 。
②若装置Ⅳ中试剂b为CCl4,可制得Cl2的CCl4溶液(Cl2可溶于CCl4溶液,且不与CCl4反应)。取稀盐酸、新制氯水、Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明____________________________ 。
③验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图2),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

若能够证明氯水中HClO在光照下发生了分解反应,则图3中纵坐标可以表示的物理量是
_________ (填字母)。(注:酸性溶液中,c(H+)越大,pH越小,溶液酸性越强)。
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数 e.溶液的颜色
据此数据,可分析得到HClO在光照下发生的化学反应方程式为__________________ 。
(3)若要模拟工业制备漂白粉,装置Ⅳ中试剂b为_____ ,制备漂白粉的化学方程式为______________ 。
若用43.50g二氧化锰与足量浓盐酸(质量分数为36.50%)完全反应,制取氯气。将所得气体全部用于制备漂白粉,所制得的漂白粉中所含有效成分的质量为________ 。(本题要求写出计算过程,答案保留2位小数)
(1)制备Cl2。写出装置Ⅰ中发生的化学反应方程式

(2)氯水相关物质的性质探究。
①若装置Ⅳ中试剂b为H2O,制得氯水。写出Cl2与H2O反应的化学方程式为
②若装置Ⅳ中试剂b为CCl4,可制得Cl2的CCl4溶液(Cl2可溶于CCl4溶液,且不与CCl4反应)。取稀盐酸、新制氯水、Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明
③验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图2),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

若能够证明氯水中HClO在光照下发生了分解反应,则图3中纵坐标可以表示的物理量是
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数 e.溶液的颜色
据此数据,可分析得到HClO在光照下发生的化学反应方程式为
(3)若要模拟工业制备漂白粉,装置Ⅳ中试剂b为
若用43.50g二氧化锰与足量浓盐酸(质量分数为36.50%)完全反应,制取氯气。将所得气体全部用于制备漂白粉,所制得的漂白粉中所含有效成分的质量为
您最近一年使用:0次
名校
解题方法
8 . 用氯气与石灰乳充分反应可以制取漂白粉,使用漂白粉作漂白剂比使用氯水更好的理由是
| A.漂白粉更容易与水反应 | B.漂白粉相对稳定且便于贮存 |
C.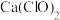 比HClO漂白快 比HClO漂白快 | D.漂白粉中的氯元素的质量分数更大 |
您最近一年使用:0次
名校
解题方法
9 . 现有以下物质:
①KHSO4 固体 ②Al ③KIO3固体 ④Fe(OH)3胶体 ⑤FeSO4溶液 ⑥干冰 ⑦氯水 ⑧乙醇 ⑨熔融碳酸钠
回答下列问题:
(1)以上物质在上述状态下能导电的是___________ 。
(2)①在水溶液中的电离方程式为___________ 。
(3)向碳酸钠溶液中通入CO2反应的化学方程式:___________ 。
(4)③可发生如下反应 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:___________ ;每生成3.81g I2,反应中转移电子的数目为___________ 。
(5)氯水中含有多种成分,因而具有多种性质。
①向氯水中滴加品红溶液观察到的现象是___________ ,可证明氯水中存在___________ 微粒。
②氯水久置过程中发生的变化,用化学反应方程式表示为___________ 。
③数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。下图是将传感器插入盛有氯水的广口瓶中测定光照氯水过程所得到的图像,该图像的纵坐标表示的意义是___________ 。
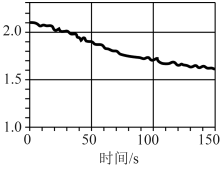
A.氯离子浓度 B.氧气体积分数 C.氯水的 D.Cl2的含量 E.氯水导电能力
D.Cl2的含量 E.氯水导电能力
①KHSO4 固体 ②Al ③KIO3固体 ④Fe(OH)3胶体 ⑤FeSO4溶液 ⑥干冰 ⑦氯水 ⑧乙醇 ⑨熔融碳酸钠
回答下列问题:
(1)以上物质在上述状态下能导电的是
(2)①在水溶液中的电离方程式为
(3)向碳酸钠溶液中通入CO2反应的化学方程式:
(4)③可发生如下反应
 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:(5)氯水中含有多种成分,因而具有多种性质。
①向氯水中滴加品红溶液观察到的现象是
②氯水久置过程中发生的变化,用化学反应方程式表示为
③数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。下图是将传感器插入盛有氯水的广口瓶中测定光照氯水过程所得到的图像,该图像的纵坐标表示的意义是

A.氯离子浓度 B.氧气体积分数 C.氯水的
 D.Cl2的含量 E.氯水导电能力
D.Cl2的含量 E.氯水导电能力
您最近一年使用:0次
解题方法
10 . 久置的氯水会失去漂白性,溶液由黄绿色变为无色。用强光照射氯水,并用传感器测定相关数据,得到如图曲线:
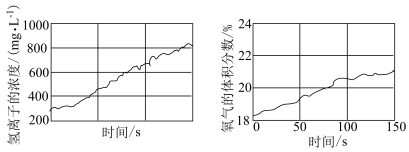
下列说法不正确的是

下列说法不正确的是
| A.久置氯水pH增大 |
| B.氯水呈黄绿色是因为溶解了氯气 |
| C.久置的氯水中氧气含量增加的原因次氯酸分解生成了氧气 |
| D.氯离子的检验,先加稀硝酸再加硝酸银,观察现象 |
您最近一年使用:0次



