解题方法
1 . 氯及其化合物是重要的化工原料。回答问题:
(1)在新制氯水中加入紫色石蕊试液的现象是___________ 。
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉
①制取漂白粉溶液的过程中,发生氧化还原反应的离子方程式为___________ 。
②将漂白粉加入含 的废水(密度为
的废水(密度为 )中,发生反应:
)中,发生反应: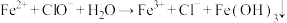 。理论上处理10吨含
。理论上处理10吨含 浓度为
浓度为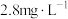 的废水(不考虑其他物质与漂白粉的反应),所需含
的废水(不考虑其他物质与漂白粉的反应),所需含 质量分数为
质量分数为 的漂白粉的质量为
的漂白粉的质量为___________ g。
(3)几种含氯离子的相对能量如下表所示:
①在上述五种离子中,最稳定的离子是___________ (填离子符号)。
②反应 的
的
___________  。
。
③写出 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:______ 。
(4)以 为原料,用
为原料,用 氧化制取
氧化制取 ,可提高效益减少污染。反应如下:
,可提高效益减少污染。反应如下:

上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可使 转化率接近
转化率接近 ,其基本原理如图所示。过程
,其基本原理如图所示。过程 的反应为
的反应为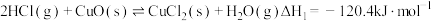 ,过程II反应的热化学方程式为
,过程II反应的热化学方程式为___________ 。

(1)在新制氯水中加入紫色石蕊试液的现象是
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石
 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉①制取漂白粉溶液的过程中,发生氧化还原反应的离子方程式为
②将漂白粉加入含
 的废水(密度为
的废水(密度为 )中,发生反应:
)中,发生反应: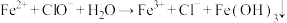 。理论上处理10吨含
。理论上处理10吨含 浓度为
浓度为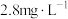 的废水(不考虑其他物质与漂白粉的反应),所需含
的废水(不考虑其他物质与漂白粉的反应),所需含 质量分数为
质量分数为 的漂白粉的质量为
的漂白粉的质量为(3)几种含氯离子的相对能量如下表所示:
| 离子 | Cl—(aq) | ClO——(aq) |  (aq) (aq) |  (aq) (aq) |  (aq) (aq) |
| 相对能量/(kJ·mol-1) | 0 | 60 | 101 | 63 | 38 |
①在上述五种离子中,最稳定的离子是
②反应
 的
的
 。
。③写出
 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:(4)以
 为原料,用
为原料,用 氧化制取
氧化制取 ,可提高效益减少污染。反应如下:
,可提高效益减少污染。反应如下:
上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可使
 转化率接近
转化率接近 ,其基本原理如图所示。过程
,其基本原理如图所示。过程 的反应为
的反应为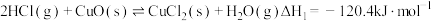 ,过程II反应的热化学方程式为
,过程II反应的热化学方程式为
您最近一年使用:0次
名校
2 . Ⅰ.完成下列问题
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为_______ ;若将100g此盐酸加水稀释至5.82mol/L,则加入水的质量_______ 100g。(填“大于”、“等于”或“小于”);
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:
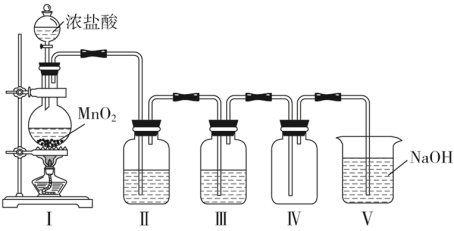
(2)装置Ⅰ中盛装浓盐酸的仪器名称为_______ ;圆底烧瓶中发生反应的离子方程式为_______ ;此反应中HCl体现出性质有_______ 和 _______ 。若生成标准状况下22.4L Cl2,被氧化的HCl分子数是_______ 。
(3)Ⅱ和Ⅲ中盛装的试剂分别是_______ 和_______ 。
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为_______ ;
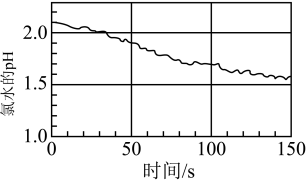
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______
(6)装置Ⅴ中NaOH溶液的作用是吸收尾气,其中发生反应的化学方程式为 _______ 。
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:

(2)装置Ⅰ中盛装浓盐酸的仪器名称为
(3)Ⅱ和Ⅲ中盛装的试剂分别是
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______

| A.光照使氯水中的次氯酸分解为盐酸,溶液的酸性增强 |
| B.随着对氯水光照时间的延长,氯水的漂白性将增强 |
| C.随着对氯水光照时间的延长,溶液中Cl-的浓度不断减小 |
| D.随着对氯水光照时间的延长,氯水颜色逐渐变浅 |
您最近一年使用:0次
3 . 1774年,舍勒在研究软锰矿(主要成分MnO2)时,将它与浓盐酸混合加热,产生了一种黄绿色气体。舍勒的方法沿用至今,实验室用如下装置制取氯气并进行氯气性质探究。
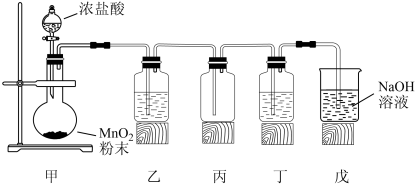
完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是_______ 。盛放浓盐酸的仪器名称为_______ 。
(2)乙为除杂装置,盛有_______ (填写下列字母编号),目的是为了_______ 。
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是_______ 。
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
(5)戊装置的作用是_______ ,该处的化学反应方程式为_______ 。
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是_______ g(保留一位小数)。

完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是
(2)乙为除杂装置,盛有
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
| 实验现象 | 原因 |
| 最初溶液从紫色逐渐变为 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | |
| 然后溶液从无色逐渐变为 | / |
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是
您最近一年使用:0次
2022-01-16更新
|
343次组卷
|
2卷引用:上海市静安区2022届高三一模化学试题
20-21高一上·浙江绍兴·阶段练习
4 . 实验室中盐酸的用途十分广泛,常常用来制备气体
I.实验室用浓盐酸配制250mL 0.3 mol/L的盐酸溶液。
(1)需要用量筒量取浓盐酸(密度为1.2 g/mL, 质量分数为36.5%) 的体积为___________ mL 。
(2)将E步骤补充完整,配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)___________ 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.继续往容量瓶内小心加水,当液面接近容量瓶刻度线1~2cm时,___________ 。
(3)下列操作造成配制的溶液溶度偏高的是___________ (填字母)。
A.配制前,容量瓶中有少量蒸馏水
B.溶解后的溶液未冷却至室温就转入容量瓶中
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时眼睛俯视刻度线
E.加蒸馏水时不慎超过了刻度线
Ⅱ.某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。

(1)A中发生反应的化学方程式为___________ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是___________ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为___________ 。
③装置F中球形干燥管的作用是___________ 。
(3)储气瓶b内盛放的试剂是___________ 。
(4)装置B中反应的离子方程式为___________ 。
I.实验室用浓盐酸配制250mL 0.3 mol/L的盐酸溶液。
(1)需要用量筒量取浓盐酸(密度为1.2 g/mL, 质量分数为36.5%) 的体积为
(2)将E步骤补充完整,配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.继续往容量瓶内小心加水,当液面接近容量瓶刻度线1~2cm时,
(3)下列操作造成配制的溶液溶度偏高的是
A.配制前,容量瓶中有少量蒸馏水
B.溶解后的溶液未冷却至室温就转入容量瓶中
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时眼睛俯视刻度线
E.加蒸馏水时不慎超过了刻度线
Ⅱ.某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。

(1)A中发生反应的化学方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置B中反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 当氨分子中的三个氢原子依次被其它原子或基团取代时,所形成的化合物叫做氨的衍生物。主要有N2H4(肼)、HN3(叠氮化氢,溶于水称为叠氮酸)、NH2OH(羟胺)。水合肼(N2H4·H2O)是制备叠氮化钠(NaN3)的原料,而叠氮化钠又是汽车安全气囊最理想的气体发生剂的原料。下面是工业水合肼法制备叠氮化钠的工艺流程。

资料:①水合肼有毒且不稳定,具有强还原性和强碱性;
②有关物质的物理性质如下表:
回答下列问题:
I.合成水合肼。实验室合成水合肼装置如下图所示,NaClO碱性溶液与尿素CO(NH2)2水溶液在400C以下反应一段时间后,再迅速升温至1100℃继续反应可以制得水合肼。

(1)实验中通过滴液漏斗向三颈瓶中缓慢滴加NaClO碱性溶液,不能反向滴加的原因是______________ ;制取N2H4•H2O的离子方程式为_______________________ 。
II.制备叠氮化钠。实验室可利用下图中所示的装置及药品制备叠氮化钠。

(2)①根据实验发现温度在20℃左右反应的转化率最高,因此可采取的措施是_______________ ;流程中蒸馏A溶液时,装置中旋塞K1、K2、K3的开关情况是_______________________ 。
②写出该方法制备叠氮化钠的化学方程式:________________________ 。
(3)流程中由B溶液获得叠氮化钠产品的实验步骤为____________________ ,减压过滤,晶体用乙醇洗涤2〜3次后,干燥。
(4)化工生产中,多余的叠氮化钠常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理6.5gNaN3,理论上需加入0.5mol•L的NaClO溶液_____________ mL。
III.羟胺(NH2OH)是一种还原剂,可以通过下列过程得到:乙烯和N2O4气体混合后,光照,发生加成反应,得到化合物A。A结构对称,所有相同元素的原子化学环境相同。A在某浓度的硫酸溶液中回馏,可得到化合物B,同时得到CO和CO2组成的混合气体(相对氢气密度为18)。经分析,B为不含碳元素的硫酸盐,其硫和氧元素的质量分数分别为19.51%和58.54%。若将A换成CH3CH2NO2进行类似的反应,也能得到B,但没有气体放出。B在液氨中即得到NH2OH。
(5)NH2OH具有弱碱性,可与酸反应生成盐,该盐阳离子的电子式为_______________ 。
(6)写出A→B的化学方程式________________________ 。

资料:①水合肼有毒且不稳定,具有强还原性和强碱性;
②有关物质的物理性质如下表:
| 物质 | 甲醇 | 水合肼 | 亚硝酸甲酯 | 叠氮化钠 |
| 熔点(℃) | -97 | -40 | -17 | 275(410℃:易分解) |
| 沸点(℃) | 64.7 | 118.5 | -12 | — |
回答下列问题:
I.合成水合肼。实验室合成水合肼装置如下图所示,NaClO碱性溶液与尿素CO(NH2)2水溶液在400C以下反应一段时间后,再迅速升温至1100℃继续反应可以制得水合肼。

(1)实验中通过滴液漏斗向三颈瓶中缓慢滴加NaClO碱性溶液,不能反向滴加的原因是
II.制备叠氮化钠。实验室可利用下图中所示的装置及药品制备叠氮化钠。

(2)①根据实验发现温度在20℃左右反应的转化率最高,因此可采取的措施是
②写出该方法制备叠氮化钠的化学方程式:
(3)流程中由B溶液获得叠氮化钠产品的实验步骤为
(4)化工生产中,多余的叠氮化钠常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理6.5gNaN3,理论上需加入0.5mol•L的NaClO溶液
III.羟胺(NH2OH)是一种还原剂,可以通过下列过程得到:乙烯和N2O4气体混合后,光照,发生加成反应,得到化合物A。A结构对称,所有相同元素的原子化学环境相同。A在某浓度的硫酸溶液中回馏,可得到化合物B,同时得到CO和CO2组成的混合气体(相对氢气密度为18)。经分析,B为不含碳元素的硫酸盐,其硫和氧元素的质量分数分别为19.51%和58.54%。若将A换成CH3CH2NO2进行类似的反应,也能得到B,但没有气体放出。B在液氨中即得到NH2OH。
(5)NH2OH具有弱碱性,可与酸反应生成盐,该盐阳离子的电子式为
(6)写出A→B的化学方程式
您最近一年使用:0次
6 . 亚氯酸钠(NaClO2)是一种高效含氯消毒剂和漂白剂,主要用于自来水、污水等水环境的杀菌消毒,也常用作纸浆、砂糖、油脂的漂白剂。图为目前生产亚氯酸钠的流程之一(夹持装置省略),所得NaClO2具有纯度高的优点。

已知:NaClO2饱和溶液在低于38℃时会析出NaClO•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
试回答下列问题:
(1)仪器a的名称为___________ 。
(2)装置A用来制取ClO2,发生反应的离子方程式为___________ 。
(3)研究测得C装置吸收液中的c(NaOH)与 对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=
对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=___________ mol/L, =
=___________ 。

(4)C装置采用“冰水浴”的目的是___________ 。
(5)充分反应后,为从产品溶液中获取NaClO2晶体,从下列选项中选出合理的操作并排序:( )→( )→( )→干燥,___________
a.趁热过滤 b.50℃水洗涤 c.加热蒸发结晶 d.冰水洗涤 e.55℃恒温减压蒸发结晶
(6)在化学定分析中为了方便计算,常用滴定度(T)表示标准液的滴定能力,是指每毫升标准溶液相当于样品中所含被测物质的质量。准确称取一定质量的NaClO2(摩尔质量为Mg/mol)样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应: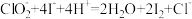 ,得待测溶液。取一定量消耗待测溶液,以淀粉溶液作指示剂,消耗
,得待测溶液。取一定量消耗待测溶液,以淀粉溶液作指示剂,消耗
 标准液V mL(已知:
标准液V mL(已知: )。则滴定度T=
)。则滴定度T=___________ g/mL。

已知:NaClO2饱和溶液在低于38℃时会析出NaClO•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
试回答下列问题:
(1)仪器a的名称为
(2)装置A用来制取ClO2,发生反应的离子方程式为
(3)研究测得C装置吸收液中的c(NaOH)与
 对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)=
对粗产品中NaClO2含量的影响如图所示。则最佳条件为c(NaOH)= =
=
(4)C装置采用“冰水浴”的目的是
(5)充分反应后,为从产品溶液中获取NaClO2晶体,从下列选项中选出合理的操作并排序:( )→( )→( )→干燥,
a.趁热过滤 b.50℃水洗涤 c.加热蒸发结晶 d.冰水洗涤 e.55℃恒温减压蒸发结晶
(6)在化学定分析中为了方便计算,常用滴定度(T)表示标准液的滴定能力,是指每毫升标准溶液相当于样品中所含被测物质的质量。准确称取一定质量的NaClO2(摩尔质量为Mg/mol)样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:
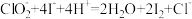 ,得待测溶液。取一定量消耗待测溶液,以淀粉溶液作指示剂,消耗
,得待测溶液。取一定量消耗待测溶液,以淀粉溶液作指示剂,消耗
 标准液V mL(已知:
标准液V mL(已知: )。则滴定度T=
)。则滴定度T=
您最近一年使用:0次
2021-05-17更新
|
896次组卷
|
6卷引用:浙江省金华市义乌市2021届高三适应性考试化学试题
浙江省金华市义乌市2021届高三适应性考试化学试题(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)福建省厦门外国语学校石狮分校2021-2022学年高三上学期第一次月考化学试题河北省石家庄市第二中学2021-2022学年高三上学期10月第二次考试化学试题(已下线)2022年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A浙江省乐清市知临中学2022-2023学年高二下学期6月期末考试化学试题
2019高三·全国·专题练习
7 . 已知某合金中除铝外还可能含有铁和铜中的一种或两种,所含金属的质量分数都在5%以上。请设计合理的实验探究该合金中铁、铜的存在。
限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、胶头滴管、药匙、酒精灯、坩埚、坩埚钳、1mol/L硫酸、新制氯水、2mol/LNaOH溶液、KSCN溶液。
完成以下实验探究过程:
(1)提出假设
假设1 该合金中除Al外还含有________ 元素;
假设2 该合金中除Al外还含有________ 元素;
假设3 该合金中除Al外还含有Fe、Cu元素。
(2)设计实验方案
基于假设3,设计出合理的实验方案。
(3)实验过程
根据(2)的实验方案,完成下列实验操作、预期现象与结论。
限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、胶头滴管、药匙、酒精灯、坩埚、坩埚钳、1mol/L硫酸、新制氯水、2mol/LNaOH溶液、KSCN溶液。
完成以下实验探究过程:
(1)提出假设
假设1 该合金中除Al外还含有
假设2 该合金中除Al外还含有
假设3 该合金中除Al外还含有Fe、Cu元素。
(2)设计实验方案
基于假设3,设计出合理的实验方案。
(3)实验过程
根据(2)的实验方案,完成下列实验操作、预期现象与结论。
| 编号 | 实验操作 | 预期现象与结论 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
您最近一年使用:0次
8 . 某化学兴趣小组探究氯与水反应的热效应及所得溶液氯元素含量,查阅大量资料并做下列实验探究验证
实验Ⅰ:在通风橱内向装有80mL蒸馏水的锥形瓶 瓶口塞上棉花团
瓶口塞上棉花团 中鼓入氯气,至溶液中pH没有明显变化停止通入氯气,使用数据采集器,测定在此过程中溶液的温度及pH变化,具体数据如图所示:
中鼓入氯气,至溶液中pH没有明显变化停止通入氯气,使用数据采集器,测定在此过程中溶液的温度及pH变化,具体数据如图所示:
实验Ⅱ:对20mL饱和氯水加热,测出c(Cl-)、pH及温度变化如图2所示。
实验Ⅲ:采用莫尔法测定氯水中氯元素的含量。此法是以 为指示剂,用
为指示剂,用 标准溶液进行滴定。其实验步骤如下:
标准溶液进行滴定。其实验步骤如下:
①准确移取25.00ml氯水试样3份,分别置于锥形瓶中,再分别加入25.00ml水;
②向试样中加入足量的 溶液;
溶液;
③除去过量的 ,冷却;
,冷却;
④调整溶液的pH,再加入
 溶液,在不断摇动下用
溶液,在不断摇动下用
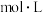
 标准溶液滴定至溶液呈砖红色
标准溶液滴定至溶液呈砖红色
 砖红色
砖红色 ]
]
⑤重复上述实验,测得消耗 标准溶液体积的平均值为vmL
标准溶液体积的平均值为vmL
回答下列问题:
(1)氯气在295K、100Kpa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。该反应的离子方程式为______ ;估算该离子反应的平衡常数______
(2)根据实验Ⅰ测定结果判断氯气与水的反应是______  填“吸热反应”或“放热反应”
填“吸热反应”或“放热反应” 理由是
理由是______
(2)分析实验Ⅱ图,小组同学推测产生该结果的原因可能是多种反应造成的,下列叙述合理的是______
A.升温,氯气挥发导致c(Cl-)减小
B.对于 和
和 的反应,升温平衡逆向移动,c(Cl-)减小,pH减小
的反应,升温平衡逆向移动,c(Cl-)减小,pH减小
C.升温,促进次氯酸分解2HClO 2HCl+O2↑
2HCl+O2↑
D.升温,可能发生3HClO 2HCl+HClO3(强酸) ,使得pH减小
2HCl+HClO3(强酸) ,使得pH减小
(4)实验Ⅲ步骤3中加足量的 溶液,目的是
溶液,目的是______
(5)用 标准溶液滴定氯离子达到化学计量点时,
标准溶液滴定氯离子达到化学计量点时, ,若此时要求不生成
,若此时要求不生成 沉淀,则
沉淀,则 最大不能超过
最大不能超过______  已知:
已知: ,
,
(6)计算实验Ⅲ氯水中氯元素的含量,列出算式:______ 
实验Ⅰ:在通风橱内向装有80mL蒸馏水的锥形瓶
 瓶口塞上棉花团
瓶口塞上棉花团 中鼓入氯气,至溶液中pH没有明显变化停止通入氯气,使用数据采集器,测定在此过程中溶液的温度及pH变化,具体数据如图所示:
中鼓入氯气,至溶液中pH没有明显变化停止通入氯气,使用数据采集器,测定在此过程中溶液的温度及pH变化,具体数据如图所示:
实验Ⅱ:对20mL饱和氯水加热,测出c(Cl-)、pH及温度变化如图2所示。

实验Ⅲ:采用莫尔法测定氯水中氯元素的含量。此法是以
 为指示剂,用
为指示剂,用 标准溶液进行滴定。其实验步骤如下:
标准溶液进行滴定。其实验步骤如下:①准确移取25.00ml氯水试样3份,分别置于锥形瓶中,再分别加入25.00ml水;
②向试样中加入足量的
 溶液;
溶液;③除去过量的
 ,冷却;
,冷却;④调整溶液的pH,再加入

 溶液,在不断摇动下用
溶液,在不断摇动下用
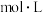
 标准溶液滴定至溶液呈砖红色
标准溶液滴定至溶液呈砖红色
 砖红色
砖红色 ]
]⑤重复上述实验,测得消耗
 标准溶液体积的平均值为vmL
标准溶液体积的平均值为vmL回答下列问题:
(1)氯气在295K、100Kpa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。该反应的离子方程式为
(2)根据实验Ⅰ测定结果判断氯气与水的反应是
 填“吸热反应”或“放热反应”
填“吸热反应”或“放热反应” 理由是
理由是(2)分析实验Ⅱ图,小组同学推测产生该结果的原因可能是多种反应造成的,下列叙述合理的是
A.升温,氯气挥发导致c(Cl-)减小
B.对于
 和
和 的反应,升温平衡逆向移动,c(Cl-)减小,pH减小
的反应,升温平衡逆向移动,c(Cl-)减小,pH减小C.升温,促进次氯酸分解2HClO
 2HCl+O2↑
2HCl+O2↑D.升温,可能发生3HClO
 2HCl+HClO3(强酸) ,使得pH减小
2HCl+HClO3(强酸) ,使得pH减小(4)实验Ⅲ步骤3中加足量的
 溶液,目的是
溶液,目的是(5)用
 标准溶液滴定氯离子达到化学计量点时,
标准溶液滴定氯离子达到化学计量点时, ,若此时要求不生成
,若此时要求不生成 沉淀,则
沉淀,则 最大不能超过
最大不能超过 已知:
已知: ,
,
(6)计算实验Ⅲ氯水中氯元素的含量,列出算式:

您最近一年使用:0次
9 . CuCl广泛应用于化工和印染等行业。在实验室中模拟热分解CuCl2·xH2O制备CuCl的原理和实验装置如下:
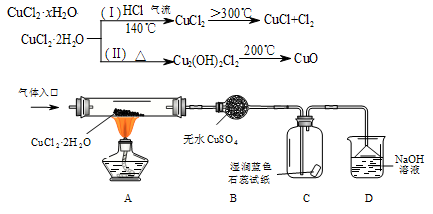
完成下列填空:
(1)在实验(Ⅰ)过程中,观察到B中固体由白色变为蓝色,C中产生的现象是__________ ,导致该现象的物质是________________________ 。
(2)装置D的作用是___________________________________ ,其中发生氧化还原反应的化学方程式是_____________________________________ 。
(3)反应结束后,CuCl产品中可能存在少量的CuCl2或CuO杂质。
①若杂质是CuCl2,则原因是_________________________________________ 。
②若杂质是CuO,则原因是__________________________________________ 。
(4)根据实验(Ⅱ),测定CuCl2·xH2O中结晶水的含量。取CuCl2·xH2O样品1.692g,经过3次灼烧、冷却、称量,得到黑色固体的质量数据如下:
则x=_____________ (保留2位小数)。

完成下列填空:
(1)在实验(Ⅰ)过程中,观察到B中固体由白色变为蓝色,C中产生的现象是
(2)装置D的作用是
(3)反应结束后,CuCl产品中可能存在少量的CuCl2或CuO杂质。
①若杂质是CuCl2,则原因是
②若杂质是CuO,则原因是
(4)根据实验(Ⅱ),测定CuCl2·xH2O中结晶水的含量。取CuCl2·xH2O样品1.692g,经过3次灼烧、冷却、称量,得到黑色固体的质量数据如下:
| 称 量 | 第1次 | 第2次 | 第3次 |
| 质量(g) | 0.820g | 0.800g | 0.800g |
则x=
您最近一年使用:0次
2018-05-02更新
|
451次组卷
|
2卷引用:【全国区级联考】上海市金山区2018届高三下学期质量监控(二模)化学试题



