名校
1 . 核心知识的准确记忆、巩固是学好化学最重要、最基础的环节。按要求回答:
(1)气体摩尔体积的单位是__________ ;
(2)物质的量浓度(c)与质量分数( )的换算公式:
)的换算公式: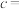
__________ ;(摩尔质量用M表示,密度 的单位为
的单位为 )
)
(3)蒸馏装置中温度计水银球的位置处于__________ ;
(4)容量瓶和分液漏斗使用前都必须进行的操作是__________ ;
(5)利用焰色反应检验物质,钾元素的焰色是__________ ;
(6) 的电离方程式为
的电离方程式为__________ ;
(7)氯气与水反应的化学方程式为__________ ;
不考虑物质挥发,新制氯水久置后导电能力变__________ (填“强或弱”)。
(8)下列溶液中 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。
(1)气体摩尔体积的单位是
(2)物质的量浓度(c)与质量分数(
 )的换算公式:
)的换算公式: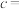
 的单位为
的单位为 )
)(3)蒸馏装置中温度计水银球的位置处于
(4)容量瓶和分液漏斗使用前都必须进行的操作是
(5)利用焰色反应检验物质,钾元素的焰色是
(6)
 的电离方程式为
的电离方程式为(7)氯气与水反应的化学方程式为
不考虑物质挥发,新制氯水久置后导电能力变
(8)下列溶液中
 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。A. 的 的 溶液 溶液 | B. 的 的 溶液 溶液 |
C.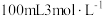 的 的 溶液 溶液 | D. 的 的 溶液 溶液 |
您最近一年使用:0次
解题方法
2 . 下列关于氯及其化合物的叙述中,正确的是
| A.用自来水配制硝酸银溶液不会引起变质 |
| B.铁在少量Cl2中燃烧,生成氯化铁 |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有HClO |
| D.等物质的量的Na2O与Na2O2与等量且足量的水反应得到溶液的质量分数不同 |
您最近一年使用:0次
名校
解题方法
3 . 用氯气与石灰乳充分反应可以制取漂白粉,使用漂白粉作漂白剂比使用氯水更好的理由是
| A.漂白粉更容易与水反应 | B.漂白粉相对稳定且便于贮存 |
C.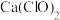 比HClO漂白快 比HClO漂白快 | D.漂白粉中的氯元素的质量分数更大 |
您最近一年使用:0次
名校
解题方法
4 . 根据下列图示所得出的结论正确的是


| A.由图甲中能量变化曲线可知该反应是吸热反应 |
B.图乙表示溶液碱性越强, 消耗速率越慢 消耗速率越慢 |
C.由图丙可知,40℃时 溶液的质量分数大于NaCl溶液的质量分数 溶液的质量分数大于NaCl溶液的质量分数 |
| D.由图丁可知,氯水在光照过程中pH逐渐减小,溶液中Cl-浓度逐渐增大 |
您最近一年使用:0次
解题方法
5 . 氯水及氯的许多化合物是高效广谱的消毒剂,同时又是生产中重要的化工原料,根据所学知识,回答下列问题:
(1)新制的氯水呈淡黄色,向氯水中滴入几滴AgNO3溶液,现象是___ ,说明氯水中有存在____ 。
(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是____ ;为了较长时间保持NaClO溶液的杀菌能力,NaClO溶液应密闭避光保存,原因是___ 。生活中,若不小心将“84”消毒液与洁厕剂(含有盐酸)混合后,易生成___ 气体(填化学式),能使人中毒。
(3)近些年来,科学家提出使用ClO2对自来水进行消毒。以NaClO2和稀盐酸为原料可制备ClO2,写出该反应的化学方程式:___ ,在上述过程中被氧化和被还原的物质的物质的量之比为____ 。
(1)新制的氯水呈淡黄色,向氯水中滴入几滴AgNO3溶液,现象是
(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是
(3)近些年来,科学家提出使用ClO2对自来水进行消毒。以NaClO2和稀盐酸为原料可制备ClO2,写出该反应的化学方程式:
您最近一年使用:0次
6 . 氯离子是维持血清电解质平衡和酸碱平衡重要物质,人体中氯的正常值范围是96~106mmol∙L−1,氯及其化合物在生活中也有着重要用途。下图为氯及其化合物的“价—类”二维图。

(1)若经体检测得某人体内 含量为
含量为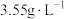 ,此测量值
,此测量值_______ (填“处于”或“不处于”)人体中氯的正常值范围内。
(2)A物质光照分解的产物可以设计成数字化实验。实验步骤如下:
I.将 传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
II.将三种传感器分别插入盛有氯水的广口瓶中;
III.用强光照射氯水,同时开始采集数据。
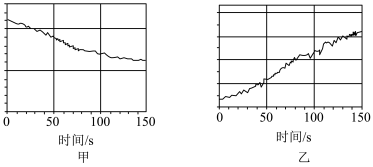
图甲和图乙的纵坐标可能分别为_______ (填序号)。
A.氯水的 、离子浓度 B.氯离子浓度、氯水的
、离子浓度 B.氯离子浓度、氯水的
C.氧气的体积分数、氯离子浓度 D.氧气的体积分数、氯水的
该过程的化学反应方程式为_______ 。
(3)某同学想利用以下试剂探究 的化学性质:
的化学性质:
A. B.
B. C.
C. D.
D.
i.从物质类别的视角, 属于强酸,可能与
属于强酸,可能与_______ 发生反应(填序号)。
ii.从元素价态的视角, 具有氧化性,可能与
具有氧化性,可能与_______ 发生反应(填序号)。
(4)碘是生命体中的必需元素,碘及其化合物在生活中也有重要的用途。实验室制取少量 可用如下方法:
可用如下方法: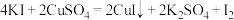 。请根据方程式回答问题:
。请根据方程式回答问题:
①从上述反应中可以判断 和
和 氧化性的关系为
氧化性的关系为_______ >_______ 。
②反应有 生成,转移
生成,转移_______  电子。
电子。

(1)若经体检测得某人体内
 含量为
含量为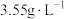 ,此测量值
,此测量值(2)A物质光照分解的产物可以设计成数字化实验。实验步骤如下:
I.将
 传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;II.将三种传感器分别插入盛有氯水的广口瓶中;
III.用强光照射氯水,同时开始采集数据。

图甲和图乙的纵坐标可能分别为
A.氯水的
 、离子浓度 B.氯离子浓度、氯水的
、离子浓度 B.氯离子浓度、氯水的
C.氧气的体积分数、氯离子浓度 D.氧气的体积分数、氯水的

该过程的化学反应方程式为
(3)某同学想利用以下试剂探究
 的化学性质:
的化学性质:A.
 B.
B. C.
C. D.
D.
i.从物质类别的视角,
 属于强酸,可能与
属于强酸,可能与ii.从元素价态的视角,
 具有氧化性,可能与
具有氧化性,可能与(4)碘是生命体中的必需元素,碘及其化合物在生活中也有重要的用途。实验室制取少量
 可用如下方法:
可用如下方法: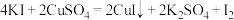 。请根据方程式回答问题:
。请根据方程式回答问题:①从上述反应中可以判断
 和
和 氧化性的关系为
氧化性的关系为②反应有
 生成,转移
生成,转移 电子。
电子。
您最近一年使用:0次
7 . 下列说法正确的是
| A.纯碱因碱性过强,不可用于食品工业 |
| B.分子筛只能用于气体混合物的分离、提纯 |
| C.新制氯水呈酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| D.合金的性能可以通过所添加合金元素的种类、含量和生成合金的条件等加以调节 |
您最近一年使用:0次
解题方法
8 . 用自来水养鱼时,将水注入鱼缸前需在阳光下暴晒一段时间,这样做的目的是
| A.分解水中的次氯酸 | B.增加氧气的含量 | C.杀菌消毒 | D.使水的温度升高 |
您最近一年使用:0次
9 . 按要求填空:
(1)写出新制氯水中含量最多的微粒的化学式_________________ (水分子除外)
(2)写出漂白粉中有效成分的名称__________________
(3)描述检验溶液中K+离子的实验操作过程 _____________
(4)配平下列化学方程式
( ) Cu+( ) HNO3(稀)=( ) Cu(NO3)2+( ) NO↑+( ) H2O
(5)按照物质的分类,次磷酸(H3PO2)属于二元酸,其与足量的NaOH溶液反应的化学方程式为______
(1)写出新制氯水中含量最多的微粒的化学式
(2)写出漂白粉中有效成分的名称
(3)描述检验溶液中K+离子的
(4)配平下列化学方程式
(5)按照物质的分类,次磷酸(H3PO2)属于二元酸,其与足量的NaOH溶液反应的化学方程式为
您最近一年使用:0次
真题
10 . 印染工业常用亚氯酸钠(NaClO2)漂白织物。亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2—,其中HClO2是漂白剂的有效成分,ClO2是有毒气体。各组分含量随pH变化情况如图所示,由图可知,使用该漂白剂的最佳pH为


| A.3.0 | B.4.0—4.5 | C.6.5—7.0 | D.9.0 |
您最近一年使用:0次
2019-01-30更新
|
472次组卷
|
6卷引用:2008年普通高等学校招生统一考试综合试题(理科使用)化学部分(上海卷)
2008年普通高等学校招生统一考试综合试题(理科使用)化学部分(上海卷)(已下线)2011-2012学年北京市朝阳区高一下学期期末统一考试化学试卷2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷第 25 届全国高中学生化学竞赛(江苏赛区)初赛试题北京市海淀区中国地质大学附属中学2019-2020学年高一上学期9月月考化学试卷(已下线)微项目 科学使用含氯消毒剂-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)



