名校
1 . 下列有关物质的性质与用途,不具有对应关系的是
| A.Na2O2为淡黄色固体,可用于潜艇中的供氧剂 |
| B.Na2CO3溶液显碱性,可用于除器皿表面的油污 |
| C.A12O3的熔点高,常用作耐火、耐高温材料 |
| D.氯水具有强氧化性,Fe2+在氯水中能被氧化成Fe3+ |
您最近一年使用:0次
解题方法
2 . 下列有关物质性质与用途对应关系不正确 的是( )
| A.NaHCO3受热易分解,可用于制胃酸中和剂 |
| B.CaO能与SO2反应,可作为工业废气处理时的脱硫剂 |
| C.硅的导电性介于导体和绝缘体之间,可用于制造计算机硅芯片的材料 |
| D.饱和氯水既有酸性又有漂白性,加入适量NaHCO3固体,其漂白性增强 |
您最近一年使用:0次
解题方法
3 . 下列有关物质性质与用途具有对应关系的是
| A.氨气具有还原性,可用作制冷剂 |
| B.次氯酸具有弱酸性,可用作有色物质的漂白剂 |
| C.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
| D.碳酸钠溶液显碱性,可用其热溶液除去金属餐具表面油污 |
您最近一年使用:0次
2020-01-19更新
|
154次组卷
|
3卷引用:江苏省无锡市普通高中2019-2020学年高三上学期期终调研试化学试题
名校
解题方法
4 . 下列实验操作及现象与结论之间对应关系错误的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫色 | I2在CCl4中的溶解度大于在水中的溶解度 |
| B | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| C | 探究新制饱和氯水成分的实验时,向氯水中滴加硝酸酸化的AgNO3溶液,有白色沉淀生成 | 氯水中含有Cl- |
| D | 向某溶液中滴加NaOH浓溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象与新制氯水中的某些成分(括号内物质)对应关系不正确的是
A.使红色布条褪色( ) ) |
B.氯水呈黄绿色( ) ) |
C.向 固体加入新制氯水,有无色气泡( 固体加入新制氯水,有无色气泡( ) ) |
D.滴加 溶液生成白色沉淀( 溶液生成白色沉淀( ) ) |
您最近一年使用:0次
6 . 验证次氯酸光照分解的产物可以设计成数字化实验(同时开始采集数据),此实验可以测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数的变化。三者变化趋势如图所示,回答下列问题:
(1)如图所示:
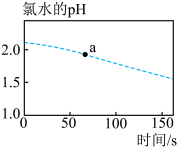
①新制氯水中所含微粒的种类有___________ 种。
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为___________ 。
③0~150s的过程中,氯水的pH逐渐减小的原因为___________ (用离子方程式表示)。
(2)如图所示:
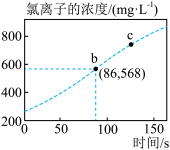
①b点对应的溶液中,所含氯离子的浓度为___________  。
。
②c点对应的溶液中,加入少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(3)如图所示:
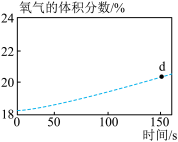
①写出一种 的用途:
的用途:___________ 。
②相同原子个数的 与
与 的质量之比为
的质量之比为___________ 。
③标准状况下,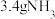 与
与___________ g 所含的电子总数相同。
所含的电子总数相同。
(1)如图所示:

①新制氯水中所含微粒的种类有
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为
③0~150s的过程中,氯水的pH逐渐减小的原因为
(2)如图所示:

①b点对应的溶液中,所含氯离子的浓度为
 。
。②c点对应的溶液中,加入少量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)如图所示:

①写出一种
 的用途:
的用途:②相同原子个数的
 与
与 的质量之比为
的质量之比为③标准状况下,
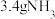 与
与 所含的电子总数相同。
所含的电子总数相同。
您最近一年使用:0次
7 . 氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
(2)反应: 。该反应中氧化产物为
。该反应中氧化产物为_______ 。
(3)已知下列三个氧化还原反应:
① ;
;
② ;
;
③ (浓)
(浓) 。
。
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的_______ (从上述三个反应中选择)作氧化剂。
(4)无水情况下, 可以和
可以和 发生如下反应:
发生如下反应:
_______ _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目_______ 。
(5)向含有 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是_______ (填序号)。
①氧化性: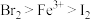
②原溶液中 一定被氧化
一定被氧化
③通入氯气后,原溶液中的 定被氧化
定被氧化
④不能确定通入氯气后的溶液中是否还存在
(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
(7) 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为_______ 。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
A.淡黄色 固体露置于空气中,逐渐变成白色 固体露置于空气中,逐渐变成白色 |
| B.用强光照射氯水,一段时间后溶液变成无色 |
| C.向氯水中滴加KI溶液,溶液变成棕黄色 |
D.向 溶液中滴加 溶液中滴加 溶液,产生红褐色沉淀 溶液,产生红褐色沉淀 |
 。该反应中氧化产物为
。该反应中氧化产物为(3)已知下列三个氧化还原反应:
①
 ;
;②
 ;
;③
 (浓)
(浓) 。
。若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的(4)无水情况下,
 可以和
可以和 发生如下反应:
发生如下反应:_______
 _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目
(5)向含有
 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是①氧化性:
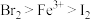
②原溶液中
 一定被氧化
一定被氧化③通入氯气后,原溶液中的
 定被氧化
定被氧化④不能确定通入氯气后的溶液中是否还存在

(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
A. | B. |
C. | D. |
 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为
您最近一年使用:0次
8 . 氯及其化合物在生产生活中都有重要的用途,下列关于氯及其化合物说法正确的是
| A.自来水厂用Cl2消毒,是因为Cl2有毒 |
| B.Cl2因具有强氧化性,所以不能用钢瓶盛放 |
| C.可以将氯气通入氢氧化钠溶液中制得漂白粉 |
| D.ClO2可用于杀菌消毒 |
您最近一年使用:0次
名校
解题方法
9 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的化学方程式___________ ;实验室用___________ 除去混在氯气中的氯化氢杂质,用___________ 除去混在里面的水蒸气;
②写出次氯酸分解的化学反应方程式___________ ;新制氯水中使其呈现黄绿色的微粒是___________ ;使紫色石蕊溶液显红色的微粒是___________ ;能使红色布条褪色的微粒是___________ 。(填化学式)
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):________ ;
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应_____________ 。
______Cl2+______OH-=______Cl-+1ClO-+3ClO +______H2O
+______H2O
(1)①写出实验室中制取氯气的化学方程式
②写出次氯酸分解的化学反应方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应______Cl2+______OH-=______Cl-+1ClO-+3ClO
 +______H2O
+______H2O
您最近一年使用:0次
10 . 氯离子是维持血清电解质平衡和酸碱平衡重要物质,人体中氯的正常值范围是96~106mmol∙L−1,氯及其化合物在生活中也有着重要用途。下图为氯及其化合物的“价—类”二维图。

(1)若经体检测得某人体内 含量为
含量为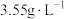 ,此测量值
,此测量值_______ (填“处于”或“不处于”)人体中氯的正常值范围内。
(2)A物质光照分解的产物可以设计成数字化实验。实验步骤如下:
I.将 传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
II.将三种传感器分别插入盛有氯水的广口瓶中;
III.用强光照射氯水,同时开始采集数据。
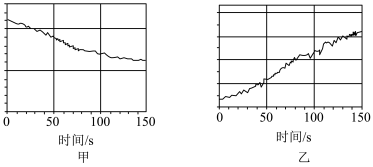
图甲和图乙的纵坐标可能分别为_______ (填序号)。
A.氯水的 、离子浓度 B.氯离子浓度、氯水的
、离子浓度 B.氯离子浓度、氯水的
C.氧气的体积分数、氯离子浓度 D.氧气的体积分数、氯水的
该过程的化学反应方程式为_______ 。
(3)某同学想利用以下试剂探究 的化学性质:
的化学性质:
A. B.
B. C.
C. D.
D.
i.从物质类别的视角, 属于强酸,可能与
属于强酸,可能与_______ 发生反应(填序号)。
ii.从元素价态的视角, 具有氧化性,可能与
具有氧化性,可能与_______ 发生反应(填序号)。
(4)碘是生命体中的必需元素,碘及其化合物在生活中也有重要的用途。实验室制取少量 可用如下方法:
可用如下方法: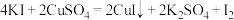 。请根据方程式回答问题:
。请根据方程式回答问题:
①从上述反应中可以判断 和
和 氧化性的关系为
氧化性的关系为_______ >_______ 。
②反应有 生成,转移
生成,转移_______  电子。
电子。

(1)若经体检测得某人体内
 含量为
含量为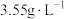 ,此测量值
,此测量值(2)A物质光照分解的产物可以设计成数字化实验。实验步骤如下:
I.将
 传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;
传感器、氢离子传感器、氧气传感器分别与数据采集器、计算机连接;II.将三种传感器分别插入盛有氯水的广口瓶中;
III.用强光照射氯水,同时开始采集数据。

图甲和图乙的纵坐标可能分别为
A.氯水的
 、离子浓度 B.氯离子浓度、氯水的
、离子浓度 B.氯离子浓度、氯水的
C.氧气的体积分数、氯离子浓度 D.氧气的体积分数、氯水的

该过程的化学反应方程式为
(3)某同学想利用以下试剂探究
 的化学性质:
的化学性质:A.
 B.
B. C.
C. D.
D.
i.从物质类别的视角,
 属于强酸,可能与
属于强酸,可能与ii.从元素价态的视角,
 具有氧化性,可能与
具有氧化性,可能与(4)碘是生命体中的必需元素,碘及其化合物在生活中也有重要的用途。实验室制取少量
 可用如下方法:
可用如下方法: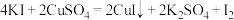 。请根据方程式回答问题:
。请根据方程式回答问题:①从上述反应中可以判断
 和
和 氧化性的关系为
氧化性的关系为②反应有
 生成,转移
生成,转移 电子。
电子。
您最近一年使用:0次



