1 . 消毒液在我们日常生活中必不可少,请结合相关知识回答下列问题。
(1)生产消毒液是将氯气通入 溶液中,发生反应的化学方程式为:
溶液中,发生反应的化学方程式为:___________ 。
(2)取少量消毒液滴加 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有___________ 离子。向氯水中滴加紫色石蕊试剂的现象:___________ 。
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,该物质的化学式:___________ ;该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学方程式:___________ 。
(1)生产消毒液是将氯气通入
 溶液中,发生反应的化学方程式为:
溶液中,发生反应的化学方程式为:(2)取少量消毒液滴加
 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,该物质的化学式:
您最近一年使用:0次
解题方法
2 . 氯水漂白性不断减弱的原因:__________ 。
您最近一年使用:0次
3 . 验证次氯酸光照分解的产物可以设计成数字化实验(同时开始采集数据),此实验可以测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数的变化。三者变化趋势如图所示,回答下列问题:
(1)如图所示:
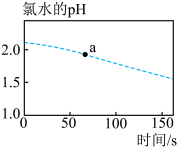
①新制氯水中所含微粒的种类有___________ 种。
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为___________ 。
③0~150s的过程中,氯水的pH逐渐减小的原因为___________ (用离子方程式表示)。
(2)如图所示:
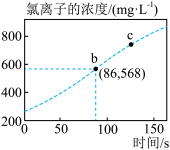
①b点对应的溶液中,所含氯离子的浓度为___________  。
。
②c点对应的溶液中,加入少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(3)如图所示:
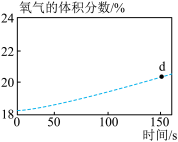
①写出一种 的用途:
的用途:___________ 。
②相同原子个数的 与
与 的质量之比为
的质量之比为___________ 。
③标准状况下,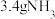 与
与___________ g 所含的电子总数相同。
所含的电子总数相同。
(1)如图所示:

①新制氯水中所含微粒的种类有
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为
③0~150s的过程中,氯水的pH逐渐减小的原因为
(2)如图所示:

①b点对应的溶液中,所含氯离子的浓度为
 。
。②c点对应的溶液中,加入少量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)如图所示:

①写出一种
 的用途:
的用途:②相同原子个数的
 与
与 的质量之比为
的质量之比为③标准状况下,
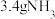 与
与 所含的电子总数相同。
所含的电子总数相同。
您最近一年使用:0次
名校
4 . 数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。如图是数字化实验得到的光照过程中氯水中的溶液pH、氯离子浓度、氧气体积的变化情况。

(1)若在光照开始时,向氯水中滴入2滴紫色石蕊试液,溶液会呈现___________颜色。
(2)图丙中 浓度增大的原因是
浓度增大的原因是___________ (用化学方程式表达)。
(3)从图中相关曲线变化可知,在光照过程中溶液的酸性逐渐___________ ,溶液导电能力___________ 。
(4) 通入石灰乳可以制得一种消毒剂,这种消毒剂俗称
通入石灰乳可以制得一种消毒剂,这种消毒剂俗称___________ ,该反应的化学方程式为:___________ 。
(5) 是一种广谱型的消毒剂,根据世界环保联盟的要求
是一种广谱型的消毒剂,根据世界环保联盟的要求 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中,还原产物是
酸化后反应制得,在以上反应中,还原产物是___________ ;还原剂和氧化剂的物质的量之比为___________ 。

(1)若在光照开始时,向氯水中滴入2滴紫色石蕊试液,溶液会呈现___________颜色。
| A.紫色 | B.红色 | C.蓝色 | D.浅黄绿色 |
(2)图丙中
 浓度增大的原因是
浓度增大的原因是(3)从图中相关曲线变化可知,在光照过程中溶液的酸性逐渐
(4)
 通入石灰乳可以制得一种消毒剂,这种消毒剂俗称
通入石灰乳可以制得一种消毒剂,这种消毒剂俗称(5)
 是一种广谱型的消毒剂,根据世界环保联盟的要求
是一种广谱型的消毒剂,根据世界环保联盟的要求 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中,还原产物是
酸化后反应制得,在以上反应中,还原产物是
您最近一年使用:0次
5 . 氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
(2)反应: 。该反应中氧化产物为
。该反应中氧化产物为_______ 。
(3)已知下列三个氧化还原反应:
① ;
;
② ;
;
③ (浓)
(浓) 。
。
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的_______ (从上述三个反应中选择)作氧化剂。
(4)无水情况下, 可以和
可以和 发生如下反应:
发生如下反应:
_______ _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目_______ 。
(5)向含有 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是_______ (填序号)。
①氧化性: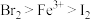
②原溶液中 一定被氧化
一定被氧化
③通入氯气后,原溶液中的 定被氧化
定被氧化
④不能确定通入氯气后的溶液中是否还存在
(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
(7) 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为_______ 。
(1)下列实验过程中的颜色变化,与氧化还原反应有关的是_______(填字母)。
A.淡黄色 固体露置于空气中,逐渐变成白色 固体露置于空气中,逐渐变成白色 |
| B.用强光照射氯水,一段时间后溶液变成无色 |
| C.向氯水中滴加KI溶液,溶液变成棕黄色 |
D.向 溶液中滴加 溶液中滴加 溶液,产生红褐色沉淀 溶液,产生红褐色沉淀 |
 。该反应中氧化产物为
。该反应中氧化产物为(3)已知下列三个氧化还原反应:
①
 ;
;②
 ;
;③
 (浓)
(浓) 。
。若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的(4)无水情况下,
 可以和
可以和 发生如下反应:
发生如下反应:_______
 _______
_______ _______Fe+_______
_______Fe+_______ _______
_______ _______
_______
配平上述反应方程式,单线桥法标出电子转移的方向和数目
(5)向含有
 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 溶液,结果溶液变为红色。已知:还原性:
溶液,结果溶液变为红色。已知:还原性: ;则下列叙述中正确的是
;则下列叙述中正确的是①氧化性:
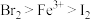
②原溶液中
 一定被氧化
一定被氧化③通入氯气后,原溶液中的
 定被氧化
定被氧化④不能确定通入氯气后的溶液中是否还存在

(6)下列转化中,不需要加入还原剂或氧化剂就能实现的是_______(填字母)。
A. | B. |
C. | D. |
 反应中被还原和被氧化的N原子数之比为
反应中被还原和被氧化的N原子数之比为
您最近一年使用:0次
6 . 阅读下列科普短文,利用所学化学知识回答下列问题.
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理.利用混凝剂 可除去天然水中的悬浮物.
可除去天然水中的悬浮物. 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注.
备受关注. 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景.
具有广阔的应用前景.
(1)混凝剂 在水中电离产生的阴离子是
在水中电离产生的阴离子是____________ .
(2)氯水中含有____________ 种分子,其中决定氯水颜色的分子是(填分子式)____________ .
(3) 与
与 的关系是互为
的关系是互为____________ ,等质量的 和
和 的分子数之比为
的分子数之比为____________ .
(4) 胶体可以与
胶体可以与 溶液反应,化学方程式为
溶液反应,化学方程式为____________ 。
(5) 溶于水反应的离子方程式:
溶于水反应的离子方程式: ,当生成标准状况下
,当生成标准状况下 的体积为
的体积为 时,反应中共转移电子
时,反应中共转移电子____________  .
.
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理.利用混凝剂
 可除去天然水中的悬浮物.
可除去天然水中的悬浮物. 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注.
备受关注. 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景.
具有广阔的应用前景.(1)混凝剂
 在水中电离产生的阴离子是
在水中电离产生的阴离子是(2)氯水中含有
(3)
 与
与 的关系是互为
的关系是互为 和
和 的分子数之比为
的分子数之比为(4)
 胶体可以与
胶体可以与 溶液反应,化学方程式为
溶液反应,化学方程式为(5)
 溶于水反应的离子方程式:
溶于水反应的离子方程式: ,当生成标准状况下
,当生成标准状况下 的体积为
的体积为 时,反应中共转移电子
时,反应中共转移电子 .
.
您最近一年使用:0次
解题方法
7 . 利用元素的化合价推测物质的性质是化学研究的重要于段。下图是铁元素的“价—类”二维图,完成下列问题:
Fe2O3属于___________ 氧化物(填“酸性”“碱性”或“两性”)。
(2)物质的制备及转化:
Fe(OH)2的制备:在FeSO4溶液中加入NaOH溶液,生成白色沉淀。但是白色沉淀迅速变成灰绿色,一段时间后变成红褐色物质,用化学方程式表示后续颜色变化的原因:___________ 。
(3)物质的检验:
将固体FeCl2溶于盐酸中,滴加KSCN,再逐滴加入氯水,溶液由无色变为___________ ,若继续滴加氯水至过量发现溶液颜色褪去,试分析溶液颜色褪去的原因可能是___________ 。
(4)物质的应用:
高铁酸钾(K2FeO4)是紫色光泽的微细结晶粉末,常用于高铁列车车厢里的一种“绿色环保高效”消毒剂,说明高铁酸钾具有很强的______ 性。

Fe2O3属于
(2)物质的制备及转化:
Fe(OH)2的制备:在FeSO4溶液中加入NaOH溶液,生成白色沉淀。但是白色沉淀迅速变成灰绿色,一段时间后变成红褐色物质,用化学方程式表示后续颜色变化的原因:
(3)物质的检验:
将固体FeCl2溶于盐酸中,滴加KSCN,再逐滴加入氯水,溶液由无色变为
(4)物质的应用:
高铁酸钾(K2FeO4)是紫色光泽的微细结晶粉末,常用于高铁列车车厢里的一种“绿色环保高效”消毒剂,说明高铁酸钾具有很强的
您最近一年使用:0次
2024-02-02更新
|
99次组卷
|
2卷引用:湖南省益阳市2023-2024学年高一上学期期末质量检测化学试题
名校
解题方法
8 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的化学方程式___________ ;实验室用___________ 除去混在氯气中的氯化氢杂质,用___________ 除去混在里面的水蒸气;
②写出次氯酸分解的化学反应方程式___________ ;新制氯水中使其呈现黄绿色的微粒是___________ ;使紫色石蕊溶液显红色的微粒是___________ ;能使红色布条褪色的微粒是___________ 。(填化学式)
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):________ ;
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应_____________ 。
______Cl2+______OH-=______Cl-+1ClO-+3ClO +______H2O
+______H2O
(1)①写出实验室中制取氯气的化学方程式
②写出次氯酸分解的化学反应方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应______Cl2+______OH-=______Cl-+1ClO-+3ClO
 +______H2O
+______H2O
您最近一年使用:0次
名校
9 . 核心知识的准确记忆、巩固是学好化学最重要、最基础的环节。按要求回答:
(1)气体摩尔体积的单位是__________ ;
(2)物质的量浓度(c)与质量分数( )的换算公式:
)的换算公式: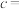
__________ ;(摩尔质量用M表示,密度 的单位为
的单位为 )
)
(3)蒸馏装置中温度计水银球的位置处于__________ ;
(4)容量瓶和分液漏斗使用前都必须进行的操作是__________ ;
(5)利用焰色反应检验物质,钾元素的焰色是__________ ;
(6) 的电离方程式为
的电离方程式为__________ ;
(7)氯气与水反应的化学方程式为__________ ;
不考虑物质挥发,新制氯水久置后导电能力变__________ (填“强或弱”)。
(8)下列溶液中 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。
(1)气体摩尔体积的单位是
(2)物质的量浓度(c)与质量分数(
 )的换算公式:
)的换算公式: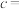
 的单位为
的单位为 )
)(3)蒸馏装置中温度计水银球的位置处于
(4)容量瓶和分液漏斗使用前都必须进行的操作是
(5)利用焰色反应检验物质,钾元素的焰色是
(6)
 的电离方程式为
的电离方程式为(7)氯气与水反应的化学方程式为
不考虑物质挥发,新制氯水久置后导电能力变
(8)下列溶液中
 与
与 溶液中的
溶液中的 相等的是__________。
相等的是__________。A. 的 的 溶液 溶液 | B. 的 的 溶液 溶液 |
C.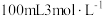 的 的 溶液 溶液 | D. 的 的 溶液 溶液 |
您最近一年使用:0次
10 . 氯化钠是日常生活必需品和重要的化工原料。
(1)生理盐水是浓度约为_______ 的NaCl溶液。
(2)写出NaCl溶于水时的电离方程式_______ 。
(3)以电解饱和食盐水为基础,生产一系列含氯、含钠化工产品的工业称为_______ 工业。该方法制得的烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法_______ 。
“洁厕灵”含有浓度较高的盐酸,可以清除污垢,除去异味。
(4)“洁厕灵”能轻松除去铁制品表面的铁锈(Fe2O3),但不能长时间浸泡,用化学方程式表示原因:_______ 、_______ 。
(5)“84消毒液”的有效成分为次氯酸钠,具有漂白、消毒、杀菌等作用。若与“洁厕灵”混用,易产生一种有毒气体,该反应的化学方程式为:_______ 。
(6)实验室通常用向上排空气法收集HCl。设计一个简单实验,验证如图所示的试管收集的HCl气体中是否含有空气_______ 。

(1)生理盐水是浓度约为
| A.0.9% | B.9% | C.7.5% | D.75% |
(2)写出NaCl溶于水时的电离方程式
(3)以电解饱和食盐水为基础,生产一系列含氯、含钠化工产品的工业称为
“洁厕灵”含有浓度较高的盐酸,可以清除污垢,除去异味。
(4)“洁厕灵”能轻松除去铁制品表面的铁锈(Fe2O3),但不能长时间浸泡,用化学方程式表示原因:
(5)“84消毒液”的有效成分为次氯酸钠,具有漂白、消毒、杀菌等作用。若与“洁厕灵”混用,易产生一种有毒气体,该反应的化学方程式为:
(6)实验室通常用向上排空气法收集HCl。设计一个简单实验,验证如图所示的试管收集的HCl气体中是否含有空气

您最近一年使用:0次



