名校
解题方法
1 . 实验室制备的 中会混有HCl,某同学设计了如图所示的实验装置进行验证,按要求回答下列问题。
中会混有HCl,某同学设计了如图所示的实验装置进行验证,按要求回答下列问题。

(1)实验室利用 制备
制备 反应的离子方程式为
反应的离子方程式为_____ 。
(2)所需实验装置从左至右的连接顺序为_____ 。
(3)装置③中Cu的作用_____ (用化学方程式表示)。
(4)有同学提出该装置存在缺陷,为排除干扰,在气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入 溶液中的气体只有一种,装置⑤中应放入
溶液中的气体只有一种,装置⑤中应放入_____ 。
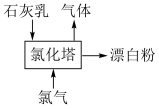
(5)工业利用氯气生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为_____ 。实际生产中,将石灰乳(含有3%-6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是_____ 。
 中会混有HCl,某同学设计了如图所示的实验装置进行验证,按要求回答下列问题。
中会混有HCl,某同学设计了如图所示的实验装置进行验证,按要求回答下列问题。
(1)实验室利用
 制备
制备 反应的离子方程式为
反应的离子方程式为(2)所需实验装置从左至右的连接顺序为
(3)装置③中Cu的作用
(4)有同学提出该装置存在缺陷,为排除干扰,在气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入
 溶液中的气体只有一种,装置⑤中应放入
溶液中的气体只有一种,装置⑤中应放入(5)工业利用氯气生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为

您最近一年使用:0次
2023-12-19更新
|
353次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2023-2024学年高一上学期12月月考化学试题
名校
解题方法
2 . 下列离子方程式书写正确的是
A.向澄清石灰水中加入过量 溶液: 溶液: |
B.将足量 通入到 通入到 的溶液中: 的溶液中: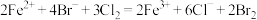 |
C.将 通入石灰乳中制漂白粉: 通入石灰乳中制漂白粉: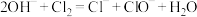 |
D.用白醋除铁锈: |
您最近一年使用:0次
名校
解题方法
3 . 下列有关化学现象的描述中正确的是
| A.氢气在氯气中燃烧产生苍白色的火焰,在瓶口出现白烟 |
| B.钠在氧气中燃烧,产生黄色的火焰,生成淡黄色的固体 |
| C.向氯水中滴加紫色石蕊溶液,溶液变为红色 |
D.氯气与过量的铁在点燃条件下反应生成 |
您最近一年使用:0次
4 . 氯化铁(FeCl3)是一种易潮解、易升华的无机化工产品。某同学在实验室制备氯气(Cl2),并用干燥纯净的氯气与 反应制备
反应制备 ,装置如图所示(部分夹持仪器已省略):
,装置如图所示(部分夹持仪器已省略):
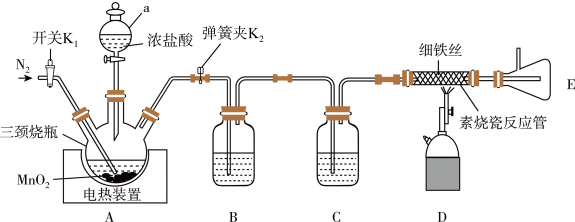
回答下列问题:
(1)仪器a的名称是___________ ,装置B、C装的试剂分别是___________ 、___________ 。
(2)写出三颈烧瓶中反应的离子方程式___________ 。
(3)实验开始前需要通入一段时间N2,其目的是___________ 。
(4)该装置存在的不足之处是___________ ,改进方法中需要用到的试剂为___________ 。
A.浓硫酸 B.无水CaCl2 C.无水硫酸铜 D.碱石灰
 反应制备
反应制备 ,装置如图所示(部分夹持仪器已省略):
,装置如图所示(部分夹持仪器已省略):
回答下列问题:
(1)仪器a的名称是
(2)写出三颈烧瓶中反应的离子方程式
(3)实验开始前需要通入一段时间N2,其目的是
(4)该装置存在的不足之处是
A.浓硫酸 B.无水CaCl2 C.无水硫酸铜 D.碱石灰
您最近一年使用:0次
2023-12-12更新
|
282次组卷
|
2卷引用:重庆市广益中学校2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
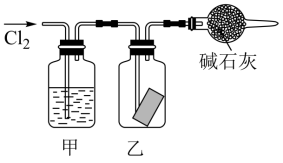
5 . 将一定量 通过甲装置后,再通过放有湿润红色布条的乙装置,红色布条不褪色。甲装置中所盛试剂可能是
通过甲装置后,再通过放有湿润红色布条的乙装置,红色布条不褪色。甲装置中所盛试剂可能是
①浓硫酸 ②NaOH溶液 ③纯碱溶液 ④饱和食盐水 ⑤KI溶液
 通过甲装置后,再通过放有湿润红色布条的乙装置,红色布条不褪色。甲装置中所盛试剂可能是
通过甲装置后,再通过放有湿润红色布条的乙装置,红色布条不褪色。甲装置中所盛试剂可能是①浓硫酸 ②NaOH溶液 ③纯碱溶液 ④饱和食盐水 ⑤KI溶液

| A.①④⑤ | B.①②③ | C.②③④ | D.②③⑤ |
您最近一年使用:0次
2023-12-11更新
|
99次组卷
|
2卷引用:山东省莱西市第一中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 某同学在pH试纸上滴几滴新制氯水,现象如图所示,下列有关该实验的说法中正确的是


A.该实验说明 分子具有漂白性 分子具有漂白性 | B.若用久置的氯水进行实验,现象相同 |
C.该实验说明 扩散速度比HClO分子快 扩散速度比HClO分子快 | D.将新制氯水放置几天后溶液酸性减弱 |
您最近一年使用:0次
2023-12-03更新
|
318次组卷
|
6卷引用:山东省莱阳市第一中学2023-2024学年高一上学期10月月考化学试题
山东省莱阳市第一中学2023-2024学年高一上学期10月月考化学试题山东省泰安市2022-2023学年高一上学期11月期中考试化学试题安徽省2023-2024学年高一上学期期中联考化学试题(已下线)专题02 海水中的重要元素——钠和氯-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)宁夏银川市唐徕中学2023-2024学年高一上学期期中考试化学试题山东省泰安市宁阳县第四中学2023-2024学年高一上学期期中考试化学试题
7 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②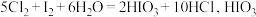 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②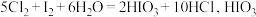 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是
A.还原性: |
B.b点溶液中 |
C.a点时已通入标准状况下氯气的总体积为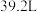 |
D.c点溶液中阴离子的个数为 |
您最近一年使用:0次
2023-12-01更新
|
928次组卷
|
4卷引用:河北省河北正中实验中学2023-2024学年高一上学期月考三化学试题
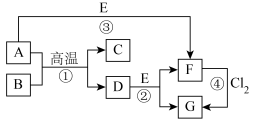
8 . 部分元素的单质及其化合物(或其溶液)的转化关系如图。已知A是生活中使用广泛的金属单质,常温下B是无色无味的液体,E是胃酸的主要成分。
(1)写出下列物质的化学式:E_______ ;G_______ 。
(2)反应①的化学方程式为_______ ;反应②的离子方程式为_______ 。
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为_______ (填离子符号),下列实验操作及现象能证明溶液中含有该金属阳离子的是_______ (填标号),反应④中氧化剂和还原剂的物质的量之比为_______ 。
a.取样,滴加氯水后滴加 ,溶液变红
,溶液变红
b.取样,滴加 溶液,产生白色沉淀,白色沉淀迅速变成灰绿色,最终变成红褐色
溶液,产生白色沉淀,白色沉淀迅速变成灰绿色,最终变成红褐色
c.取样,加入铜粉,无明显现象
(4)写出C在生产、生活中的一种用途:_______ 。
(1)写出下列物质的化学式:E
(2)反应①的化学方程式为
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为
a.取样,滴加氯水后滴加
 ,溶液变红
,溶液变红b.取样,滴加
 溶液,产生白色沉淀,白色沉淀迅速变成灰绿色,最终变成红褐色
溶液,产生白色沉淀,白色沉淀迅速变成灰绿色,最终变成红褐色c.取样,加入铜粉,无明显现象
(4)写出C在生产、生活中的一种用途:
您最近一年使用:0次
2023-12-01更新
|
443次组卷
|
2卷引用:河北省邢台市质检联盟2023-2024学年高一上学期11月月考化学试题
名校
9 . 下列方案设计、现象和结论正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 比较 和 和 溶液碱性强弱 溶液碱性强弱 | 同温下,向等浓度的两溶液中分别滴入3滴酚酞,观察现象 | 观察到红色较深的是 ,说明碱性 ,说明碱性 大于 大于 |
| B | 区别 和 和 固体 固体 | 分别在两支试管中分别加入少量待检验固体,再加入几滴水,用温度计测定变化 | 温度升高的是 固体,温度降低的是 固体,温度降低的是 固体 固体 |
| C | 检验纯碱溶液中是否存在NaCl | 向待测液中加入 溶液,观察现象 溶液,观察现象 | 若有白色沉淀产生,则溶液中存在 |
| D | 检验 是否有漂白性 是否有漂白性 | 将干燥的 通入装有潮湿有色布条的广口瓶中,观察现象 通入装有潮湿有色布条的广口瓶中,观察现象 | 若有色布条颜色逐渐褪去,则说明 有漂白性 有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-29更新
|
596次组卷
|
3卷引用:浙江省杭州市富阳区实验中学2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
10 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
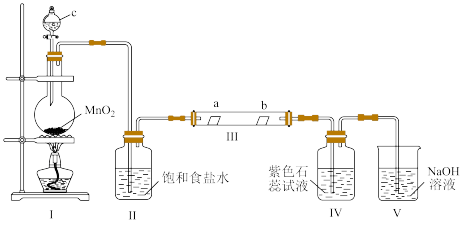
(1)装置Ⅰ中仪器c的名称是_______ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式,为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象_______ 。
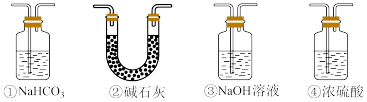
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有_______ 。
(6)常温下装置Ⅴ反生反应的离子方程式为_______ 。
(7)有一种“地康法”制取氯气的反应原理如图所示:
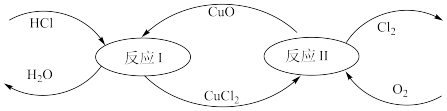
在450℃条件下,反应Ⅱ的化学方程式为_______ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)实验结束后,欲回收利用装置Ⅰ中未反应完的
 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有(6)常温下装置Ⅴ反生反应的离子方程式为
(7)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
2023-11-29更新
|
228次组卷
|
3卷引用:广东省惠州市惠州一中2023-2024学年高一上学期第二次阶段性考试化学试卷



